Resumen
- La vitamina D puede ser sintetizada en la piel después de exponerse a la luz solar y es entonces metabolizada en el hígado y riñón a la metabólicamente forma activa llamada 1α,25-dihidroxivitamina D. A través de la unión al receptor de la vitamina D (RVD), la 1α,25-dihidroxivitamina D puede regular la expresión de cientos de genes involucrados en funciones del esqueleto y otras funciones biológicas. (Más información)
- La vitamina D es esencial para el mantenimiento de la mineralización ósea a través de la regulación de calcio y homeostasis del fósforo. La vitamina D también exhibe muchos efectos no-esqueléticos, particularmente en los sistemas inmune, endocrino, y cardiovascular. (Más información)
- La vitamina D es importante para el desarrollo y mantenimiento óseo normal. Una deficiencia severa de vitamina D causa raquitismo en niños y osteomalacia en adultos. (Más información)
- El hiperparatiroidismo secundario debido a la insuficiencia de vitamina D puede incrementar la degradación ósea y precipitar la osteoporosis. Ensayos clínicos aleatorios indican que la suplementación con al menos 800 UI/día de vitamina D puede reducir el riesgo de caídas y fracturas en individuos de edad avanzada. (Más información)
- La vitamina D puede regular la diferenciación celular y crecimiento al unirse al receptor de la vitamina D encontrado en la mayoría de las células del cuerpo. Estudios basados en la observación han reportado asociaciones entre la baja exposición al sol, un estatus pobre de la vitamina D, y el riesgo incrementado de desarrollar cáncer colorrectal y de seno. Ensayos clínicos aleatorios son necesarios para evaluar si la prevención de cáncer podría beneficiarse de la suplementación de vitamina D. (Más información)
- Varios estudios basados en la observación han reportado asociaciones inversas entre el estatus de la vitamina D y la susceptibilidad o severidad de enfermedades autoinmunes, incluyendo la diabetes mellitus tipo 1, esclerosis múltiple, artritis reumatoides, y lupus eritematoso sistémico. (Más información)
- Evidencia actual proveniente de estudios basados en la observación sugiere una relación inversa entre las concentraciones circulantes de vitamina D y el riesgo de diabetes mellitus tipo 2. Aún no se conoce si corrigiendo la deficiencia de vitamina D en individuos con intolerancia a la glucosa puede disminuir el riesgo de la progresión a diabetes tipo 2. (Más información)
- Ensayos clínicos aleatorios están actualmente investigando si la suplementación con vitamina D puede limitar el deterioro cognitivo y progresión de la enfermedad en individuos con enfermedades neurodegenerativas. (Más información)
- La insuficiencia de vitamina D en mujeres embarazadas puede estar asociada con varios efectos adversos para la madre y el recién nacido. La seguridad y beneficios de la suplementación con vitamina D durante el embarazo necesitan ser evaluados en ensayos clínicos. (Más información)
- Estudios observacionales han documentado una asociación entre la deficiencia de vitamina D y una mayor incidencia y gravedad de la enfermedad por coronavirus, COVID-19. (Más información)
- Estudios preliminares han demostrado que la suplementación con vitamina D puede ofrecer mejoras prometedoras en el tratamiento de la dermatitis atópica (eccema) y la enfermedad de Crohn. (Más información)
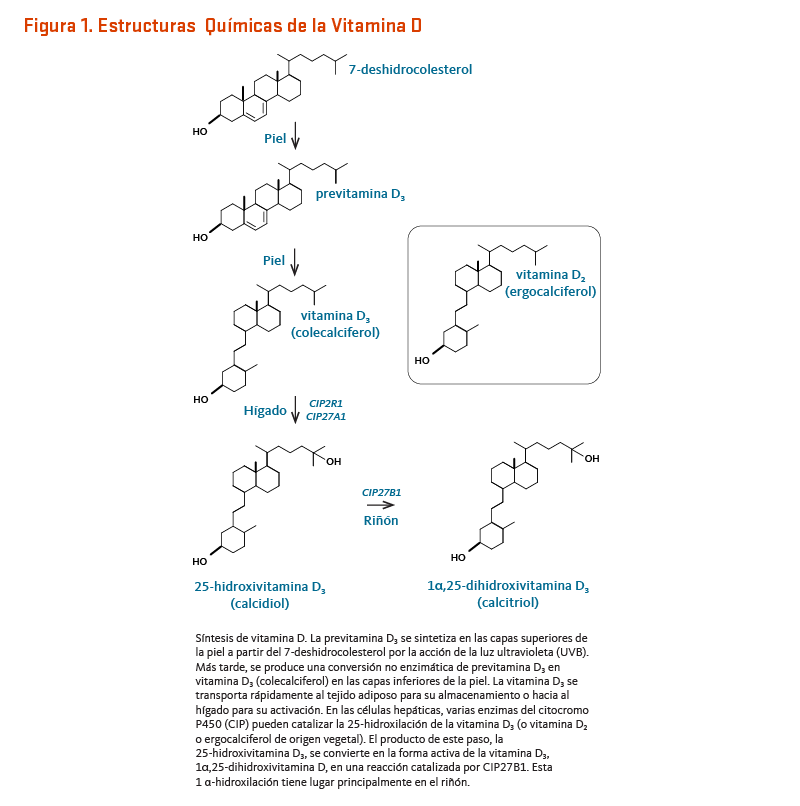
La vitamina D es una vitamina liposoluble que regula la homeostasis del calcio y es vital para la salud ósea (1). Mientras que esta puede ser también obtenida de fuentes dietéticas o suplementos, la vitamina D3 (colecalciferol) es sintetizada en la piel humana a partir de la conversión del 7-dehidrocolesterol luego de la exposición a la radiación ultravioleta-B (UVB) de la luz solar. La vitamina D2 (ergocalciferol) es una vitamina D análoga fotosintetizada en plantas, hongos, y levaduras; la vitamina D2 es también utilizada en la fortificación de alimentos con vitamina D (2). Cuando la vitamina D3 en la piel es inadecuada debido a insuficiente exposición a la radiación UVB, la ingesta oral de vitamina D es necesaria Fpara satisfacer los requerimientos de vitamina D.
Función
Metabolismo de la vitamina D
El colecalciferol y ergocalciferol son precursores biológicamente inactivos de la vitamina D y deben ser convertidos a formas biológicamente activas en el hígado y riñones (Figura 1). De hecho, luego de la ingesta dietética o síntesis en la epidermis de la piel después de la exposición a la radiación UVB, ambas formas de la vitamina D entran en la circulación y son transportadas al hígado por la proteína de unión a vitamina D (y en menor medida por la albúmina). En los hepatocitos (células del hígado), la vitamina D es hidroxilada para formar 25-hidroxivitamina D (calcidiol; calcifediol). La exposición a la luz solar o la ingesta dietética de vitamina D incrementan las concentraciones en suero de 25-hidroxivitamina D. La 25-hidroxivitamina D constituye la principal forma de vitamina D circulante, y la suma de los niveles de 25-hidroxivitamina D2 y 25-hidroxivitamina D3 en el suero es usada como un indicador del estatus nutricional de la vitamina D (3). La enzima renal 25-hidroxivitamina D-1α-hidroxilasa (también conocida como CYP27B1) eventualmente cataliza una segunda hidroxilación que convierte a la 25-hidroxivitamina D en 1α,25-hidroxivitamina D (calcitriol). La producción de 1α,25-dihidroxivitamina D en los riñones es regulada por varios factores, incluyendo el fósforo, calcio, hormona paratiroidea (PTH), el factor de crecimiento de fibroblastos 23 (FGF-23), y la propia 1α,25-dihidroxivitamina D del suero. Mientras que los riñones son la fuente principal de la actividad de la 1α-hidroxilasa, la producción externo-renal de 1α-dihidroxivitamina D ha sido también demostrada en una variedad de tejidos, incluyendo la piel, glándula paratiroidea, senos, colon, próstata, como también en células del sistema inmunológico y células óseas (2). La mayoría de los efectos fisiológicos de la vitamina D en el cuerpo están relacionados a la actividad de 1α,25-dihidroxivitamina D (4). Varias formas de la vitamina D están listadas en Figura 1.
[Figura 1 - Clic para Agrandar]
Mecanismos de acción
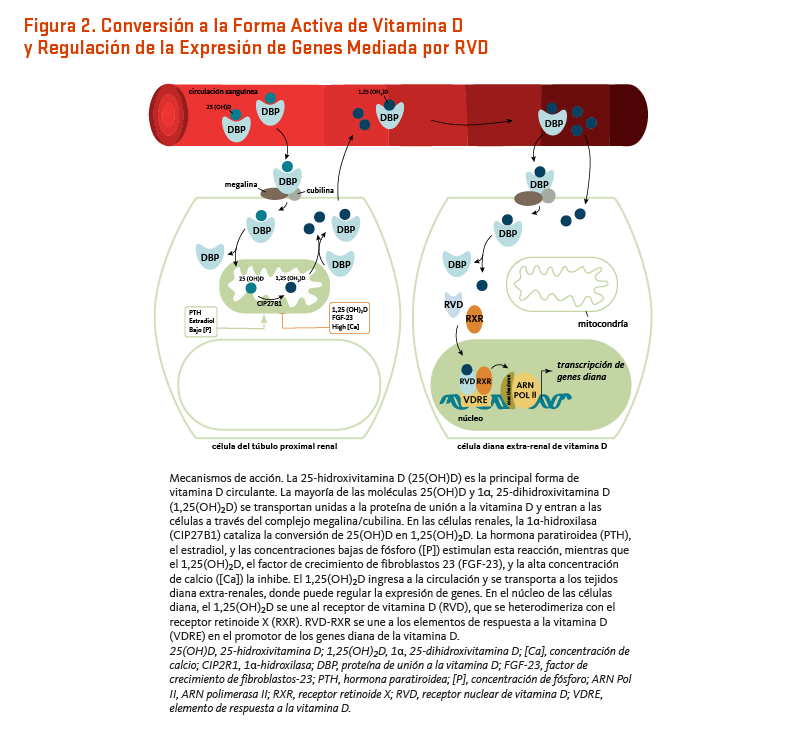
La mayoría, sino todas, las acciones de la vitamina D son mediadas a través de un factor de transcripción nuclear conocido como receptor de vitamina D (RVD) (Figura 2) (5). Al entrar al núcleo de una célula, la 1α,25-dihidroxivitamina D se une al RVD y recluta otro receptor nuclear conocido como receptor del ácido retinoico X (RXR). En la presencia de 1α,25-dihidroxivitamina D, el complejo RVD/RXR se une a pequeñas secuencias de ADN conocidas como elementos de respuesta a vitamina D (VDREs) e inicia una cascada de interacciones moleculares que modulan la transcripción de genes específicos. Miles de VDREs han sido identificados a través del genoma, y se piensa que la activación del RVD por la 1α,25-dihidroxivitamina D directamente y/o indirectamente regula de entre 100 a 1,250 genes (6).
[Figura 2 - Clic para Agrandar]
Balance de calcio
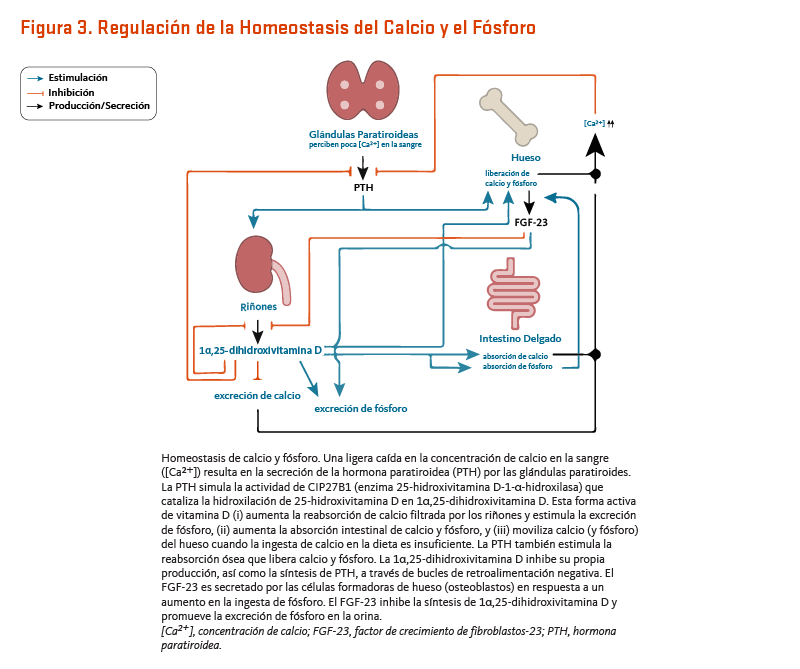
El mantenimiento del calcio en el suero dentro de un rango estrecho es vital para el funcionamiento normal del sistema nervioso, como también para el crecimiento óseo y mantenimiento de la densidad ósea. La vitamina D es esencial para la utilización eficiente del calcio por el cuerpo (1). Las glándulas paratiroideas captan las concentraciones de calcio en el suero y secretan la hormona paratiroidea (PTH) si las concentraciones de calcio disminuyen por debajo de lo normal (Figura 3). Incrementos en la PTH estimulan la actividad de la enzima 25-hidroxivitamina D3-1α-hidroxilasa en el riñón, resultando en una producción incrementada de 1α,25-hidroxivitamina D. La forma activa de vitamina D, 1α,25-hidroxivitamina D, se libera en la circulación y se transporta a los tejidos objetivo. Dentro de las células diana, la 1α,25-dihidroxivitamina se une e induce la activación de RVD, lo que conduce a cambios en la expresión génica que normalizan el calcio sérico al (1) aumentar la absorción intestinal de calcio dietético, (2) aumentar la reabsorción de calcio filtrado por los riñones, y (3) movilizando calcio del hueso cuando no hay suficiente calcio dietético para mantener las concentraciones normales de calcio en suero (7).
[Figura 3 - Clic para Agrandar]
Balance del fósforo
Las regulaciones del calcio y homeostasis del fósforo están estrechamente relacionadas, y las hormonas calciotrópicas de la PTH y la 1α,25-hidroxivitamina D pueden también controlar el fósforo del suero. Específicamente, la 1α,25-hidroxivitamina D incrementa la absorción intestinal de fósforo al estimular la expresión de un cotransportador sodio-fosfato en el intestino delgado. Mientras que la PTH incrementa la excreción urinaria de fósforo al reducir la reabsorción en el riñón, aún no es claro si la 1α,25-dihidroxivitamina D puede directamente regular el transporte renal de fósforo. La hormona fosfatúrica del factor de crecimiento fibroblástico 23 (FGF-23), secretada por los osteoblastos (células formadoras de hueso), limita la producción de la 1,25-hidroxivitamina D al inhibir la 25-hidroxivitamina D-1α-hidroxilasa (Figura 3) (revisado en 8).
Diferenciación celular
Se dice que las células que se dividen rápidamente son células en proliferación. La diferenciación resulta en la especialización de células para funciones específicas. En general, la diferenciación celular lleva a una disminución en la proliferación. Mientras que la proliferación celular es esencial para el crecimiento y cicatrización de heridas, la proliferación incontrolada de células con ciertas mutaciones puede llevar al cáncer. La forma activa de la vitamina D, 1α,25-dihidroxivitamina D inhibe la proliferación y estimula la diferenciación de las células mediante su unión al RVD (1).
Inmunidad
Actuando a través del RVD la 1α,25-dihidroxivitamina D es un potente modulador del sistema inmune. El RVD es expresado por la mayoría de las células del sistema inmune, incluyendo las células T regulatorias y las células presentadoras de antígeno, como las células dendríticas y macrófagos (9). Bajo circunstancias específicas, los monocitos, macrófagos, y células T pueden expresar la enzima 25-dihidroxivitamina D3-1α-hidroxilasa y producir 1α,25-dihidroxivitamina D, la cual actúa localmente para regular la respuesta inmune (10, 11). Existe evidencia científica considerable que la 1α,25-dihidroxivitamina D posee una variedad de efectos en la función del sistema inmune, que podrían mejorar la inmunidad innata e inhibir el desarrollo de la autoinmunidad (12). Inversamente, la deficiencia de vitamina D puede comprometer la integridad del sistema inmunológico y conducir a respuestas inmunes inapropiadas (véase Enfermedades autoinmunes).
Secreción de insulina
El RVD es expresado por las células secretoras de insulina del páncreas, y los resultados de estudios en animales sugieren que la 1α,25-dihidroxivitamina D desempeña un papel en la secreción de insulina bajo condiciones de un incremento de la demanda de insulina (13, 14). Estudios prospectivos y de corte transversal sugieren que niveles insuficientes de vitamina D pueden tener un efecto adverso en la secreción de insulina y tolerancia a la glucosa en la diabetes mellitus tipo 2 (diabetes mellitus no dependiente de insulina) (revisado en 15).
Regulación de la presión sanguínea
El sistema renina-angiotensina juega un papel importante en la regulación de la presión sanguínea (16). La renina es una enzima que cataliza el clivaje (separación) de un péptido pequeño (angiotensina I) de una proteína más grande (angiotensinógeno) producida en el hígado. La enzima convertidora de angiotensina (ECA) cataliza el clivaje de la angiotensina I para formar angiotensina II, un péptido que puede incrementar la presión sanguínea al inducir la constricción de pequeñas arterias y al incrementar la retención de sodio y agua. La tasa de síntesis de angiotensina II es dependiente de la renina (17). Investigación en ratones sin el gen que codifica para el RVD, indica que la 1α,25-dihidroxivitamina D disminuye la expresión del gen que codifica para la renina a través de su interacción con el RVD (18). Ya que la activación inapropiada del sistema renina-angiotensina puede contribuir al desarrollo de hipertensión, alcanzar niveles adecuados de vitamina D podría ser importante para disminuir el riesgo de presión sanguínea alta (véase Hipertensión).
Deficiencia
En la deficiencia de vitamina D, la absorción de calcio no puede ser incrementada lo suficiente para satisfacer las necesidades de calcio del cuerpo (4). En consecuencia, la producción de la PTH por las glándulas paratiroideas es incrementada y calcio es movilizado del esqueleto para mantener niveles normales de calcio en el suero — una condición conocida como hiperparatiroidismo secundario. A pesar de que hace mucho tiempo se sabe que la deficiencia severa de vitamina D tiene consecuencias serias para la salud ósea, investigaciones sugieren que estados menos obvios de deficiencia de vitamina D son comunes, e incrementan el riesgo de osteoporosis y otros problemas de salud (véase Prevención de Enfermedad).
Severa deficiencia de vitamina D
Raquitismo
En infantes y niños la deficiencia severa de vitamina D resulta en el fracaso de la mineralización de los huesos. El proceso de mineralización, que involucra la producción de cristales de fosfato de calcio por las células formadoras de hueso, determina la dureza y resistencia de los huesos. La deficiencia de vitamina D severamente afecta los huesos que crecen rápidamente. Las placas de crecimiento de los huesos continúan alargándose, pero en la ausencia de una mineralización adecuada, los miembros que soportan el peso (brazos y piernas) se arquean. En infantes, el raquitismo podría resultar en un retraso en el cierre de las fontanelas (partes blandas) en el cráneo, y la caja torácica podría deformarse debido a la acción de arrastre del diafragma. En casos severos, bajos niveles de calcio en el suero (hipocalcemia) podrían causar convulsiones. Aunque la fortificación de alimentos ha llevado a la complacencia con respecto a la deficiencia de vitamina D, en ciudades alrededor del mundo aún se reportan casos de raquitismo nutricional (19, 20).
Osteomalacia
Aunque los huesos adultos no están más en crecimiento, estos están en un constante estado de renovación, o "remodelación." En adultos con una deficiencia severa de vitamina D, la matriz de colágeno del hueso se conserva, pero el mineral óseo se pierde progresivamente, resultando en el ablandamiento de huesos (osteomalacia), dolor de huesos, y un incremento en el riesgo de osteoporosis (21).
Debilidad y dolor muscular
La deficiencia de vitamina D causa debilidad y dolor muscular en niños y adultos. El dolor y la debilidad muscular fueron los síntomas prominentes de la deficiencia de vitamina D en un estudio en mujeres musulmanas árabes y danesas viviendo en Dinamarca (22). En un estudio de corte transversal en 150 pacientes consecutivos remitidos a una clínica en Minnesota para la evaluación de dolor musculoesquelético persistente, no especifico, el 93% tuvieron niveles de 25-hidroxivitamina D en el suero iguales o por debajo de los 20 ng/mL, con una concentración media de 12.1 ng/mL, lo cual es un indicativo de la insuficiencia de vitamina D (23). La pérdida de fuerza muscular contribuye en gran medida al incremento del riesgo de caídas y fracturas de hueso, especialmente en personas mayores (24). Además, la insuficiencia de vitamina D a largo plazo puede ser un factor contribuidor a la osteoporosis en los ancianos (véase Osteoporosis).
Factores de riesgo de la deficiencia de vitamina D
Tanto los factores ambientales como las prácticas culturales dan como resultado variaciones en el estatus de la vitamina D:
- Condiciones ambientales: Ubicaciones geográficas, incluyendo latitud y altitudes, y condiciones atmosféricas (p. ej., contaminación del aire, presencia de nubes) influyen en gran medida a la intensidad de la radiación UVB que alcanza el suelo. Cambios estacionales también afectan la calidad y cantidad de los rayos UVB y de este modo la producción de vitamina D en la piel (25-27).
- Estilo de vestimenta cubierta: En un estudio de 2,032 en mujeres del Medio Oriente, que vistieron un velo en la cabeza o cubrieron toda la piel por razones religiosas o culturales, el 96% tuvieron niveles de 25-hidroxivitamina D en el suero por debajo de los 20 ng/mL, y el 60% tuvieron niveles de vitamina D por debajo de los 12 ng/mL (28). El raquitismo y osteomalacia no son comunes en las regiones del Medio Oriente y Norte de África donde niños y mujeres cubren la mayoría de toda su piel cuando salen al exterior (29).
- Medidas de protección solar: Las prácticas de protección solar, incluyendo el limitar la exposición al sol, vestir ropas protectoras y sombreros, y aplicar bloqueador solar, obstaculizan la exposición de la piel a la luz solar y por lo tanto dan lugar a una producción menor de vitamina D3 y metabolitos de la vitamina D circulantes a menos que haya una ingesta oral adecuada. Debe notarse que la aplicación de protector solar (2 mg/cm2) con un factor de protección solar (FPS) de 10 reduce la radiación UVB en un 90% (30).
- Infantes exclusivamente amamantados: Los infantes que son exclusivamente amamantados y no reciben suplementación con vitamina D están en un riesgo alto de deficiencia de vitamina D, particularmente si tienen la piel oscura y/o reciben poca exposición solar (19). La leche humana generalmente provee de entre 10-80 UI de vitamina D por litro (L), que corresponde a 0.2 a 1.5 μg/día (8-60 UI/día) cuando se usa un promedio diario de ingesta de leche de 0.75 L (25 oz) (31). La Academia Americana de Pediatría recomienda que todos los infantes amamantados y parcialmente amamantados les sea dado un suplemento de vitamina D de 400 UI/día (19). La suplementación materna de vitamina D durante el período de lactancia puede contribuir a un mejorado estatus de vitamina D en el infante que está siendo amamantado, especialmente en poblaciones con una prevalencia alta de deficiencia de vitamina D (32). Infantes mayores y niños pequeños que son alimentados exclusivamente con substitutos de la leche (p. ej., fórmulas a base de soya) y alimentos para el destete que no están fortificados con vitamina D están un riesgo de una deficiencia de vitamina D (33).
La eficiencia de la síntesis de vitamina D, absorción, y metabolismo también depende en una variedad de factores biológicos:
- Pigmentación de la piel: Las personas con una complexión oscura sintetizan menos vitamina D al exponerse a la luz solar que aquellos con un color de piel más claro (34). Una encuesta nacional estadounidense reportó niveles promedio de 25-hidroxivitamina D en el suero de 28.1 ng/mL, 21.6 ng/mL, y 16.9 ng/mL en mujeres caucásicas, méxico-americanas, y afroamericanas de ≥20 años de edad, respectivamente (25).
- Variaciones genéticas: Un estudio internacional, multicéntrico, de asociación del genoma completo (en inglés, GWAS) de 15 cohortes, que incluyó a ~ 30,000 participantes de ascendencia europea — conocido como el consorcio SUNLIGHT [Estudio de Determinantes Genéticos Subyacentes de la Vitamina D y Rasgos Altamente Relacionados] — identificó variaciones comunes (llamadas polimorfismos) en genes implicados en la síntesis de colesterol, la hidroxilación y el transporte de vitamina D que influyen en el estado de la vitamina D (35). Si bien los determinantes genéticos del bajo nivel de vitamina D se están identificando en poblaciones de origen europeo (36, 37) y asiático (38, 39), se necesitan estudios de asociación del genoma completo en poblaciones de ascendencia africana.
- Edad avanzada: Las personas de la tercera edad tienen una capacidad reducida para sintetizar vitamina D en la piel cuando se exponen a la radiación UVB y son más propensos a permanecer en interiores y usar bloqueador solar, lo cual previene la síntesis de vitamina D. Se ha estimado que a través de Canadá, los EE.UU., y Europa, la prevalencia de la deficiencia de vitamina D oscila entre 20%-100% en personas de la tercera edad que viven libremente (40). Por otra parte, adultos que se encuentran en instituciones y que no son suplementados con vitamina D están en un riesgo extremadamente alto de una deficiencia de vitamina D (41, 42).
- Enfermedad renal crónica (ERC): La deficiencia de vitamina D en pacientes con insuficiencia renal se debe a una síntesis reducida de 1α,25-dihidroxivitamina D y una mayor pérdida de 25-hidroxivitamina D en la orina (43).
- Síndromes de malabsorción de grasas: La deficiencia de vitamina D es común entre personas con fibrosis quística y con tanto enfermedades hepáticas colestásicas y no colestásicas debido a la disminución de la absorción de la vitamina D dietética y a la alteración de la conversión de vitamina D a 25-hidroxivitamina D (revisado en 44).
- Enfermedad inflamatoria intestinal: Las personas con una enfermedad intestinal inflamatoria como la enfermedad de Crohn parecen estar en un riesgo incrementado de una deficiencia de vitamina D, especialmente aquellas que han tenido resecciones intestinales pequeñas (45).
- Obesidad:
- La obesidad (índice de masa corporal ≥30 kg/m2) incrementa el riesgo de la deficiencia de vitamina D (46). Una vez la vitamina D es sintetizada en la piel o ingerida, esta puede ser secuestrada en los depósitos de grasa corporal, haciéndola menos biodisponible para las personas con una mayor masa corporal grasa. Por otra parte, ensayos de la suplementación de vitamina D han mostrado que las personas obesas alcanzaron niveles mucho más bajos de 25-hidroxivitamina D del suero en comparación a participantes con pesos normales (IMC <25 kg/m2) con dosis orales equivalentes (47).
- Deficiencia de magnesio: Recientes descubrimientos sugieren que altas ingestas de magnesio podrían reducir el riesgo de la insuficiencia de vitamina D. El magnesio regula la actividad de enzimas críticas en el metabolismo de la vitamina D, lo cual explicaría cómo la deficiencia de magnesio afecta negativamente el estatus de la vitamina D (48).
Evaluación del estado nutricional de vitamina D
La creciente toma de conciencia de que la deficiencia de vitamina D tiene serias consecuencias para la salud más allá del raquitismo y la osteomalacia; resalta la necesidad de una evaluación precisa del estatus nutricional de la vitamina D. Actualmente se entiende que la medida de la concentración total de la 25-hidroxivitamina D en el suero (1 ng/mL correspondiente a 2.5 nmol/L) es el mejor indicador para evaluar el estatus de la vitamina D.
Sin embargo, evidencia de alta calidad aún es necesaria para asegurar que los valores de corte actuales son óptimos para definir estados de insuficiencia y deficiencia (40). Además, sólo recientemente, se han realizado esfuerzos para la estandarización de los ensayos de 25-hidroxivitamina D desarrollados comercialmente y en laboratorio, de modo que las directrices se han desarrollado utilizando datos de investigación en gran medida no estandarizados (49). Aunque valores de referencia del laboratorio para los niveles suficientes de vitamina D se habían basado inicialmente en los niveles de 25-hidroxivitamina D del suero provenientes de cohortes de individuos saludables, estudios adicionales han sugerido que los valores de corte basados en la salud que apuntan a la prevención de hiperparatiroidismo secundario y pérdida ósea deberían ser considerablemente más altos. En efecto, mientras que se considera que las concentraciones de 25-hidroxivitamina D del suero menores a 8-10 ng/mL (20-25 nmol/L) indican una deficiencia severa asociada al raquitismo y osteomalacia, varios estudios han observado que los niveles de PTH (50, 51) y de la absorción de calcio (52) no fueron optimizados en relación a los niveles de 25-hidroxivitamina D del suero por debajo de los 32 ng/mL (80 nmol/L).
A pesar de todo, estudios más recientes han fallado en encontrar valores de umbral de las concentraciones de 25-hidroxivitamina D del suero en relación a la supresión de la PTH y la absorción óptima del calcio. Por una parte, el análisis de corte transversal reciente de 312,962 muestras clínicas no encontró evidencia de un umbral para la supresión de la PTH en la curva bien ajustada que muestra la asociación inversa entre las mediciones emparejadas de la PTH del suero y la 25-hidroxivitamina D, incluso con una concentración de 25-hidroxivitamina D más allá de los 70 ng/mL (175 nmol/L) (53). Esto contradijo un reciente análisis de la Encuesta Nacional de Examinación de Salud y Nutrición de los EE.UU. (NHANES 2003-2006) que estimó la supresión máxima de la PTH para las concentraciones de 25-hidroxivitamina D de 40 ng/mL (100 nmol/L) y mayores (54). Además, ambos estudios identificaron evidencia de hiperparatiroidismo leve (PTH sérica >65 pg/mL) en individuos con niveles de 25-hidroxivitamina D del suero mucho más allá de los 20 ng/mL (50 nmol/L), cuestionando el uso de PTH en el suero como un indicador razonable de la insuficiencia de vitamina D (53, 54). Por otra parte, un ensayo aleatorio controlado con placebo reciente en mujeres posmenopáusicas con una insuficiencia de vitamina D (25-hidroxivitamina D sérica <20 ng/mL) suplementadas con dosis diarias de vitamina D3 de entre 400 a 4,800 UI encontró poco cambio (6%) en la absorción de calcio sobre una concentración normal de 25-hidroxivitamina D con un rango de 20 a 66 ng/mL (55).
Los puntos de corte actuales propuestos por el Instituto de Medicina (en inglés, IOM) son los siguientes: como deficiencia valores de 25-hidroxivitamina D del suero ≤12 ng/mL (30 nmol/L); como insuficiencia valores de 25-hidroxivitamina D del suero de 12-19 ng/mL (30-49 nmol/L); y como suficiencia valores de 25-hidroxivitamina D del suero de 20-50 ng/mL (50-125 nmol/L) (56). Las ingestas dietéticas de referencia (REP, IDR) establecidas por el Instituto de Medicina están basadas en el logro de concentraciones de 25-hidroxivitamina D circulante (20-50 ng/mL) que son adecuadas para mantener la salud ósea y una óptima absorción de calcio (57).
Sin embargo, teniendo en cuenta el papel potencial de los niveles circulantes menores de 30 ng/mL en la carga de muchas enfermedades crónicas (6), la Sociedad de Endocrinología Estadounidense ha sugerido definir los valores de corte de la siguiente manera: como deficiencia valores de 25-hidroxivitamina D del suero ≤20 ng/mL (≤ 50 nmol/L); como insuficiencia valores de 25-hidroxivitamina D del suero de 21-29 ng/mL (51-74 nmol/L); como suficiencia valores de 25-hidroxivitamina D del suero de 30-100 ng/mL (75-250 nmol/L) (40). Sin embargo, este rango alternativo deseado es apoyado por algunos estudios basados en la observación, pero no está basado en datos de ensayos controlados aleatorios (véase Prevención de Enfermedad) (47). Con estos últimos valores de corte mencionados, estudios provenientes de todo el mundo han estimado que la hipovitaminosis D está bastante extendida y que niños y adultos de todas las edades están en un riesgo igual de insuficiencia y deficiencia (58). Datos de estudios de suplementación indican que las ingestas de vitamina D de por lo menos 800-1,000 UI/día son requeridas por adultos que viven en latitudes templadas para alcanzar niveles de 25-hidroxivitamina D del suero de por lo menos 30 ng/mL (75 nmol/L) (40).
Finalmente, las concentraciones totales de 25-hidroxivitamina en el suero pueden no siempre adecuadamente reflejar la biodisponibilidad de la vitamina D (59), y evidencia adicional es necesaria para mejorar la determinación del estatus de la vitamina D en diferentes poblaciones étnicas.
La IDR
En el 2010, la Junta de Nutrición y Alimentos (JNA) del Instituto de Medicina estableció una ingesta diaria recomendada (IDR) basada en la cantidad de vitamina D necesaria para la salud ósea. Mientras que la IDR se incrementó en comparación al nivel de ingesta adecuada (IA) establecida en 1997, los niveles óptimos de las ingestas recomendadas y de 25-hidroxivitamina D del suero que minimizan el hiperparatiroidismo y maximizan la salud ósea en la población general permanecen controversiales (40). La IDR para la vitamina D se muestra en la Tabla 1 por etapa de la vida y género.
| Etapa de la Vida | Edad | Machos | Hembras | ||
|---|---|---|---|---|---|
| μg/día | UI/día | μg/día | UI/día | ||
| Infantes (IA) | 0-6 meses |
10
|
400
|
10
|
400
|
| Infantes (IA) | 6-12 meses |
10
|
400
|
10
|
400
|
| Niños | 1-3 años |
15
|
600
|
15
|
600
|
| Niños | 4-8 años |
15
|
600
|
15
|
600
|
| Niños | 9-13 años |
15
|
600
|
15
|
600
|
| Adolescentes | 14-18 años |
15
|
600
|
15
|
600
|
| Adultos | 19-70 años |
15
|
600
|
15
|
600
|
| Adultos | 71 años y más |
20
|
800
|
20
|
800
|
| Embarazo | Todas las edades |
-
|
-
|
15
|
600
|
| Período de lactancia | Todas las edades |
-
|
-
|
15
|
600
|
Prevención de Enfermedad
Mortalidad
En un análisis de seguimiento de nueve años de la Tercera Encuesta Nacional de Examinación de Salud y Nutrición de los EE.UU. (NHANES III) que incluyó a 15,099 participantes (de los cuales el 77% eran caucásicos), las concentraciones séricas de 25-hidroxivitamina D — estandarizadas según la metodología desarrollada por el Programa de Estandarización de Vitamina D [en inglés, VDSP] — fueron examinados en relación con la mortalidad. El análisis sugirió un aumento en la mortalidad por todas las causas con una disminución de las concentraciones séricas de 25-hidroxivitamina D <16 ng/mL (60). En contraste, el riesgo de mortalidad por todas las causas varió poco para las concentraciones séricas basales de 25-hidroxivitamina D en el rango de 16 a 40 ng/mL (60). Se obtuvieron resultados similares en un meta-análisis de ocho estudios de cohorte prospectivos que consideraron la relación entre las concentraciones estandarizadas de 25-hidroxivitamina D y la mortalidad durante un período de seguimiento medio de 10.5 años. Se encontró que el riesgo de muerte era 19% más alto con concentraciones de 25-hidroxivitamina D entre 12 y 15,99 ng/mL y 56% más alto con concentraciones <12 ng/mL en comparación con el riesgo asociado con concentraciones entre 30 y 39,99 ng/mL (61). Un meta-análisis de 73 estudios de cohorte prospectivos, que incluyó a >800,000 participantes, encontró que el tercil más bajo versus el más alto de las concentraciones séricas de 25-hidroxivitamina D se asoció con un mayor riesgo de mortalidad por todas las causas (+35%), mortalidad por enfermedades cardiovasculares (+35%) y mortalidad por cáncer (+14%) (62). Sin embargo, un análisis de aleatorización mendeliana — que limita el sesgo debido a la confusión y la causalidad inversa (63) — de los datos de tres grandes cohortes danesas de 95,766 adultos encontró una asociación significativa genéticas de bajas concentraciones en plasma de 25-hidroxivitamina D por todas las causas y relacionada con el cáncer, pero no con la mortalidad relacionada con la enfermedad cardiovascular (64). Finalmente, dos metanálisis de ensayos aleatorios controlados han sugerido una moderada reducción en la mortalidad por todas las causas en las personas mayores suplementadas con vitamina D y calcio, pero no sólo con vitamina D (62, 65). Ensayos adicionales controlados con placebo necesitan examinar más a fondo si la suplementación con vitamina D sola o en combinación con calcio podría ayudar a prevenir la muerte prematura en individuos repletos.
Osteoporosis
Estado de vitamina D, osteoporosis y riesgo de fractura
Aunque las causas de la osteoporosis son multifactoriales, la insuficiencia de vitamina D puede ser un factor etiológico importante en los adultos mayores. La osteoporosis afecta un tercio de las mujeres de entre 60-70 años de edad y dos tercios de las mujeres de 80 años y mayores (66). Una encuesta multinacional (18 países diferentes con latitudes en un rango entre los 64 grados norte y 38 grados sur) de más de 2,600 mujeres posmenopáusicas con osteoporosis, reveló que el 31% de los sujetos tenían concentraciones de 25-hidroxivitamina D <20 ng/mL (50 nmol/L) (67). Además, un reciente estudio de caso y control que incluyó 111 pacientes con una fractura de cadera y 73 controles (edad media, 83 años) encontró que bajos niveles séricos tanto de 25-hidroxivitamina D como vitamina K1 en comparación con control se asociaban con un incremento en el riesgo de una fractura de cadera (68). Sin suficiente vitamina D proveniente de la exposición al sol o de la ingesta dietética, la absorción intestinal del calcio puede ser significativamente reducida. Esto incrementa la secreción de PTH por las glándulas paratiroideas; la elevación prolongada de PTH puede resultar en una reabsorción ósea incrementada, la cual en turno puede incrementar el riesgo de fracturas osteoporóticas (69).
Suplementos de vitamina D y densidad mineral ósea
La pérdida progresiva de la densidad mineral ósea (DMO) que conduce a la osteopenia (pre-osteoporosis) y la osteoporosis se observa comúnmente en adultos mayores, especialmente en los ancianos. Los resultados de un meta-análisis de 23 ensayos aleatorios controlados con más de 4,000 participantes (edad media, 59 años) mostraron poca evidencia de un efecto de la suplementación con vitamina D en la DMO en cualquiera de los cinco sitios esqueléticos examinados, incluida la columna lumbar, la fémur cuello, trocánter, antebrazo y cuerpo total. Se informó un aumento significativo en la DMO solo en el cuello femoral (70). Sin embargo, se sugirió que las personas en este grupo de edad tendrían una ingesta adecuada de calcio y, por lo tanto, un metabolismo óseo normal, lo que explica la falta de un efecto de la vitamina D en el fortalecimiento de la masa ósea (71). Por el contrario, en las personas mayores, la suplementación con vitamina D es esencial para corregir y mantener concentraciones adecuadas de 25-hidroxivitamina D en suero y para prevenir el hiperparatiroidismo secundario y la pérdida de DMO (72).
Suplementos de vitamina D y riesgo de fractura
Un estudio de cohorte prospectivo que siguió a más de 72,000 mujeres posmenopáusicas en los EE.UU. durante 18 años encontró que aquellas que consumieron al menos 600 UI/día de vitamina D de la dieta y los suplementos tenían un riesgo 37% menor de fractura de cadera osteoporótica que las mujeres que consumieron menos de 140 UI/día de vitamina D (73). Sin embargo, la suplementación diaria con 400 UI de vitamina D3, en combinación con 1,000 mg de calcio, no redujo significativamente el riesgo de fractura de cadera en comparación con un placebo en 36,282 mujeres posmenopáusicas del ensayo Women's Health Initiative (74), lo que sugiere que puede haber un umbral de ingesta de vitamina D que es necesario para observar reducciones en el riesgo de fractura. Los resultados de un análisis genético de los datos de este ensayo también sugirieron que los efectos beneficiosos de la suplementación con vitamina D y calcio en el riesgo de fractura podrían limitarse a las mujeres con el riesgo genético más bajo de baja DMO (75). Sin embargo, este ensayo ha sido cuestionado por razones que incluyen mala adherencia y el hecho de que a los participantes se les permitió tomar suplementos adicionales de vitamina D y calcio que podrían haber confundido los resultados. Además, el uso de la terapia de reemplazo hormonal no se consideró en el estudio del efecto de la vitamina D y el calcio en la salud esquelética en mujeres posmenopáusicas a pesar de ser un factor de confusión importante en esta población (57, 76).
Otro ensayo, el estudio de la Evaluación Aleatorizada de Calcio o Vitamina D (RECORD), reportó que la vitamina D3 suplementaria en forma oral (800 UI/día) sola, o en combinación con calcio (1,000 mg/día), no previno la ocurrencia de fracturas osteoporóticas en adultos de la tercera edad que ya habían experimentado una fractura osteoporótica de bajo impacto (77). También en este último estudio, un cierto número de limitaciones, incluyendo una pobre adherencia y/o el hecho de que la suplementación con vitamina D no elevó los niveles de 25-hidroxivitamina D del suero a un nivel que protegería contra las fracturas, podrían explicar la carencia de algún efecto (78). A pesar de la alta adherencia al tratamiento, la incidencia de fractura no vertebral fue similar en mujeres posmenopáusicas suplementadas con vitamina D3 (dosis inicial de 200,000 UI seguida de 100,000/mes) o placebo durante más de tres años en el ensayo de Evaluación de Vitamina D (ViDA) (79). Sin embargo, el Equipo de Trabajo de Servicios Preventivos de EE.UU. que realizó el meta-análisis de 11 ensayos aleatorios controlados con placebo, incluidas 52,915 personas mayores (de las cuales el 69% eran mujeres posmenopáusicas), descubrió que la suplementación con vitamina D (300-1,000 UI/día) y calcio (500-1,200 mg/día) por hasta siete años resultaron en una reducción del 12% en el riesgo de cualquier nueva fractura (80). Otro meta-análisis de 11 ensayos aleatorizados, doble ciego, controlados con placebo en el efecto de la suplementación con vitamina D en 31,022 personas (91% mujeres) de 65 años y mayores indicó que aquellos con la mayor ingesta de vitamina D (792-2,000 UI/día) tenían un riesgo 30% menor de fractura de cadera y un riesgo 14% menor de cualquier fractura no espinal (81). Finalmente, un tercer meta-análisis de ensayos que examinó el efecto de la combinación de vitamina D y calcio en la prevención de fracturas en hombres mayores y mujeres posmenopáusicas también concluyó que el riesgo de nuevas fracturas, incluidas las fracturas de cadera, era significativamente reducido en aquellos complementados en comparación con los controles (82). Curiosamente, los tres meta-análisis han encontrado que la prevención de fracturas por la suplementación de vitamina D y calcio se limita a las personas mayores institucionalizadas. De hecho, el riesgo de fractura no se redujo significativamente por la vitamina D en las personas mayores que viven en la comunidad (80-82).
Suplementos de vitamina D y equilibrio postural, fuerza muscular y riesgo de caída
Un meta-análisis de siete estudios observacionales en 840 fallers y 1,330 no fallers encontró concentraciones de 25-hidroxivitamina D en suero significativamente más bajas en fallers que en no fallers (83). Además, otro metaanálisis de cuatro cohortes de tres estudios observacionales reportó una modesta pero significativa asociación inversa entre el estatus de la vitamina C y el riesgo de caída (83). Varios ensayos aleatorios controlados han examinado el impacto de la suplementación con vitamina D en la fuerza muscular, el equilibrio postural o el riesgo de caída en sujetos mayores. Un meta-análisis de estos ensayos encontró evidencia limitada de un efecto de la suplementación con vitamina D sobre la fuerza muscular y la movilidad, basado en un solo tipo de prueba para cada resultado. Sin embargo, en un reciente estudio aleatorizado, doble ciego, controlado con placebo en 160 mujeres posmenopáusicas (edades, 50-65 años) con un estatus subóptimo de vitamina D (concentración media de 25-hidroxivitamina D sérica <20 ng/mL), suplementación con 1,000 UI/día de vitamina D3 mejoró significativamente el estatus de la vitamina D, así como la fuerza muscular de las extremidades superiores e inferiores y los parámetros de equilibrio postural (84, 85). Se encontró que los riesgos de caídas y caídas recurrentes eran de dos a tres veces mayores en mujeres en el grupo de control que en aquellos suplementados con vitamina D3 (85). Por el contrario, otro estudio controlado aleatorio de 12 meses en 200 adultos mayores (de los cuales el 58% tenía una concentración basal de 25-hidroxivitamina D sérica <20 ng/mL) no mostró beneficios con respecto a la función de la extremidad inferior o probabilidades de caer en aquellos suplementados con 2,000 UI/día (+/- 10 µg de calcidiol) en comparación con aquellos que recibieron 800 UI/día (86). El análisis post hoc recientemente publicado del ensayo ViDA no encontró diferencias entre las probabilidades de caer y el número de caídas informadas por 5,108 participantes que viven en la comunidad (edades, 50-84 años) independientemente de si fueron asignados al azar para recibir vitamina D suplementaria (100,000 UI/mes, es decir, ~3.350 UI/día) o un placebo durante una media de 3.4 años (79). a mayoría de los participantes de ViDA tenían concentraciones séricas de 25-hidroxivitamina D ≥20 ng/mL, lo que podría explicar al menos en parte la falta de un efecto de la vitamina D en las caídas (87).
En general, la evidencia actual sugiere que los suplementos de vitamina D3 de 800-1,000 UI/día pueden ser útiles para reducir las caídas y las tasas de fracturas en adultos mayores. Para que la suplementación con vitamina D sea efectiva en la preservación de la salud ósea, se debe consumir calcio dietético adecuado (1,000 a 1,200 mg/día) (véase el artículo sobre Calcio) (88).
Cáncer
Estudios ecológicos primero sugirieron una asociación entre latitudes septentrionales, la deficiencia de vitamina D, y la incidencia de cáncer (89). Desde la década de 1980 varios estudios de cohorte prospectivos han examinado la asociación de la ingesta o estatus de la vitamina D y varios tipos de cáncer. Una reciente revisión sistemática y meta-análisis de 16 estudios prospectivos, incluyendo 137,567 sujetos, reportó una reducción del 11% en la incidencia total de cáncer y una reducción del 17% en la mortalidad por cáncer con cada incremento de 20 ng/mL (50 nmol/L) en las concentraciones de 25-hidroxivitamina D circulante. Sin embargo, un análisis de subgrupos basados en el sexo de ocho estudios encontró una asociación inversa entre la vitamina D circulante y la mortalidad por cáncer en mujeres, pero no en hombres (90). Además, evidencia creciente sugiere que algunas variaciones en el gen que codifica para el receptor de la vitamina D (RVD) podrían influir en el estatus individual de la vitamina D y posteriormente modificar la susceptibilidad a los cánceres de sitio específicos (91) e influir en la supervivencia al cáncer (92). Finalmente, se ha encontrado que muchos tumores malignos expresan el RVD, incluyendo de seno, pulmón, piel (melanoma), colon y hueso (93), sugiriendo que podrían ser susceptibles a los efectos de la vitamina D. Numerosos estudios experimentales han demostrado que las formas biológicamente activas de la vitamina D, como la 1α,25-dihidroxivitamina D y sus análogas, tras la unión al RVD, pueden controlar el destino de la célula al inhibir la proliferación y/o induciendo la diferenciación celular o muerte (apoptosis) de un cierto número de células de tipo cancerosas (94).
Cáncer colorrectal
La distribución geográfica de la mortalidad del cáncer de colon se asemeja a la distribución geográfica histórica del raquitismo (95), aportando evidencia circunstancial de que la exposición reducida a luz solar y un estado nutricional de la vitamina D disminuido podrían estar relacionados con un riesgo aumentado de cáncer de colon. La evidencia de los estudios observacionales ha apoyado en gran medida esta hipótesis. Un meta-análisis reciente de cuatro estudios de cohorte prospectivos, cuatro estudios transversales y siete estudios de caso y control encontró una relación inversa entre la vitamina D circulante y la incidencia de adenoma colorrectal — un tumor benigno que puede transformarse en maligno (96). El análisis identificó una reducción del riesgo del 32% entre los cuantiles superior versus inferior de las concentraciones séricas de 25-hidroxivitamina D (96). Además, existe una fuerte evidencia de los meta-análisis de estudios de cohorte prospectivos para sugerir que mayores ingestas de vitamina D y concentraciones séricas de 25-hidroxivitamina D están asociadas con reducciones en el riesgo de cáncer colorrectal (97-99). El meta-análisis más reciente de cuatro cohortes prospectivas, 17 estudios de caso y control anidados y tres estudios de caso y control encontró un riesgo 38% menor de cáncer colorrectal con cuantiles altos versus bajos de concentraciones circulantes de 25-hidroxivitamina D (100). Un análisis de dosis-respuesta estimó que las concentraciones séricas de 25-hidroxivitamina D de ~20 a 30 ng/mL (en comparación con ≤12 ng mL) se asociaron con un riesgo 17% menor de cáncer colorrectal, y el riesgo fue aún menor (-35%) con una concentración sérica de 55 ng/mL (100). Un análisis anterior de dosis-respuesta basado en cinco estudios de caso y control anidados había estimado que las concentraciones séricas de 25-hidroxivitamina D ≥33 ng/mL (en comparación con ≤12 ng/mL) se asociaron con un riesgo 50% menor de cáncer colorrectal (101).
Sin embargo, en un ensayo aleatorizado, doble ciego, controlado con placebo, de siete años en 36,282 mujeres posmenopáusicas que participaron en el estudio Women's Health Initiative, una combinación de vitamina D3 suplementaria (400 UI/día) y calcio (1,000 mg/día) no disminuyó la incidencia de cáncer colorrectal (102). Otro ensayo aleatorio controlado de suplementos de vitamina D3 (1,000 UI/día), con o sin suplementos de calcio (1,200 mg/día), no encontró reducción en el riesgo de recurrencia de adenoma colorrectal durante un período de tres a cinco años, en comparación con el placebo, después de la extracción inicial de adenoma en los participantes (103). No está claro si estas dosis diarias de vitamina D son demasiado bajas para detectar algún efecto sobre la incidencia de cáncer (101, 104). Se necesitan ensayos clínicos aleatorios adicionales para evaluar si la suplementación con vitamina D podría ayudar a prevenir el cáncer colorrectal. Además, no está claro si las variaciones genéticas (polimorfismos) en la secuencia de genes implicados en el metabolismo y la función de la vitamina D pueden influir en la relación entre el estatus de la vitamina D y el riesgo de adenoma colorrectal o cáncer colorrectal (105-107).
Finalmente, la creciente evidencia sugiere que un estado adecuado de vitamina D puede estar relacionado con una mejor supervivencia de los pacientes con cáncer colorrectal. Un meta-análisis de cinco estudios prospectivos encontró un riesgo 35% menor de mortalidad específica por cáncer colorrectal en pacientes con cáncer con concentraciones séricas de 25-hidroxivitamina D más altas. Un análisis de dosis-respuesta estimó que cada aumento de 8 ng/mL en la concentración de 25-hidroxivitamina D se asoció con una disminución del 10% en la mortalidad por cáncer colorrectal (108).
Cáncer de seno
Aunque la evidencia ecológica sugiere que la mortalidad por cáncer de seno aumenta con el aumento de las latitudes y la disminución de la exposición a la luz solar (109), los datos de observación más recientes proporcionan poco apoyo para una asociación entre el estado nutricional de la vitamina D y el riesgo de cáncer de seno. Un estudio prospectivo temprano en mujeres que participaron en la primera Encuesta Nacional de Examinación de Salud y Nutrición de los EE.UU. (NHANES I) encontró que las mujeres caucásicas con una exposición al sol y una ingesta de vitamina D adecuadas tuvieron un riesgo significativamente reducido de cáncer de mama 20 años después (110). Sin embargo, cuando este estudio se incluyó en un meta-análisis con nueve estudios prospectivos más recientes, no hubo diferencias significativas en el riesgo de desarrollar cáncer de seno entre los niveles más altos y más bajos de ingestas de vitamina D (111). Además, si existe una asociación entre las concentraciones circulantes de vitamina D y el riesgo de cáncer de seno no están claros. Un meta-análisis de 14 estudios observacionales (9,110 casos y 16,244 controles) informó una reducción general del riesgo del 16% cuando se comparó el cuantil más alto de las concentraciones séricas de 25-hidroxivitamina D con el más bajo. Esta asociación inversa fue estadísticamente significativa en mujeres posmenopáusicas pero no en mujeres premenopáusicas (112). Sin embargo, otro meta-análisis que incluyó un conjunto similar de 14 estudios prospectivos (dos estudios fueron diferentes) no encontró una asociación general (111). Además, un meta-análisis de estudios realizados en pacientes en la etapa temprana del cáncer de seno identificaron asociaciones entre un estado inadecuado de vitamina D y un mayor riesgo de recurrencia y muerte (113). La evidencia de los ensayos aleatorios controlados actualmente es demasiado limitada para concluir si la suplementación con vitamina D puede reducir la incidencia de cáncer de seno (revisado en 114).
No obstante, tres meta-análisis han encontrado una asociación inversa entre las concentraciones circulantes de vitamina D y la mortalidad relacionada con el cáncer de seno (111, 115, 116). En un meta-análisis de un estudio retrospectivo y cinco estudios de cohorte prospectivos, las categorías más altas versus más bajas de vitamina sérica; las concentraciones de D se asociaron con una reducción del 33% en la mortalidad; un análisis de dosis-respuesta encontró una reducción del 12% por aumento de 8 ng/mL en la vitamina D en suero (115).
Finalmente, la evidencia actual no sugiere que variaciones genéticas específicas en la codificación genética para el VDR puedan influir en el riesgo de cáncer de seno (117, 118).
Otros tipos de cáncer
Evidencia que asocie el estatus de la vitamina D con otros tipos de cáncer es actualmente limitada. Mientras que la incidencia del cáncer de próstata parece estar inversamente asociada con la disponibilidad de la luz solar, estudios prospectivos de cohorte no han encontrado generalmente relaciones significativas entre los niveles de 25-hidroxivitamina D del suero y el riesgo posterior de desarrollar cáncer de próstata (119, 120). De hecho, algunos estudios han sugerido un mayor riesgo de cáncer de próstata con concentraciones circulantes de vitamina D más altas. Por ejemplo, un estudio anidado de caso y control de hombres (622 casos y 1,451 controles) de Escandinavia encontró una relación en forma de U entre las concentraciones séricas de 25-hidroxivitamina D y el riesgo de cáncer de próstata. En ese estudio, las concentraciones séricas de 25-hidroxivitamina D de 7.6 ng/mL o inferiores, o 32 ng/mL o superiores, se asociaron con un mayor riesgo de cáncer de próstata (121). Un meta-análisis de 17 estudios de caso y control anidado, tres estudios prospectivos de cohorte, y un estudio retrospectivo de cohorte encontraron un riesgo 17% mayor de cáncer de próstata en individuos en las categorías más altas versus más bajas de concentraciones de 25-hidroxivitamina D en sangre (122). Se han destacado, en una publicación reciente, factores de confusión potenciales que podrían explicar la detección de un ligero aumento en los casos de cáncer de próstata en los hombres con altas concentraciones circulantes de vitamina D (123).
Finalmente, meta-análisis recientes de estudios observacionales encontraron una relación inversa entre el estado de la vitamina D y el riesgo de cáncer de pulmón (124, 125) y cáncer de vejiga (126, 127). Sin embargo, en los pocos y a menudo heterogéneos estudios publicados hasta la fecha, las concentraciones séricas de 25-hidroxivitamina D no se asociaron con otros tipos de cáncer, incluido el linfoma no Hodgkin (128), cáncer de ovario (129), cáncer gástrico (130), o cáncer de piel (131).
Enfermedades autoinmunes
La diabetes mellitus dependiente de insulina (diabetes mellitus tipo 1), la esclerosis múltiple (EM), la artritis reumatoide (AR), y el lupus eritematoso sistémico (LES) son ejemplos de enfermedades autoinmunes. Las enfermedades autoinmunes ocurren cuando el cuerpo organiza una respuesta inmune en contra de su propio tejido, en lugar de un patógeno externo. Las enfermedades autoinmunes ocurren cuando el cuerpo monta una respuesta inmune contra su propio tejido, en lugar de un patógeno extraño. En la diabetes mellitus tipo 1, las células β del páncreas productoras de insulina son el objetivo de una respuesta inmune inapropiada. En la EM, los objetivos son las células productoras de mielina del sistema nervioso central, y en la AR, los objetivos son las células productoras de colágeno de las articulaciones (132). El LES se caracteriza por la presencia de un amplio espectro de autoanticuerpos que provocan daños potenciales a múltiples tejidos (133). Las respuestas autoinmunes están mediadas por células inmunes llamadas células T. Se ha encontrado que la forma biológicamente activa de la vitamina D, 1α, 25-dihidroxivitamina D, modula las respuestas de las células T, de modo que las respuestas autoinmunes disminuyen. Los estudios ecológicos han encontrado que la prevalencia de enfermedades autoinmunes (particularmente para MS; 134) aumenta a medida que aumenta la latitud, lo que sugiere que una menor exposición a la radiación UVB y las asociadas disminuciones en la síntesis de vitamina D en la piel pueden desempeñar un papel en la patología de estas enfermedades. Los resultados de varios estudios de cohorte prospectivos también sugieren que un estado adecuado de vitamina D a diferentes edades (incluso in utero, en la primera infancia y durante la adolescencia) podría posiblemente disminuir el riesgo de enfermedades autoinmunes.
Diabetes mellitus tipo 1
Niveles más bajos de vitamina D circulante han sido reportados en pacientes recién diagnosticados con diabetes mellitus tipo 1 en comparación con sujetos no diabéticos del mismo sexo y edad (135, 136). Una mayor prevalencia de una insuficiencia y deficiencia de vitamina D ha sido también observada en niños pre-diabéticos que desarrollaron múltiples autoanticuerpos en los islotes (anticuerpos contra células pancreáticas que secretan insulina) en comparación a niños negativos de autoanticuerpos. Sin embargo, un estudio prospectivo que dio seguimiento al cohorte de niños pre-diabéticos encontró que sus estatus de vitamina D, definidos como insuficiente, deficiente, o suficiente, no se asoció con la tasa de progresión a diabetes tipo 1 después de 5 a 10 años de seguimiento (137). Un estudio de cohorte prospectivo más temprano de niños nacidos en Finlandia durante el año 1966 y con un seguimiento de 30 años encontró que los niños suplementados con vitamina D durante el primer año de vida tuvieron un riesgo 88% menor de desarrollar diabetes tipo 1 en comparación con aquellos que no recibieron una suplementación. Por otra parte, niños con sospecha de haber tenido raquitismo (deficiencia severa de vitamina D) durante el primer año de vida mostraron un riesgo significativamente mayor de desarrollar diabetes tipo 1 (138). Por lo tanto, la suplementación con vitamina D parece proteger contra el inicio de la diabetes tipo 1, y un estatus subóptimo de la vitamina D en la infancia puede tener efectos a largo plazo en las respuestas inmunes más tarde en la vida.
Existen también datos limitados sugiriendo que la insuficiencia de vitamina D materna durante el embarazo puede influir en el riesgo de diabetes tipo 1 en el recién nacido. En un reciente estudio de caso y control, el riesgo de la aparición de diabetes tipo 1 en la niñez era más de dos veces mayor en niños cuyas madres tuvieron niveles de 25-hidroxivitamina D del suero <21.6 ng/mL (54 nmol/L) durante el último trimestre del embarazo en comparación con los niños nacidos de mujeres con 25-hidroxivitamina D en el suero >35.6 ng/mL (89 nmol/L) (139). Otros estudios de caso y control han encontrado que la suplementación con vitamina D durante el embarazo se asoció con un riesgo menor de que sus hijos desarrollarán autoanticuerpos relacionados con la diabetes (140, 141). Sin embargo, un estudio amplio conducido en madres de niños en un riesgo genético incrementado de padecer diabetes no reportó asociación alguna entre la aparición de autoanticuerpos islote y/o aparición de diabetes en sus hijos en el primer año de vida y la ingesta de vitamina D materna durante el embarazo (142). Otro estudio de caso y control falló en observar una relación entre la 25-hidroxivitamina D del suero durante el embarazo temprano y el diagnóstico de diabetes tipo 1 en la descendencia (143). Estudios prospectivos amplios son necesarios para establecer si el estatus de la vitamina D materna durante el embarazo puede influir en el riesgo de diabetes tipo 1 en la descendencia.
Finalmente, la relación de los polimorfismos en genes relacionados con el metabolismo de la vitamina D y la diabetes tipo 1 está actualmente bajo investigación. Se ha propuesto que polimorfismos específicos en los genes, como el CYP27B1 (que codifica para la 25-hidroxivitamina D3-1α-hidroxilasa) y el RVD, pueden ser funcionalmente relevantes para la acción de la vitamina D y podrían de esta manera afectar la susceptibilidad a la enfermedad. En un estudio conducido en 8,517 niños y adolescentes con diabetes tipo 1 y 7,320 sujetos de control, polimorfismos en los genes que involucran la síntesis del colesterol y la hidroxilación de la vitamina D fueron ligados a los niveles de vitamina D circulantes y al estatus diabético (26).
Esclerosis múltiple
Niveles bajos de exposición al sol y una deficiencia de vitamina D parecen estar asociados con el desarrollo de la esclerosis múltiple (EM). Un estatus de la vitamina D pobre podría comprometer la función de células inmunes específicas críticas en la regulación de varias respuestas inmunes y ayudar a desencadenar autoinmunidad en la EM (144). Los determinantes genéticos del estatus bajo de vitamina D se han relacionado recientemente con una mayor susceptibilidad a la EM de inicio en adultos en un análisis aleatorizado mendeliano de datos del Consorcio de Genética de Esclerosis Múltiple (145). Esto se hizo eco de los resultados de varios estudios observacionales que sugirieron una asociación entre la suficiencia de vitamina D y disminución del riesgo de EM. Un estudio retrospectivo de los niveles de radiación UV ambiental y los casos de EM realizados en Australia revelaron que la incidencia de EM en la descendencia estaba inversamente relacionada con la exposición materna a los rayos UV durante el embarazo temprano (146). La exposición al sol fue también usada como un marcador sustituto para la exposición de la vitamina D en un reciente estudio de caso y control que incluyó 1,660 pacientes con EM y 3,050 controles. Los autores encontraron que las actividades al aire libre poco frecuentes y el uso de bloqueador solar durante la infancia temprana y la adolescencia se asociaron con un significante incremento en el riesgo de desarrollar EM más tarde en la vida (147). En un estudio de corte transversal, la exposición al sol y la ingesta de aceite de hígado de bacalao (rico en vitamina D) durante la infancia fueron ligados a un comienzo tardío de los síntomas entre veteranos con EM recidivante (148). Adicionalmente, un estudio de caso y control en el personal militar de los EE.UU. incluyendo 257 casos de EM diagnosticada, encontró que los sujetos caucásicos en el quintil más alto de la 25-hidroxivitamina D del suero (>39.6 ng/mL) tuvieron un riesgo 62% menor de desarrollar EM en comparación al quintil más bajo (<25.3 ng/mL) (149). Además, en dos cohortes amplias de más de 187,000 mujeres estadounidenses con un seguimiento de por lo menos 10 años, el uso de un suplemento de vitamina D (≥400 UI/día) se asoció con una reducción del 41% en el riesgo de desarrollar EM (150). Otro estudio prospectivo no controlado monitoreó la incidencia de recaída en relación con el estatus de la vitamina D en 156 pacientes con EM recurrente-remitente antes y después de recibir vitamina D suplementaria (100,000 UI/mes; 6-42 meses, mediana de 31 meses), en adición al tratamiento inmunomodulador de primera línea (151). Cada aumento de 4 ng/mL en la concentración sérica de 25-hidroxivitamina D se asoció con una disminución del 14,9% en la incidencia de recaída (151). En un estudio multicéntrico realizado en pacientes recién diagnosticados con un síndrome clínicamente aislado (SCA) y tratado con interferón (IFN)-β, el estatus de la vitamina D fue predictivo de la actividad y progresión de la EM. Las concentraciones séricas más altas de 25-hidroxivitamina D (≥20 ng/mL o ≥50 nmol/L) en el primer año después del diagnóstico de SCA predijeron un tiempo más largo para el diagnóstico de EM, menor número de nuevas lesiones, y menores cambios en la lesión y el volumen cerebral durante los siguientes cuatro años de seguimiento (152). Sin embargo, un estudio retrospectivo sugirió que el estatus de la vitamina D en pacientes con EM recurrente-remitente no tenía valor predictivo con respecto al tiempo de conversión a EM progresiva secundaria, que se caracteriza por un empeoramiento de discapacidad (153).
Los ensayos clínicos no han podido demostrar ningún beneficio de la suplementación con vitamina D, sola o en combinación con el tratamiento con IFN-β, con respecto a las tasas de recaída y los síntomas relacionados con la discapacidad en pacientes con EM (154, 155). En otros ensayos, la vitamina D3 suplementaria también falló en demostrar actividades inmunomoduladores (156-159). En un reciente ensayo aleatorizado, controlado con placebo en 53 pacientes tratados con IFN-β con EM recurrente-remitente, la suplementación con vitamina D3 (7,000 UI/día durante cuatro semanas, seguido de 14,000 UI/día hasta la semana 48) mostró poco efecto sobre la proporción de algunos linfocitos T y B reguladores durante el período de estudio de 48 semanas. La vitamina D3 solo pareció ayudar a mantener la proporción de células T CD4+ antiinflamatorias — que disminuyeron en los pacientes que recibieron placebo — pero no pudieron mejorar su reactividad cuando se estimularon con 1,25-dihidroxivitamina D in vitro (157). En otro ensayo, se encontró que la suplementación con vitamina D3 (10,400 UI/día durante tres meses) a pacientes con EM recurrente-remitente reduce la proporción de células T CD4+ productoras de IL-17 proinflamatorias, que se cree que juegan un papel central en el desarrollo de EM (160).
Artritis reumatoide
La deficiencia de vitamina D puede también estar involucrada en la etiología y/o progresión de la artritis reumatoide (AR), aunque la evidencia proviene primeramente de estudios en animales. La ausencia de receptores de la vitamina D (RVD) en ratones genéticamente modificados ha sido ligada a niveles más altos de inflamación y a un incremento en la susceptibilidad a la autoinmunidad (161). Cuando los ratones transgénicos que espontáneamente desarrollan artritis inflamatoria también están deficientes de RVD, estos desarrollan una forma más agresiva de artritis crónica (162). También, polimorfismos específicos en el gen del RVD han sido ligados a un incremento en la susceptibilidad a la AR en ciertas poblaciones, aunque la manera en que estas variantes genéticas incluyen la funcionalidad de la vitamina D no es completamente comprendida (163-165). Los datos actuales, sin embargo, apuntan a un papel de la vitamina D en la modulación del proceso inflamatorio que subyace a muchas enfermedades crónicas, incluyendo la AR. Varios estudios de corte transversal en individuos con niveles moderados a altos de inflamación han reportado tanto ninguna asociación o una asociación inversa entre la 25-dihidroxivitamina D circulante y los marcadores de la inflamación. No obstante, existe una carencia de ensayos de intervención para mostrar si la suplementación con vitamina D podría limitar la inflamación y reducir el riesgo de una enfermedad (incluyendo la AR) en sujetos con niveles altos de inflamación (166).
Actualmente, no está claro si la prevalencia de una deficiencia de vitamina D está ligada a la incidencia de la AR. En un estudio de cohorte amplio de casi 30,000 mujeres posmenopáusicas estadounidenses, los sujetos con las ingestas totales más altas de vitamina D (≥467.7 UI/día) tuvieron un riesgo 33% menor de desarrollar AR después de 11 años de seguimiento que aquellos con las ingestas más bajas (<221.4 UI/día) (167). A pesar de todo, más análisis recientes de dos cohortes amplias de casi 200,000 mujeres estadounidenses con un seguimiento de varias décadas no encontró asociación alguna entre las ingestas dietéticas reportadas de vitamina D (usando cuestionarios de frecuencia de alimentos) durante la adolescencia o adultez y la incidencia de AR más tarde en la vida (168, 169). Además, varios estudios que exploraron la relación entre la vitamina D circulante y la actividad patológica en los pacientes con AR han reportado resultados mixtos (revisado en 170). Sin embargo, dos meta-análisis recientes de estudios observacionales encontraron una relación inversa entre el estado de la vitamina D y la actividad de la enfermedad en pacientes con AR, evaluada mediante el Índice de la Actividad de la Enfermedad 28 (en inglés, DAS28) (171, 172). Finalmente, existe una escasez de estudios que exploren el efecto de la suplementación con vitamina D en la actividad patológica en los sujetos con artritis. Un pequeño estudio aleatorio, doble ciego, controlado con placebo en 22 pacientes con AR falló en demostrar mejoras en la actividad patológica y el nivel de inflamación en sujetos suplementados con calcio (1,500 mg/día) y altas dosis de vitamina D2 (ergocalciferol; un promedio de más de 4,500 UI/día) por un año en comparación al placebo (173). Otro ensayo controlado aleatorio de tres meses en 41 mujeres con AR temprana no encontró beneficios adicionales de la vitamina D3 suplementaria (una dosis en bolo de 300,000 UI) a la atención estándar (metotrexato y glucocorticoides) con respecto al recuento de linfocitos T colaboradores, producción de citocinas, o parámetros clínicos incluida la actividad de la enfermedad (174). La vitamina D suplementaria tampoco logró reducir la tasa de recurrencia de la enfermedad en pacientes con AR incluidos en dos pequeños ensayos aleatorios controlados (175, 176). Dado que estos estudios tienen varias limitaciones, incluidos los pequeños tamaño de la muestra, se justifica la investigación adicional.
Lupus eritematoso sistémico
Más prevalente y severo en poblaciones no caucásicas (hispanos, descendientes de africanos, y asiáticos) (177), el lupus eritematoso sistémico (LES) es una enfermedad autoinmune con manifestaciones clínicas heterogéneas. La enfermedad puede potencialmente afectar la mayoría de los tejidos y órganos, incluyendo la piel (erupciones en la piel y la fotosensibilidad), los riñones (nefritis), y las articulaciones (artritis). Existe evidencia de un papel de la vitamina D en la prevención del LES en modelos animales (178). Curiosamente, un reciente meta-análisis de 11 estudios de caso y control encontró que polimorfismos específicos del RVD estaban ligados al LES particularmente en asiáticos (179). Sin embargo, la relevancia funcional de tales variantes genéticas es desconocida (180). Los análisis de dos estudios de cohorte prospectivos amplios de casi 200,000 mujeres estadounidenses falló en mostrar una asociación entre la ingesta dietética de vitamina D (medida vía cuestionarios de frecuencia de alimentos) durante la adolescencia o adultez y la incidencia de LES más tarde en la vida (168, 169).
A pesar de todo, un estatus subóptimo de la vitamina D es comúnmente observado en sujetos con LES, y esto es parcialmente explicado por la falta de exposición al sol, la cual tiende a agravar los síntomas de la enfermedad (181, 182). Las concentraciones de 25-hidroxivitamina D del suero fueron inversamente correlacionadas con medidas de la actividad patológica en una cohorte de 378 pacientes con LES (183). La corrección de la insuficiencia de vitamina D con altos niveles de vitamina D3 (100,000 UI/semana por un mes de seguimiento por 100,000 UI/mes por seis meses) en 20 sujetos con LES fue ligada a la reducción en los signos de un desequilibrio inmunológico y en los niveles de autoanticuerpos típicamente detectados en LES, sugiriendo un valor terapéutico para la vitamina D en el tratamiento de la enfermedad (184). Otro estudio prospectivo conducido en 52 pacientes deficientes de vitamina D con lupus eritematoso cutáneo (un tipo de lupus con trastornos de la piel sólo) reportó una reducción en la severidad de la enfermedad en el grupo suplementado con vitamina D3 1,400 UI/día inicialmente, seguido por 800 UI/día) y calcio por un año en comparación a los pacientes no tratados (185). La suplementación con vitamina D3 (200 UI/día por un año) fue también capaz de reducir el nivel de citoquinas inflamatorias en un estudio aleatorio controlado con placebo conducido en 267 pacientes con LES (186). En otro ensayo aleatorizado, controlado con placebo, la suplementación con vitamina D3 (50,000 UI/semana durante seis meses) mejoró el índice de actividad de la enfermedad del LES (en inglés, SLEDAI) y los puntajes de la Medida de Actividad del Lupus del Consenso Europeo (en inglés, ECLAM), así como algunas medidas de fatiga en jóvenes adultos con LES de inicio juvenil (187). Sin embargo, en otros dos estudios recientes, la suplementación con vitamina D3 (dosis de bolo semanales/mensuales equivalentes a ~800 a 7,000 UI/día durante 6 a 24 meses) mejoró el estado de la vitamina D en pacientes con LES pero falló en mostrar algún beneficio con respecto a la actividad de la enfermedad (188, 189). Si bien la administración oral de vitamina D a pacientes con LES es bien tolerada, su eficacia sigue siendo cuestionable y merece mayor investigación en ensayos clínicos.
Resumen
Por lo tanto, la evidencia de estudios epidemiológicos en humanos sugiere que, si bien aún no se puede concluir que la suplementación con vitamina D es beneficiosa en la prevención o el tratamiento de enfermedades autoinmunes, es razonable suponer que corregir la insuficiencia de vitamina D y mantener niveles suficientes podría ayudar a disminuir el riesgo de enfermedad (190).
Enfermedad cardiovascular
Hipertensión (presión sanguínea alta)
La hipertensión es un factor de riesgo bien conocido para las enfermedades cardiovasculares (ECV) (191). Los resultados de estudios clínicos y basados en la observación sugieren un papel de la vitamina D en la disminución de la presión sanguínea, el cual podría ser parcialmente explicado por el hecho de que la 1,25-dihidroxivitamina D inhibe la síntesis de renina (véase Función). Así, la deficiencia de vitamina D y la posterior regulación positiva del sistema renina-angiotensina pueden contribuir a la presión sanguínea alta y el riesgo de ECV. Se ha sugerido que los niveles elevados de la PTH pueden incrementar el riesgo de hipertensión y ECV (6). A pesar de todo, en un reciente estudio de cohorte prospectivo de 3,002 individuos (con 59 años de edad al inicio del estudio), la incidencia de hipertensión, la cual afectó al 41% de los participantes durante el período de seguimiento de nueve años, no fue mayor en aquellos con niveles de 25-hidroxivitamina D del suero menores a 20 ng/mL y fue asociada sólo marginalmente con niveles elevados de PTH (192). No obstante, un meta-análisis de siete estudios prospectivos, incluyendo un total de 48,633 con casi 5,000 casos de hipertensión incidente, encontró un riesgo 30% menor de hipertensión en aquellos en el tercil superior vs. aquellos en el tercil más inferior de las concentraciones séricas de 25-hidroxivitamina D. El análisis dosis-respuesta estimó que cada 10 ng/mL de incremento en el nivel de 25-hidroxivitamina D del suero se asoció con un riesgo 12% menor de hipertensión (193). Otro meta-análisis de 14 estudios de corte transversal y 4 prospectivos también reportó una relación inversa entre la 25-hidroxivitamina D y la hipertensión (194).
Disfunción endotelial
La disfunción del endotelio vascular, la cual contribuye a un riesgo incrementado de enfermedad cardiovascular (ECV), es común en pacientes con una enfermedad renal crónica (ERC) (195). En pacientes con ERC, la función endotelial anormal está asociada con valores bajos de la dilatación mediada por flujo (DMF) de la arteria braquial, un marcador sustituto de la salud vascular. En un estudio reciente conducido en sujetos con una leve a moderada ERC, los niveles de 25-hidroxivitamina D del suero fueron positivamente asociados con valores de la DMF, sugiriendo un enlace entre el estatus de la vitamina D sub-óptimo y la disfunción endotelial (196). En un estudio de intervención preliminar, 26 pacientes con una ERC moderada y una insuficiencia/deficiencia de vitamina D fueron suplementados dos veces con 300,000 UI de vitamina D3 (en las semanas 1 y 8) y seguidos por un total de 16 semanas. La suplementación con vitamina D casi duplicó los niveles de 25-hidroxivitamina D del suero y disminuyó los niveles de PTH en un 68.5%; el estatus mejorado de la vitamina D fue acompañado por el incremento de los valores de DMF y la reducción de los niveles de los marcadores de disfunción endotelial (197). Un meta-análisis reciente de 12 pequeños ensayos aleatorios controlados en participantes con alto riesgo de ECV encontró un aumento significativo en la DMF con la suplementación con vitamina D (dosis diarias, 2,500-5,000 UI; dosis semanal, 50,000 UI; dosis mensual, 60,000 UI; dosis única de bolo, 100,000-200,000 UI) durante ocho semanas a seis meses (198).
Eventos cardiovasculares en estudios observacionales y ensayos clínicos
Hasta la fecha, la muchos estudios epidemiológicos que investigan la relación entre la vitamina D y los resultados de las ECV han provisto resultados mixtos (revisado en 199). Estudios recientes de aleatorización mendeliana no encontraron asociación entre las concentraciones séricas de 25-hidroxivitamina D genéticamente bajas y los riesgos de enfermedad coronaria, enfermedad cardíaca isquémica o infarto al miocardio (200, 201), lo que sugiere que las asociaciones informadas en estudios observacionales pueden deberse a confusión o causalidad inversa. En un ensayo de la Evaluación Aleatorizada de Calcio o Vitamina D (RECORD) en 5,292 personas mayores (véase Osteoporosis), la suplementación con 800 UI/día de vitamina D3 (± calcio) redujo el riesgo de primera falla cardíaca, pero no tuvo ningún efecto sobre el riesgo de infarto al miocardio y accidente cerebrovascular en comparación con la suplementación con calcio solo o placebo (202). Los datos sobre el efecto de la suplementación con vitamina D sobre los eventos cardiovasculares se obtuvieron de 21 estudios aleatorios controlados (incluido el ensayo RECORD) en 13,033 participantes (≥60 años) y se combinaron en un meta-análisis (202). No se encontró ningún efecto de la vitamina D (incluidos los análogos de la vitamina D) para eventos cardiovasculares mayores, como fallo cardíaco, infarto al miocardio y accidente cerebrovascular durante los períodos de seguimiento de 1 a 6,2 años (202). Sin embargo, se recomienda precaución al interpretar estos resultados, ya que los ensayos se diseñaron inicialmente para evaluar el efecto de la vitamina D en la salud ósea, y los resultados cardiovasculares no fueron criterios de valoración primarios. Varios ensayos controlados aleatorios que exploran el efecto de la suplementación con vitamina D sobre el riesgo de ECV están actualmente en curso (203), incluyendo dos grandes ensayos, el Ensayo de la Vitamina D y Omega-3 Trial (VITAL) en los EE.UU. (204) y el ensayo D-Health en Australia (205). Recientemente se publicaron los resultados de un ensayo aleatorio controlado, el ensayo de Evaluación de Vitamina D (ViDA) en Nueva Zelanda. El número total de eventos de ECV y el tiempo hasta el primer evento de ECV durante el seguimiento no fue diferente entre los que fueron suplementados con vitamina D3 (dosis inicial de 200,000 UI durante el primer mes seguido de dosis mensuales de 100,000 UI) y aquellos que recibieron un placebo por un mediana 3,3 años (206).
Diabetes mellitus tipo 2
Las personas con un síndrome metabólico están en un riesgo incrementado de contraer diabetes mellitus tipo 2 (diabetes mellitus no dependiente de insulina) y enfermedad cardiovascular (ECV). Un síndrome metabólico se refiere a varios desórdenes metabólicos, incluyendo dislipidemia, hipertensión, resistencia a la insulina y obesidad. Un reciente estudio encontró que la prevalencia de diabetes tipo 2 fue asociada con niveles subóptimos de 25-hidroxivitamina D del suero (<30 ng/mL) en 1,801 pacientes con un síndrome metabólico. Durante un período de seguimiento de ocho años, se reportaron riesgos más bajos de mortalidad por todas las causas (riesgo 72% menor) y de mortalidad por ECV específica (riesgo 64% menor) en individuos con concentraciones séricas de 25-hidroxivitamina D mayores a 30 ng/mL (75 nmol/L) cuando fueron comparados con aquellos con concentraciones por debajo de los 10 ng/mL (25 nmol/L) (207).
En personas saludables, la suficiencia de vitamina D es positivamente correlacionada con una sensibilidad a la insulina y una función de las células β pancreáticas adecuada. De manera contraria, la deficiencia de vitamina D podría afectar la homeostasis de la glucosa y causar una intolerancia a la glucosa y una resistencia a la insulina (208). En un estudio de corte transversal conducido en 12,719 adultos, de los cuales 4,057 tuvieron prediabetes (es decir un riesgo incrementado de desarrollar diabetes tipo 2), la prevalencia de la prediabetes se asoció con concentraciones inferiores de 25-hidroxivitamina D del suero (≤32.4 ng/mL). Los sujetos con las concentraciones más bajas de 25-hidroxivitamina D del suero (≤17.7 ng/mL) fueron más propensos a ser actuales fumadores, obesos, y tener hipertensión (209). La insuficiencia de vitamina D en individuos en alto riesgo puede acelerar la progresión a una diabetes evidente. En un estudio prospectivo de 2,387 hombres y mujeres de mediana edad con un seguimiento de 8 a 10 años, el riesgo de la progresión a diabetes tipo 2 a partir de la prediabetes fue 62% más bajo en mujeres y 60% más bajo en hombres en el cuartil más alto en comparación al más bajo de la vitamina D circulante (>28.4 ng/mL vs. <18.5 ng/mL). Un análisis dosis-respuesta midió una reducción promedio del 23% en el riesgo de la progresión a diabetes tipo 2 por cada incremento de 4 ng/mL (10 nmol/L) en la concentración sérica de 25-hidroxivitamina D (210). Una revisión reciente y un meta-análisis de 18 estudios de cohorte prospectivos, que incluyeron a más de 210,000 participantes seguidos durante un período medio de 10 años, encontraron que las personas en el tercio superior de los niveles de vitamina D (reportados como vitamina D circulante o ingestas dietéticas) tenían menos riesgos de desarrollar diabetes tipo 2 (riesgo 19% menor) y síndrome metabólico (riesgo 14% menor) en comparación con los del tercio inferior (211). En otro meta-análisis de nueve estudios prospectivos, que incluyó a 28,258 personas mayores (edad media, 67.7 años), se encontró que las concentraciones de vitamina D circulantes más bajas versus más altas al inicio del estudio se asociaron con un riesgo 17% mayor de desarrollar diabetes tipo 2 durante una mediana período de seguimiento de 7.3 años (212). Actualmente, la evidencia limitada sugiere que la suplementación con vitamina D puede mejorar la sensibilidad a la insulina en individuos con intolerancia a la glucosa o que manifiestan diabetes tipo 2 (213-216). Existe la necesidad de ensayos clínicos bien diseñados para examinar si mantener niveles adecuados de vitamina D puede prevenir resultados metabólicos adversos en individuos sanos y en riesgo.
Enfermedades neurodegenerativas
El deterioro cognitivo y la enfermedad de Alzheimer
La enfermedad de Alzheimer (EA) es la forma más común de demencia, caracterizada por la presencia de placas β-amiloides extra-neuronales y agregados intra-neuronales de proteínas Tau (conocidos como ovillos neurofibrilares) en el cerebro. Modelos mecanicistas actualmente estudiados en la investigación en animales sugieren que la deficiencia de vitamina D o desórdenes del metabolismo de la vitamina D y/o la interrupción de la vía vitamina D-RVD en las regiones cerebrales de la corteza y el hipocampo pueden estar involucrados en la degeneración de las neuronas y la pérdida de las funciones cognitivas (217). La evidencia experimental que apoya un papel de la vitamina D en la regulación de los canales del calcio, la neuroprotección, y la inmunomodulación en el sistema nervioso central también implica que el estatus bajo de la vitamina D puede preceder o contribuir a la disfunción cognitiva con la edad (218).
Varios estudios observacionales han examinado el deterioro cognitivo y la enfermedad cerebral degenerativa en los ancianos en relación con la ingesta dietética de vitamina D y la concentración sérica de 25-hidroxivitamina D. En un gran estudio de cohorte francés sobre osteoporosis y fracturas de cadera en mujeres posmenopáusicas, las deficiencias en el rendimiento cognitivo global, evaluadas con el Cuestionario Corto Portátil del Estado Mental de Pfeiffer (en inglés, SPMSQ), se asociaron con una menor ingesta de vitamina D dietética (<1,400 UI/semana vs. ≥1,400 UI/semana) en 5,596 mujeres de edad avanzada (edad media, 80.5 años) (219). Un estudio con un seguimiento de siete años de un subgrupo de 498 mujeres indicó que el riesgo de padecer la enfermedad de Alzheimer (pero no otros tipos de demencia) fue 77% menor en aquellas en el quintil más alto vs. aquellas en el quintil más bajo de las ingestas de vitamina D basales (220). Algunos, pero no todos, los estudios observacionales han encontrado una asociación entre las bajas concentraciones séricas de 25-hidroxivitamina D y el deterioro cognitivo leve en adultos mayores (219, 221, 222). El análisis de corte transversal y longitudinal de dos estudios prospectivos, que incluyó 1,604 hombres (223) y 6,257 mujeres (224) de edades a partir de los 65 años, informó una probabilidad 60% mayor de deterioro cognitivo al inicio del estudio y un riesgo 58% mayor de deterioro cognitivo durante un período de seguimiento de cuatro años en mujeres, pero no en hombres, con deficiencia de vitamina D (25-hidroxivitamina D circulante <10 ng/mL vs. ≥30 ng/mL). En el estudio de caso y control anidado, multiétnico, Singapore Kidney Eye Study, que incluyó a 2,273 individuos (edad media, 70.4 años), las concentraciones séricas de 25-hidroxivitamina D se correlacionaron inversamente con los déficits cognitivos que afectan la memoria episódica retrógrada, la memoria semántica y la orientación en el tiempo, según lo evaluado por el Examen Mental Abreviado (en inglés, AMT) (225).
Sin embargo, las revisiones sistemáticas y los meta-análisis de los estudios observacionales han arrojado resultados mixtos sobre la asociación del estado de la vitamina D con el rendimiento cognitivo y la EA (226-230). Además, el análisis reciente de datos de 1,182 hombres seguidos durante 18 años en el Estudio Longitudinal Uppsala de Hombres Adultos (en inglés, ULSAM) no logró encontrar asociaciones de determinantes genéticos de la síntesis de vitamina D, ingestas de vitamina D y concentraciones en el plasma de 25-hidroxivitamina D con riesgos de deficiencias cognitivas, EA, demencia vascular o demencia por todas las causas (231). Por el contrario, otro estudio de aleatorización mendeliano asoció los determinantes genéticos del estatus bajo de vitamina D a un mayor riesgo de EA en el conjunto de datos del Proyecto Internacional del Genoma del Alzheimer (17,008 casos de EA y 37,154 casos saludables) (232).
Sin embargo, la prevalencia de la insuficiencia/deficiencia de vitamina D oscila entre el 70% y 90% en los adultos mayores, y la corrección de niveles bajos de la 25-hidroxivitamina D del suero puede ayudar a mejorar los procesos cognitivos, en particular las funciones ejecutiva (233). En un pequeño estudio controlado no aleatorio en una clínica para pacientes ambulatorios, se evaluó la función cognitiva global al inicio del estudio y después de 16 meses en 20 pacientes suplementados con 800 UI/día (o 100,000 UI/mes) de vitamina D y en 24 sujetos de control. La suplementación de pacientes ambulatorios con vitamina D resultó en la corrección del estatus bajo de vitamina D (la concentración sérica promedio de 25-hidroxivitamina D fue de 16,8 ng/mL al inicio y 30 ng/mL a los 16 meses) y se asoció con una puntuación significativamente mejorada en las pruebas de cognición en comparación con el grupo no suplementado (234). En un ensayo clínico aleatorio controlado con placebo en 32 pacientes con leve a moderada EA que recibieron insulina nasal, altas dosis de la suplementación con vitamina D2 por ocho semanas (hasta 36,000 UI/día) no mejoraron significativamente el rendimiento cognitivo en comparación con dosis bajas (1,000 UI/día) (235). Más investigaciones son necesarias para investigar una relación causal entre la reposición de la vitamina D y los beneficios cognitivos potenciales a largo plazo en adultos mayores. Además, es de gran importancia evaluar si la corrección de la deficiencia de vitamina D en sujetos con deterioro cognitivo pueden mejorar el impacto de la terapia contra la demencia (236).
Enfermedad de Parkinson
La enfermedad de Parkinson (EP) ha sido asociada con una alta prevalencia de insuficiencia de vitamina D entre los pacientes, especialmente aquellos con mayores problemas de movilidad (237). Un estudio de caso y control de 296 pacientes ambulatorios con una edad media de 65 años indicó que el 23% de los sujetos con EP tenían concentraciones séricas de 25-hidroxivitamina D inferiores a 20 ng/mL en comparación con el 16% y el 10% de EA y personas sanas, respectivamente (238). En un estudio de cohorte prospectivo realizado entre 3,173 hombres y mujeres de 50-79 años y libres de EP al inicio del estudio, los individuos en el cuartil más alto de 25-hidroxivitamina D en suero (≥20 ng/mL para mujeres y ≥22.8 ng/mL para hombres) tenían un riesgo 67% menor de EP en comparación con los del cuartil más bajo (≤10 ng/mL para las mujeres y ≤11.2 ng/mL para los hombres) (239). Los meta-análisis que agrupaban datos de estudios observacionales mostraron que la insuficiencia de vitamina D se informaba con mayor probabilidad en sujetos con EP que en controles sanos (240-242).
En un estudio aleatorizado, doble ciego, controlado con placebo, 112 pacientes con EP (edad media, 72 años) en tratamiento estándar con DP fueron suplementados con 1,200 UI/día de vitamina D o un placebo durante 12 meses. La suplementación con vitamina D casi duplicó la concentración sérica de 25-hidroxivitamina D (de una media de 22.5 ng/mL a 41.7 ng/mL) en sujetos suplementados y limitó la progresión de la EP, como lo indica una mayor proporción de pacientes que no mostraron empeoramiento (según lo evaluado en la etapa de Hoehn y Yahr y la United Parkinson Disease Rating Scale parte II) en el grupo suplementado en comparación con el grupo placebo (243). Se desconoce si la insuficiencia de vitamina D tiene un papel en la patogénesis de la enfermedad, pero la reposición de vitamina D puede proveer de beneficios a la salud que van más allá de la prevención y/o el tratamiento de EP. Por ejemplo, la deficiencia de vitamina D puede contribuir al riesgo incrementado de osteoporosis y fracturas óseas en individuos con desórdenes neurológicos, incluyendo la EP y la esclerosis múltiple (244-246). Curiosamente, se encontró que la exposición al sol estaba asociada con un estatus de la vitamina D mejorada, una mayor densidad mineral ósea del segundo hueso metacarpiano, y una menor incidencia de fractura de cadera en un estudio prospectivo conducido en 324 personas de la tercera edad con EP (247).
Resultados adversos del embarazo
Una revisión sistemática y meta-análisis recientes de 31 estudios basados en la observación en el estatus de la vitamina D materno y los resultados del embarazo indicaron que la insuficiencia de vitamina D puede estar asociada con la diabetes mellitus gestacional, preeclampsia, y vaginosis bacteriana en mujeres embarazadas. La vitamina D sérica materna baja durante el embarazo también se relacionó con un mayor riesgo para los lactantes pequeños para la edad gestacional y los lactantes de bajo peso al nacer, pero no para la cesárea (248). Sin embargo, el número de ensayos de intervención actualmente es demasiado limitado para extraer conclusiones sobre si la suplementación con vitamina D durante el embarazo podría reducir la incidencia de los resultados adversos mencionados anteriormente (249).
Diabetes mellitus gestacional
La hiperglicemia anormal debido a la disfunción de células β pancreáticas caracteriza a la aparición de la diabetes mellitus gestacional (DMG) en mujeres embarazadas sin antecedentes de diabetes mellitus tipo 2. Esta condición está asociada con resultados adversos maternos serios, incluyendo preeclampsia, un riesgo alto de un parto por cesárea, y un riesgo de por vida incrementado de desarrollar un síndrome metabólico y diabetes mellitus tipo 2. La DMG puede también contribuir a un riesgo incrementado de macrosomía fetal (peso excesivo al nacer), hipoglicemia neonatal, dificultad respiratoria neonatal, y un riesgo de por vida incrementado de obesidad, intolerancia a la glucosa, diabetes mellitus tipo 2, y enfermedades cardiovasculares en los hijos (revisado en 250).
Un reciente estudio prospectivo conducido en 655 mujeres embarazadas encontró que la concentración media de 25-hidroxivitamina D del suero durante el primer trimestre del embarazo fue significativamente menor en 54 mujeres que desarrollaron una DMG incidente en comparación al resto de la cohorte (23 ng/mL vs. 25.4 ng/mL). Después de varios ajustes para los factores de confusión de estatus de la vitamina D y el riesgo de DMG (incluyendo un historial previo de diabetes tipo 2 y DMG), el estudio encontró que cada disminución de 7.5 ng/mL en la concentración de 25-hidroxivitamina D del suero durante el embarazo temprano fue asociada con un riesgo 48% mayor de desarrollar DMG (251). Las bajas concentraciones séricas de 25-hidroxivitamina D (<29,4 ng/mL) durante el segundo trimestre del embarazo también se asociaron con la incidencia de DMG en un estudio anidado de caso y control de 118 mujeres con DMG y 219 sujetos de control pareados (252). Cinco meta-análisis (248, 253-256), incluyendo estudios observacionales de calidad moderada a alta, también informaron que las concentraciones de vitamina D en suero materno durante el embarazo estaban inversamente relacionadas con el riesgo de desarrollar DMG a pesar de la evidencia de sesgo entre los estudios, como el uso de diferentes métodos para la medición de 25-hidroxivitamina D en suero, mediciones realizadas en diferentes trimestres y diferentes criterios para evaluar la DMG (revisado en 257).
Además, evidencia para el papel de la vitamina D en la regulación de la glucosa durante el embarazo fue recientemente reportada en un ensayo aleatorio, doble ciego, controlado con placebo en 54 mujeres embarazadas diagnosticadas con DMG. La suplementación con 50,000 UI de vitamina D3 dos veces durante un período de seis semanas (en e l día 1 y el día 21) resultó en una concentración significativamente menor de glucosa en plasma en ayunas y de insulina en suero, resistencia a la insulina reducida, y sensibilidad a la insulina mejorada en comparación con el placebo (258). Esto sugiere que la deficiencia de vitamina D puede afectar negativamente la tolerancia a la glucosa durante el embarazo y contribuir a la aparición de DMG. Sin embargo, no se han evaluado los beneficios potenciales de los suplementos de vitamina D en la prevención de la intolerancia a la glucosa y la DMG durante el embarazo. Un ensayo aleatorio controlado multicéntrico (DALI) está en curso en Europa para evaluar los efectos de la vitamina D y las intervenciones en el estilo de vida (alimentación saludable y actividad física) sobre el estado metabólico de las mujeres embarazadas con riesgo de DMG (criterios de inclusión: IMC anterior al embarazo ≥ 29 kg/m2) (259). Hallazgos preliminares sugieren que una alimentación saludable y la actividad física pueden ayudar a reducir el aumento de peso gestacional, en comparación con el estándar de atención; sin embargo, es poco probable que estos cambios en el estilo de vida reduzcan el riesgo de DMG entre las mujeres embarazadas obesas (260). Los resultados con respecto al efecto de la suplementación con vitamina D en el estudio DALI aún no se han publicado.
Resultados de salud en la descendencia
Durante el embarazo, el aumento de la absorción intestinal de calcio y la movilización de calcio desde el esqueleto permite la acumulación de calcio dentro del esqueleto fetal. Sin embargo, los estudios basados en la observación que examinaron la relación entre el estado materno de vitamina D y las medidas del crecimiento óseo fetal no han proporcionado resultados consistentes (261, 262). Además, los datos recientes del Estudio de Osteoporosis con Vitamina D Materna (MAVIDOS) sugirieron que no hay diferencia en la densidad mineral ósea (DMO) corporal total de los recién nacidos de madres aleatorizadas a la suplementación diaria con vitamina D3 (1,000 UI) o placebo a partir de <17 semanas gestación hasta el parto (263). Además, el riesgo de fractura en niños daneses de 10 a 18 años fue similar, independientemente de si sus madres estuvieron expuestas a vitamina D adicional por fortificación durante el embarazo (264). Si bien la suplementación materna con vitamina D durante el embarazo previene efectivamente el riesgo de deficiencia de vitamina D en el recién nacido (265), hay poca evidencia de que el estado neonatal de vitamina D influya en el riesgo de fractura más tarde durante la infancia (266).
Algunos estudios observacionales han aportado pruebas bastante débiles en apoyo de una relación entre la suficiencia materna de vitamina D durante el embarazo y la incidencia de afecciones respiratorias y alergias en los niños (267). Un ensayo aleatorio controlado encontró que la suplementación de 108 mujeres embarazadas en el tercer trimestre (en la semana 27 de gestación hasta el parto) con 800 UI/día o una dosis en bolo de 200,000 UI de vitamina D3 no disminuyó el riesgo de sibilancias, rinitis alérgica, diagnóstico de alergia a los alimentos, infecciones del tracto respiratorio menores, o eccema en la descendencia a los tres años de edad en comparación con placebo (N=50) (268). Un ensayo aleatorio controlado doble ciego más reciente encontró que la suplementación con vitamina D3 de 295 mujeres embarazadas danesas, desde las semanas 22 a 26 de gestación hasta el parto, con 2,800 UI/día (70 μg/día) — comparado con 400 UI/día (10 μg/día) de vitamina D3 (es decir, la recomendación actual en Dinamarca) (N=286) — redujo el riesgo de episodios problemáticos de síntomas pulmonares en un 17% en la descendencia durante los primeros tres años de vida (269). Sin embargo, no se informaron diferencias con respecto al riesgo de sibilancias persistentes, asma, sensibilización alérgica, infecciones del tracto respiratorio o eccema entre los grupos de tratamiento y control (269). En un ensayo similar, aleatorizado, doble ciego y controlado- el Vitamin D Antenatal Asthma Reduction Trial — realizado en 777 mujeres embarazadas de EE.UU. con antecedentes de asma, rinitis alérgica o eccema (o cuya pareja tenía ese historial), suplementación con 2,400 UI/día (60 μg/día) o 400 UI/día (10 μg/día) no dieron lugar a diferencias en el riesgo de desarrollar asma o sibilancias recurrentes en sus hijos a la edad de tres años (270). A pesar de la falta de importancia informada en estudios individuales, el análisis agrupado de los tres ensayos encontró una reducción del 19% en el riesgo de sibilancias recurrentes en niños cuyas madres recibieron suplementos de vitamina D en dosis altas versus bajas durante el embarazo (271). En una cohorte de 378 parejas de madres e hijos, las altas concentraciones séricas de 25-hidroxivitamina D medidas en la semana 34 del embarazo se asociaron con un aumento de la alergia alimentaria del niño durante los primeros dos años de vida, lo que garantiza una evaluación cuidadosa de la seguridad de suplementos de vitamina D durante el embarazo (272).
Dado que la insuficiencia de vitamina D se ha relacionado con la autoinmunidad (ver Enfermedades autoinmunes), también se ha propuesto que el mal estatus de la vitamina D materna durante el embarazo puede contribuir a un mayor riesgo de diabetes autoinmune (diabetes mellitus tipo 1 dependiente de insulina) en la descendencia. Sin embargo, los resultados de un estudio de 3,723 niños con alto riesgo genético de diabetes tipo 1 y seguidos durante un período medio de 4.3 años encontró que la ingesta materna de vitamina D (de alimentos y/o suplementos) durante el tercer trimestre del embarazo (evaluada a través de cuestionarios de frecuencia de alimentos) no se asoció con autoinmunidad avanzada de células β o diabetes clínica (142). En un estudio anidado de caso y control, no hubo diferencia en la concentración sérica media de 25-hidroxivitamina D durante el primer trimestre del embarazo entre 343 madres de niños con diabetes tipo 1 y 343 madres control (143). Un estudio de seguimiento sugirió que los polimorfismos específicos del VDR materno, en lugar del estatus de la vitamina D, pueden estar relacionados con una mayor susceptibilidad a desarrollar diabetes tipo 1 en niños (273). Otro estudio anidado de caso y control (119 madres de niños con diabetes tipo 1 y 129 madres control) encontró una asociación inversa entre la concentración materna de la proteína de unión a vitamina D — pero no la concentración de 25-hidroxivitamina D — durante el tercer trimestre del embarazo y el riesgo de diabetes tipo 1 en niños (274). En la actualidad, no existe una causalidad establecida entre el estatus materno de vitamina D durante el embarazo y el riesgo de enfermedad autoinmune en la descendencia.
Infecciones respiratorias agudas
Más de 200 virus son responsables de causar infecciones familiares del tracto respiratorio superior (TRS), conocidas como el resfriado común, resultando en síntomas de congestión y secreción nasal, tos, dolor de garganta, y estornudos (275). El análisis de datos de corte transversal de 18,883 participantes (de 12 años de edad y mayores) de la Tercera Encuesta Nacional de Examinación de Salud y Nutrición de los EE.UU. (NHANES III) reportó una relación inversa entre las concentraciones séricas de 25-hidroxivitamina D o y una reciente (auto-reportada) infección del TRS (ITRS). En comparación a los niveles de vitamina D circulantes iguales a o por encima de los 30 ng/mL, el riesgo de una ITRS fue 24% mayor en los individuos con concentraciones de entre 10 a 29 ng/mL y 36% mayor en aquellos con niveles por debajo de los 10 ng/mL (276). Un análisis de subgrupo indicó que concentraciones séricas bajas de 25-hidroxivitamina D en sujetos con asma y una enfermedad pulmonar obstructiva crónica (EPOC) fueron ligados a una mayor susceptibilidad a una ITRS al compararse con las personas sin una enfermedad pulmonar.
En un ensayo aleatorio, doble ciego, controlado con placebo conducido en 322 adultos saludables (edades ≥18 years) dosis mensuales de vitamina D3 (200,000 UI por los primeros 2 meses y 100,000 UI por los 16 meses siguientes) aumentaron significativamente la concentración sérica promedio de 25-hidroxivitamina D del suero (de 29 ng/mL a 48 ng/mL) en el grupo de intervención pero no disminuyó la ocurrencia de ITRS en comparación con placebo (277). Además, en un ensayo clínico más grande, multicéntrico, de cuatro brazos en 2,259 sujetos (de entre 45-75 años de edad) con un historial de adenoma colorrectal, la suplementación diaria de vitamina D3 de 1,000 UI no redujo el número o la duración de los episodios de ITRS durante el invierno o el resto del año, incluso entre los participantes con las concentraciones séricas más bajas de 25-hidroxivitamina D basales (278). Además, el análisis post-hoc de los datos de un ensayo aleatorio controlado con placebo en 644 individuos (60-84 años de edad) encontró que la suplementación mensual con 30,000 UI o 60,000 UI de vitamina D3 por un período máximo de un año no disminuyó significativamente la tasa de prescripciones de antibióticos para las infecciones bacterianas de las vías respiratorias. El análisis estratificado, sin embargo, encontró que las dosis de 60,000 UI/mes disminuyeron el riesgo del uso de antibióticos en un 47% en participantes de 70 años de edad y mayores (279). Además, al compararse al placebo, la suplementación con vitamina D3 (con 2,000 UI/día) en mujeres embarazadas por 3 meses hasta el nacimiento seguida por la suplementación de sus infantes (800 UI/día) a partir de su nacimiento hasta la edad de 6 meses significativamente disminuyó el número de infección respiratorias agudas después del período de intervención, en niños de 6-18 meses de edad (280). Curiosamente, a pesar de la heterogeneidad significativa entre los ensayos, el análisis agrupado de estos datos con el de 21 ensayos adicionales sugirió una reducción general del 12% en la incidencia de ITRS con vitamina D3 administrada como dosis en bolo (cada semana, mes, o cada tres meses), dosis diarias, o una combinación de bolo y dosis diarias (281). Los análisis de subgrupos revelaron una reducción del 42% en el riesgo de ITRS con la suplementación con vitamina D3 en sujetos con concentraciones séricas basales de 25-hidroxivitamina D <10 ng/mL, mientras que no hubo efecto protector de la vitamina D3 en aquellos con concentraciones ≥10 ng/mL. Además, se encontró que las grandes dosis de bolo (≥30,000 UI) no eran efectivas en comparación con las dosis diarias o semanales, de modo que, en los análisis de subgrupos que excluían las dosis de bolo, los regímenes diarios y semanales de vitamina D3 parecían proteger contra la ITRS, independientemente del estatus basal de la vitamina D. Finalmente, el efecto de la suplementación con vitamina D3 en ITRS no parecía variar con la edad, el IMC, la presencia de asma o EPOC, y el estado de vacunación contra la gripe (281).
Los resultados de un gran ensayo clínico en Nueva Zelanda, el Estudio de Evaluación de Vitamina D (ViDA), confirmaron la ineficacia de grandes dosis de bolo de vitamina D para reducir el riesgo de infecciones respiratorias agudas (282). En este ensayo doble ciego controlado con placebo en 5,110 adultos mayores (de 50-84 años al inicio del estudio), la suplementación con una dosis inicial de 200,000 UI de vitamina D3 seguida de 100,000 UI/mes de vitamina D3 durante una mediana de 3.3 años no tuvo ningún efecto sobre la incidencia de (autoinformado) infecciones respiratorias agudas (HR, 1.01; IC del 95%, 0.94-1.07). Tras la estratificación de los datos por estatus de vitamina D, se observó un resultado nulo similar (HR, 1.08; IC del 95%, 0.95-1.23) en los participantes del estudio con concentraciones de vitamina D en la sangre ≤20 ng/ml (≤50 nmol/L; 282).
El recientemente completado VITAL (Ensayo de la Vitamina D y Omega-3) puede proporcionar evidencia adicional de un efecto de la dosificación diaria (2,000 UI/día de vitamina D) sobre el riesgo de infecciones de las vías respiratorias en adultos mayores, aunque la prevención de enfermedades infecciosas es un resultado secundario en el ensayo (204, 283, 284).
En un ensayo en niños en edad preescolar, la suplementación con vitamina D con 2,000 UI/día durante al menos cuatro meses no disminuyó la incidencia (285) o la gravedad (286) de infecciones del tracto respiratorio en invierno en comparación con la suplementación con 400 UI/día durante al menos cuatro meses. La suplementación con 2,000 UI/día dio lugar a concentraciones séricas medias de 25-hidroxivitamina D significativamente más altas en comparación con la dosis más baja (48.7 ng/mL vs. 36.8 ng/mL), pero la dosis de 400 UI puede haber sido suficiente para prevenir las infecciones de tracto respiratorio en estos niños pequeños (285). En un ensayo controlado con placebo en 1,300 niños y adolescentes sanos en zonas rurales de Vietnam (concentraciones basales de 25-hidroxivitamina D de 26 ng/mL para el grupo control y de intervención), la suplementación con 14,000 UI/semana de vitamina D durante ocho meses redujo significativamente la incidencia de infecciones respiratorias virales no relacionadas con la influenza en un 24%, pero no la incidencia de la infección por influenza A o B (287).
Enfermedad por coronavirus, COVID-19
La enfermedad por coronavirus, COVID-19, es causada por una infección con el severo síndrome respiratorio agudo coronavirus-2 (SARS-CoV-2). Este virus se originó en Wuhan, China a fines de 2019 y se extendió rápidamente por todo el mundo provocando una pandemia global. Síntomas similares a los de la gripe, incluyendo tos, fiebre, fatiga y dificultad para respirar, así como varios otros síntomas diversos caracterizan a COVID-19 (consulte los sitios web de la CDC y la OMS). Los efectos de la enfermedad varían ampliamente, y los más severos resultan en neumonía, dificultad respiratoria, y muerte. Algunas personas infectadas con SARS-CoV-2, sin embargo, son asintomáticas, pero pueden transmitir el virus a otras (288). Además, las personas infectadas con SARS-CoV-2 pueden propagar la enfermedad antes de que experimenten síntomas (es decir, transmisión presintomática) (289), lo que le da importancia al público medidas de salud como lavarse las manos, usar mascarillas, distanciamiento social, y pruebas y rastreo de contactos para reducir la pandemia.
Varios estudios observacionales han examinado la correlación del estado de la vitamina D y la incidencia de COVID-19, y la mayoría — pero no todos (290-292) — han encontrado una deficiencia o insuficiencia de vitamina D asociada con un mayor riesgo de infección por SARS-CoV-2. En un estudio de cohorte retrospectivo de más de 191,000 residentes de los EE.UU. a los que se les administró una prueba de SARS-CoV-2 durante un período de tres meses en la primavera de 2020, la positividad del SARS-CoV-2 se asoció fuertemente con una concentración sérica más baja de 25-hidroxivitamina D, medida a un solo punto en los 12 meses previos a la prueba viral (293). En este estudio, cada incremento de 1 ng/mL de 25-hidroxivitamina D en suero se vinculó con un 1.6% menos de riesgo de positividad para SARS-CoV-2, siendo el riesgo más bajo a concentraciones séricas de 55 ng/mL y superiores (293). En un estudio poblacional retrospectivo entre 7,807 personas en Israel, incluidos 782 casos positivos de SARS-CoV-2, las concentraciones en el plasma de 25-hidroxivitamina D por debajo de 30 ng/mL se asociaron con un 50% más de riesgo de infección por SARS-CoV-2 en comparación con concentraciones más altas de vitamina D (294). La evaluación del estatus de vitamina D en este estudio se realizó antes de la prueba viral, pero faltan detalles sobre el período de tiempo. La relación temporal de la medida del estatus de la vitamina D y la prueba de diagnóstico de COVID también es una preocupación en un análisis de un gran conjunto de datos del Biobanco del Reino Unido, que encontró que el estatus de la vitamina D no estaba asociado con la infección por SARS-CoV-2: el estudio utilizó evaluaciones de estatus de vitamina D realizadas de 10 a 14 años antes de la prueba de diagnóstico COVID-19 (291). De acuerdo con los hallazgos de la mayoría de los estudios disponibles, un pequeño estudio de cohorte retrospectivo (295) y cinco estudios de caso y control (296-300) informaron una asociación inversa del estatus de vitamina D y la infección por SARS-CoV-2. Un meta-análisis de 2021 de 10 estudios observacionales, que incluyeron 361,934 participantes, informó una asociación entre la insuficiencia o deficiencia de vitamina D y un mayor riesgo de COVID-19 (OR, 1.43; IC del 95%: 1.00-2.05), aunque la heterogeneidad entre los estudios fue alta (301). Además, en un análisis de datos del Biobanco del Reino Unido, se descubrió que el uso regular de suplementos de vitamina D estaba asociado con un riesgo 34% menor de infección por SARS-CoV-2 en comparación con los no consumidores de suplementos de vitamina D (292).
Adicionalmente, la mayor parte de la investigación observacional disponible sugiere una asociación entre el estatus bajo de vitamina D y la gravedad de COVID-19, con estudios que encuentran que la deficiencia de vitamina D está relacionada con un mayor riesgo de gravedad de la enfermedad, medido por la necesidad de hospitalización, ingreso a la unidad de cuidados intensivos (302) etapa de la neumonía (en hombres pero no en mujeres; 303), necesidad de ventilación no invasiva (304), necesidad de ventilación mecánica invasiva (305), o una combinación de estos y otros indicadores (297). Otro estudio encontró que el estatus insuficiente de vitamina D, definido como concentraciones de 25-hidroxivitamina D en plasma por debajo de 30 ng/mL, se asoció con una mayor probabilidad de hospitalización relacionada con COVID, pero la asociación no alcanzó significación estadística (p=0,061) excepto en un sub-análisis de personas mayores de 50 años (OR, 2.71; IC 95%: 1.55-4.78; p<0,001) (294). En contraste con la mayor parte de la evidencia hasta la fecha, un estudio de caso y control encontró que la deficiencia de vitamina D no estaba relacionada con la gravedad de COVID-19 (298). Además, algunos estudios han analizado la relación del estatus de vitamina D y la mortalidad por COVID-19, y tres encontraron que la deficiencia de vitamina D se asocia con un mayor riesgo de muerte (303, 305, 306) y dos no encontraron asociación (304, 307), aunque uno de los estudios que no encontró asociación utilizó mediciones del estatus de la vitamina D más de 10 años antes de la prueba de diagnóstico COVID-19 (307).
Dado que existen varios factores de riesgo conocidos de enfermedad grave por COVID-19, incluida la edad avanzada, la obesidad y la diabetes tipo 2 o enfermedad cardiovascular preexistente (308), es importante que los estudios observacionales controlen posibles factores de confusión. Dos estudios cuasiexperimentales informaron que la suplementación en bolo con vitamina D3 (ya sea 50,000 UI por mes o 80,000-100,000 UI cada dos o tres meses) antes o durante la infección por SARS-CoV-2 se asoció con una enfermedad menos grave y una mejor supervivencia en pacientes ancianos frágiles con COVID-19 (309, 310). Actualmente se están llevando a cabo varios ensayos controlados aleatorios de la suplementación con vitamina D en la prevención y el tratamiento de COVID-19; los resultados de estos ensayos informarán sobre la causalidad de la asociación. Sin embargo, los datos actualmente disponibles indican que la mejora del estatus de la vitamina D a través de la suplementación representa un factor de riesgo modificable para COVID-19.
Tratamiento de Enfermedad
Dermatitis atópica
La dermatitis atópica o eccema es particularmente prevalente en países industrializados, afectando de entre el 10%-20% de los niños y de entre el 1%-3% de los adultos. La dermatitis atópica es un desorden inflamatorio crónico de la piel caracterizada por áreas secas y con prurito (picazón) de la piel en sujetos afectados. La inflamación cutánea local y la disfunción inmune pueden dañar la barrera epidérmica e incrementar la susceptibilidad a las infecciones cutáneas y reacciones atópicas en los individuos afectados. La enfermedad es usualmente asociada con otras enfermedades atópicas, incluyendo alergias a los alimentos, el asma, y la rinitis alérgica (311).
Aunque la etiología de la enfermedad no es completamente explicada, la deficiencia de vitamina D puede contribuir a la aparición y/o severidad de la enfermedad (312). Recientemente, utilizando conjuntos de datos a gran escala de personas caucásicas de ascendencia europea, incluido los consorcios del recurso de UK Biobank (313) y el SUNLIGHT (35), el asma de GABRIEL (314), y eccema EAGLE (315), un estudio de aleatorización mendeliano no encontró asociación entre las concentraciones séricas de 25-hidroxivitamina D genéticamente bajas y los riesgos de dermatitis atópica, asma, o altas concentraciones séricas de inmunoglobulina (Ig)-E (316).
Varios estudios aleatorios controlados han examinado si la vitamina D podría ser una herramienta adjunta eficaz en el manejo de la enfermedad, posiblemente mediante la regulación de las reacciones inflamatorias locales y la estimulación de las actividades antimicrobianas en la piel. Además, el efecto beneficioso de la fototerapia observado en casos específicos de dermatitis atópica puede estar parcialmente mediado por la acción de la vitamina D (311). En un pequeño estudio aleatorizado, doble ciego, controlado con placebo en 45 pacientes con dermatitis atópica y bajo nivel de vitamina D (70% de los sujetos tenían concentraciones séricas de 25-hidroxivitamina D <20 ng/mL), administración diaria de 1,600 UI de administración oral de vitamina D3, sola o junto con 600 UI/día de vitamina E, durante un período de 60 días redujo significativamente el alcance y la intensidad del eccema, según lo evaluado por el puntaje SCORAD (SCORing Atopic Dermatitis) (317). La vitamina D3 (1,600 UI/día durante 60 días) también mejoró el estatus de la vitamina D y redujo la gravedad de la enfermedad en 53 pacientes con dermatitis atópica en otro pequeño ensayo aleatorizado (318). Más recientemente, la vitamina D3 (1,000 UI/día durante un mes) mejoró la gravedad de la dermatitis atópica relacionada con el invierno en niños mongoles, como lo demuestran los cambios en el Eczema Area and Severity Index (EASI) y los puntajes de la Investigator’s Global Assessment (IGA) (319). Un meta-análisis de cuatro ensayos pequeños (incluidos los citados anteriormente) confirmó que la vitamina D suplementaria puede conducir a mejoras clínicas medibles en las personas afectadas (320). Se necesitan ensayos más grandes para fortalecer estos hallazgos preliminares y determinar el régimen de suplementación más apropiado y efectivo. Es de notarse que el tratamiento tópico de la psoriasis con análogos de la vitamina D ha sido aprobado por la Administración de Drogas y Alimentos de los EE.UU. (FDA) y puede ser efectivo en el manejo de otros desórdenes cutáneos (321).
Enfermedades inflamatorias intestinales
Se cree que varios factores ambientales y genéticos mal definidos contribuyen al desarrollo de la respuesta inmune inapropiada de la microbiota intestinal que causa la colitis ulcerosa (CU) y la enfermedad de Crohn (EC). Mientras que los polimorfismos específicos del RVD pueden estar ligados a un incremento en la susceptibilidad de desarrollar CU y EC (322), se encontró que las ingestas altas de vitamina D y niveles circulantes pronosticados estaban asociados con una reducción en la incidencia de CU y EC en una cohorte amplia de 72,719 mujeres (323). Un meta-análisis de seis estudios observacionales encontró una asociación inversa entre el estatus de la vitamina D y la gravedad de la EC (324). Tres estudios han investigado si la vitamina D3 podría beneficiar a los pacientes con EC, posiblemente a través de la reducción de la inflamación intestinal. En un estudio multicéntrico, doble ciego, controlado con placebo, la tasa de recaída en pacientes con EC en remisión después de un año de tratamiento fue significativamente menor en aquellos suplementados diariamente con 1,200 UI de vitamina D3 y 1,200 mg de calcio en comparación con aquellos que recibieron calcio por sí solo (13% vs. a 29%) (325). En un segundo estudio piloto, dosis diarias incrementadas de vitamina D3 partiendo de 1,000 UI hasta 5,000 UI, fueron administradas sobre un período de 24 semanas en 18 pacientes con EC a fin de lograr niveles circulantes de 25-hidroxivitamina D >40 ng/mL. Aunque la mitad de los pacientes fallaron en lograr los 40 ng/mL, la concentración media de 25-hidroxivitamina D fue elevado a 45 ng/mL (a partir de un nivel medio basal de 16 ng/mL), y el mejoramiento general del estatus de la vitamina D fue asociado con una disminución significante de la severidad de la enfermedad según la evaluación de los puntajes vía Actividad de la Enfermedad de Crohn (CDAI) (326). En un ensayo de tres meses, aleatorizado, doble ciego, controlado con placebo, en 27 pacientes con EC en remisión, la suplementación diaria con vitamina D3 (2,000 UI) mejoró el estatus de la vitamina D pero no tuvo un efecto significativo sobre la permeabilidad intestinal ('intestino permeable') o medidas de inflamación y actividad de la enfermedad (327). Sin embargo, el estudio sugirió que lograr concentraciones séricas de 25-hidroxivitamina D ≥30 ng/mL podría ayudar a disminuir la inflamación intestinal y mejorar la calidad de vida de los pacientes. Se necesitan estudios adicionales para confirmar la eficacia terapéutica de la vitamina D en las enfermedades inflamatorias intestinales.
Enfermedad cardiovascular
El análisis prospectivo de 41,504 registros médicos electrónicos del estudio Intermountain Heart Collaborative encontró que sólo un tercio de los pacientes tuvieron concentraciones séricas adecuadas de 25-hidroxivitamina D (>30 ng/mL); la insuficiencia de vitamina D (concentraciones séricas de 25-hidroxivitamina D ≤30 ng/mL) fue asociada con un incremento en la prevalencia e incidencia de muchas condiciones cardiovasculares, incluyendo la hipertensión, enfermedad coronaria cardíaca, insuficiencia cardíaca, y accidentes cerebrovasculares (328). El estatus subóptimo de la vitamina D ha sido también ligado a la rigidez arterial y a la disfunción endotelial vascular — fuertes determinantes de la hipertensión incidente y resultados cardiovasculares adversos (329).
Hipertensión
Varios estudios de intervención han evaluado el efecto de la suplementación con vitamina D en la presión sanguínea alta. Un ensayo clínico controlado temprano de 18 hombres y mujeres con hipertensión leve sin tratar; viviendo en Los Países Bajos encontró que la exposición a la radiación UVB tres veces a la semana por seis semanas durante el invierno incrementó las concentraciones séricas de 25-hidroxivitamina D en un 162%, disminuyó los niveles de PTH en un 15%, y disminuyó las medidas de la presión sanguínea diastólica y sistólica ambulatoria de 24 horas en un promedio de 6 mm Hg (330). Un reciente meta-análisis de 16 ensayos controlados aleatorios que involucraron 1,879 participantes, tanto saludables como con condiciones cardiometabólicas preexistentes (incluyendo la hipertensión), no encontró una reducción significante en las presiones sistólica y diastólica sanguíneas con la suplementación de vitamina D (800-8,571 UI/día por cinco semanas a un año). Sin embargo, un análisis de subgrupo de seis ensayos encontró una reducción significativa de 1.31 mm Hg en la presión sanguínea diastólica en individuos con condiciones preexistentes. Si bien se pueden esperar mejoras en la presión sanguínea en casos de insuficiencia/deficiencia de vitamina D, los autores notaron que el estatus subóptimo de vitamina D en los participantes no se observó exclusivamente en aquellos con condiciones cardiometabólicas (331). Por el contrario, en dos estudios de intervención recientes — el ensayo de hipertensión con vitamina D de Estiria (332) y el ensayo de la terapia con Vitamina D en individuos con alto riesgo de hipertensión [DAYLIGHT] (333) — los sujetos con (pre)hipertensión suplementada con vitamina D3 (400 a 4,000 UI/día durante dos a seis meses) no mostraron evidencia de disminución de la presión sanguínea, independientemente de sus estatus de vitamina D basales (insuficientes o adecuados, de acuerdo con los límites actuales de la OIM).
Las condiciones que disminuyen la síntesis de vitamina D en la piel, tales como tener la piel de color oscuro, vivir en latitudes templadas, y el envejecimiento, están asociados con el incremento de la prevalencia de la hipertensión (334), sugiriendo que la vitamina D puede disminuir los niveles de la presión sanguínea en grupos selectos de individuos. En el meta-análisis previamente mencionado, un ensayo de cuatro brazos, doble ciego, controlado con placebo fue conducido en 283 afroamericanos que al azar recibieron suplementos de vitamina D3 diarios de 1,000 UI, 2,000 UI, o 4,000 UI por un período de tres meses. La presión sanguínea sistólica se redujo unos 0.66 mm Hg con 1,000 UI/día, 3.4 mm Hg con 2,000 UI/día y en unos 4 mm Hg con 4,000 UI/día mientras que incrementó 1.7 mm Hg en el grupo de placebo cuando se comparó con los valores basales. Una reducción significante del 0.2 mm Hg en la presión sanguínea sistólica fue detectada por cada incremento de 1 ng/mL en la concentración de 25-hidroxivitamina D. Sin embargo, no hubo diferencia estadística en el cambio de tres meses en la presión sanguínea entre la vitamina D3 y el placebo (335). Otro estudio aleatorizado, controlado con placebo en 150 participantes de edad avanzada (edad media, 77 años) mostró que la suplementación con 100,000 UI de vitamina D3 cada tres meses durante un año no disminuyó significativamente la presión arterial en comparación con el placebo (336).
Se necesita más investigación para determinar si la suplementación con vitamina D es útil en la prevención o el manejo de la hipertensión.
Insuficiencia cardiaca congestiva
La insuficiencia cardíaca congestiva (también llamada insuficiencia cardíaca) es caracterizada por un aumento del ritmo cardíaco y la posterior hipertrofia del ventrículo izquierdo del corazón. La insuficiencia cardiaca está asociada con una fracción de eyección ventricular izquierda (FEVI) reducida, evaluada con un ecocardiograma. Los inhibidores de la enzima convertidora de angiotensina (ECA) (véase Regulación de la presión sanguínea) son actualmente usados como terapia de primera elección en los pacientes con insuficiencia cardíaca. Curiosamente, en un estudio de corte transversal reciente en pacientes saludables sometidos a una angiografía coronaria, las concentraciones séricas insuficientes de 25-hidroxivitamina D de <30 ng/mL fueron asociadas con tasas de flujo coronario más pobres (337). El estatus subóptimo de vitamina D también se ha relacionado con un peor pronóstico en pacientes con insuficiencia cardíaca (338). En los últimos años, varios estudios de intervención han examinado el efecto de la suplementación con vitamina D en personas con insuficiencia cardíaca. En un estudio aleatorio, doble ciego controlado con placebo de 12 semanas, la suplementación diaria con 1,200 UI de vitamina D3 en niños con una insuficiencia cardíaca congestiva crónica llevó a un incremento significativo del estatus de la vitamina D acompañado por una mejora del rendimiento muscular del corazón (FEVI incrementada) como también por niveles más bajos de PTH y citoquinas pro-inflamatorias (339). En otro ensayo aleatorio, doble ciego, controlado con placebo en 64 pacientes de la tercera edad con insuficiencia cardíaca, los participantes que recibieron 800 mg/día de calcio y 50,000 UI/semana de vitamina D3 no desempeñaron significativamente mejor en las tareas de rendimiento físico (usadas como proxy para evaluar la capacidad aeróbica y la fortaleza músculo esquelética) en comparación con aquellos suplementados con calcio solo (340). Un meta-análisis reciente de siete pequeños ensayos controlados aleatorizados con placebo en 573 sujetos con insuficiencia cardíaca mostró que la suplementación con vitamina D (de 1,000 UI/día a 50,000 UI/semana) durante seis semanas a nueve meses podría reducir las concentraciones séricas de PTH, tumor necrosis factor α (TNF-α), y proteína C reactiva (PCR). Sin embargo, no hubo diferencias significativas en la FEVI, la concentración de interleucina-10 (IL-10) circulante, y la concentración de renina entre los pacientes tratados con vitamina D y los que recibieron un placebo (341). Finalmente, en el ensayo EVITA (Efecto de la vitamina D sobre la mortalidad por todas las causas) en pacientes con insuficiencia cardíaca en etapa terminal y estatus inadecuado de la vitamina D (valores basales de 25-hidroxivitamina D en suero, 8.6-19.7 ng/mL), suplementación con 4,000 UI/día durante tres años no redujo el riesgo de mortalidad en comparación con el placebo (342).
Fuentes
Luz solar
La radiación solar ultravioleta-B (UVB; longitudes de onda de 290 a 315 nanómetros) estimula la producción de vitamina D3 en la epidermis de la piel (343). La exposición a la luz solar puede proveer a la mayoría de las personas de su requerimiento entero de vitamina D. Los niños y adultos jóvenes que pasan un tiempo corto en exteriores, dos o tres veces a la semana, generalmente sintetizan toda la vitamina D que necesitan para prevenir una deficiencia. Un estudio reportó que las concentraciones séricas de vitamina D luego de la exposición a una dosis eritemal mínima de luz solar estimulada (la cantidad de luz requerida para causar un leve enrojecimiento de la piel) en todo el cuerpo fue equivalente a ingerir aproximadamente de 10,000 a 25,000 UI de vitamina D (344). Las personas con un color de piel oscuro sintetizan notablemente menos vitamina D con la exposición a luz solar que aquellas con piel de color más claro (34). Adicionalmente, los adultos mayores tienen una capacidad reducida para sintetizar vitamina D a partir de la exposición a la luz solar y frecuentemente utilizan bloqueador solar o ropa protectora con el fin de prevenir el cáncer a la piel y el daño solar. La aplicación de bloqueador solar con un FPS de 10 reduce la producción de vitamina D en un 90% (30). En latitudes cercanas a los 40 grados norte y 40 grados sur (Boston está a 42 grados norte), hay radiación UVB insuficiente disponible para la síntesis de vitamina D desde noviembre hasta principios de marzo. Diez grados más al norte o al sur (Edmonton, Canadá) el "invierno de vitamina D" se extiende desde mediados de octubre a mediados de marzo. Se ha estimado que unos 15 minutos de exposición solar diaria en manos, brazos, y cara, alrededor de las 12 pm a través de todo el año en latitudes de 25 grados (Miami, FL) y durante la primavera, verano, y otoño, en latitudes de 42 grados (Boston, MA), pueden proveer a un individuo de piel clara con 1,000 UI de vitamina D (345).
Fuentes alimenticias
La vitamina D se encuentra de forma natural en solo algunos pocos alimentos como pescados grasos (macarela, salmón, sardinas), aceites de hígado de pescado, huevos de gallinas que han sido alimentadas con vitamina D, y hongos expuestos a la luz solar o radiación UVB. En los EE.UU., la leche y la fórmula infantil son fortificadas con vitamina D para que contenga 400 UI (10 μg) por cuarto. Sin embargo, otros productos lácteos, como el queso y el yogurt, no siempre son fortificados con vitamina D. Algunos cereales, panes, y jugos de frutas, pueden también ser fortificados con vitamina D. Realizar estimados precisos de la ingesta recomendada promedio de vitamina D resulta difícil debido a la alta variabilidad del contenido de vitamina D de los alimentos fortificados (346). El contenido de vitamina D de algunos productos ricos en vitamina D están listados en la Tabla 2 en ambos unidades internacionales (UI) y microgramos (μg). Para obtener más información sobre el contenido de nutrientes de alimentos específicos, revise la base de datos de composición de alimentos de la USDA. El metabolito 25-hidroxivitamina D también está presente en niveles bajos en ciertos alimentos, como carnes, productos lácteos, y huevos (347, 348).
| Alimento |
Porción
|
Vitamina D (UI) | Vitamina D (μg) |
|---|---|---|---|
|
Salmón rosado, enlatado
|
3 onzas | 465 | 11.6 |
| Macarela caballa, enlatada (deshuesada) | 3 onzas | 248 | 6.2 |
| Sardinas enlatadas en aceite | 3 onzas | 164 | 4.1 |
| Leche, baja en grasa (1%), fortificada con vitamina D |
8 onzas fluidas
|
108 | 2.7 |
| Jugo de naranja, fortificado con vitamina D | 8 onzas fluidas | 100 | 2.5 |
| Cereal, fortificado | 1 porción (usualmente 1 taza) | 40-50 | 1.0-1.3 |
| Yema de huevo | 1 grande | 37 | 0.9 |
Suplementos
La mayoría de los suplementos de vitamina D disponibles sin una prescripción contienen colecalciferol (vitamina D3). Los suplementos multivitamínicos generalmente contienen 400 UI-1,000 UI (10 μg-25 μg) de vitamina D2 o vitamina D3. Los suplementos de vitamina D de un solo ingrediente pueden aportar entre 400 a 5,000 UI de vitamina D3, pero 400 UI es la dosis más comúnmente disponible (66). Varios suplementos de calcio también pueden proporcionar vitamina D. Un meta-análisis de ensayos aleatorios controlados sugirió que las dosis en bolo de vitamina D2 (ergocalciferol) pueden no ser siempre tan efectivas como la vitamina D3 para elevar las concentraciones séricas de 25-hidroxivitamina D, pero no hay diferencia en eficacia se encontró con la suplementación diaria con vitamina D2 o vitamina D3 (349). Sin embargo, un ensayo aleatorizado, doble ciego, controlado con placebo de 25 semanas, encontró que la suplementación diaria con 1,000 UI de vitamina D3 iniciada al final del verano es más eficaz que la vitamina D2 para mantener las concentraciones de 25-hidroxivitamina D en verano durante los meses de otoño e invierno (350).
Existe un interés creciente en el uso de la forma hidroxilada de colecalciferol, 25-hidroxivitamina D3 (calcidiol; calcifediol), como suplemento. Este metabolito de la vitamina D es sintetizado por el hígado de humanos y animales a partir del colecalciferol producido en la piel o consumido en la dieta, y está presente en algunos alimentos (por ejemplo, carnes, leche, huevos) en niveles bajos (347, 348). En general, los estudios clínicos han encontrado que el calcifediol es de dos a cinco veces más potente para aumentar las concentraciones de 25-hidroxivitamina D en la sangre en comparación con la suplementación con dosis equivalentes de colecalciferol (351-359). Por lo tanto, la suplementación con calcifediol puede representar un medio para mejorar el estatus de la vitamina D de manera rápida y constante con dosis más bajas que el colecalciferol y puede beneficiar a aquellos individuos con condiciones que disminuyen la absorción intestinal del colecalciferol (359). Sin embargo, la forma de 25-hidroxivitamina D3 no está disponible actualmente como suplemento de venta libre en los Estados Unidos.
Seguridad
Toxicidad
La toxicidad por vitamina D (hipervitaminosis D) no ha sido observada como resultado de la exposición solar. La razón es que la exposición solar excesiva genera un cierto número de fotoproductos biológicamente inertes provenientes del 7-dehidrocolesterol y el colecalciferol (3). La toxicidad por vitamina D induce una concentración sérica anormalmente elevada de calcio (hipercalcemia), los que podrían resultar en pérdida de hueso, cálculos renales, y la calcificación de órganos como el corazón y riñones si no es tratada por un largo período de tiempo. Se ha observado hipercalcemia posterior a dosis diarias superiores a 50,000 UI de vitamina D (360). En general, la investigación sugiere que la toxicidad por vitamina D es muy poco probable en personas saludables con niveles de ingesta menores a 10,000 UI/día (361-363). Sin embargo la Junta de Nutrición y Alimentos del Instituto de Medicina estableció conservadoramente un nivel máximo de ingesta tolerable (NM) de 4,000 UI/día (100 μg/día) para todos los adultos (Tabla 3). Ciertas condiciones médicas pueden incrementar el riesgo de hipercalcemia en respuesta a la vitamina D, incluyendo el hiperparatiroidismo primario, la sarcoidosis, tuberculosis, y linfoma (361). Las personas con estas condiciones podrían desarrollar hipercalcemia en respuesta a cualquier aumento en la nutrición de vitamina D y deben consultar a un profesional de la salud calificado con relación a cualquier aumento en la ingesta de vitamina D.
| Grupo Etario | μg/día | UI/día |
|---|---|---|
| Infantes 0-6 meses | 25 | 1,000 |
| Infantes 6-12 meses | 37.5 | 1,500 |
| Niños 1-3 años | 62.5 | 2,500 |
| Niños 4-8 años | 75 | 3,000 |
| Niños 9-13 años | 100 | 4,000 |
| Adolescentes 14-18 años | 100 | 4,000 |
| Adultos 19 años y más | 100 | 4,000 |
Interacciones con drogas/fármacos
Los siguientes medicamentos no deben tomarse al mismo tiempo que la vitamina D porque pueden disminuir la absorción intestinal de vitamina D: colestiramina (Questran), colestipol (Colestid), orlistat (Xenical), y aceite mineral (364, 365). Los siguientes medicamentos incrementan el metabolismo de la vitamina D y podrían disminuir las concentraciones séricas de 25-hidroxivitamina D: fenitoína (Dilantin), fosfenitoína (Cerebyx), fenobarbital (Luminal), carbamazepina (Tegretol), y rifampicina (Rimactane) (6). La cimetidina, un bloqueador H2 que suprime la secreción de ácido del estómago, inhibe la hidroxilación de la vitamina D en el hígado (366). El tratamiento del reflujo ácido, la enfermedad por reflujo gastroesofágico (ERGE), o las úlceras con inhibidores de la bomba de protones (omeprazol, lansoprazol) pueden interferir con la absorción de calcio y aumentar el riesgo de fracturas, por lo que se recomienda a los pacientes que tomen suplementos de calcio y vitamina D (367). El medicamento antimicótico oral, ketoconazol, inhibe la enzima 25-hidroxivitamina D3-1α-hidroxilasa y se ha encontrado que reduce las concentraciones séricas de 1α, 25-hidroxivitamina D en hombres sanos (368). La Sociedad de Endocrinología también recomienda monitorear el estatus de la vitamina D de pacientes tratados con glucocorticoides y drogas para el tratamiento del VIH ya que estos medicamentos incrementan el catabolismo de la 25-hidroxivitamina D (40). El uso de algunos agentes citostáticos (inhibidores del crecimiento celular) puede también incrementar la degradación de la 25-hidroxivitamina D y 1α,25-hidroxivitamina D en pacientes con cáncer bajo quimioterapia (6). La inducción de hipercalcemia por niveles tóxicos de vitamina D puede precipitar la arritmia cardíaca en pacientes tratados con digoxina (Lanoxin) (366). La hipercalcemia también puede reducir la efectividad del verapamilo (Calan) y el diltiazem (Cardizem) en la fibrilación auricular (366).
Recomendación del LPI
El Instituto Linus Pauling (LPI) recomienda que adultos generalmente sanos tomen 2,000 UI (50 μg) de vitamina D suplementaria diariamente. La mayoría de los multivitamínicos contienen 400 UI (10 μg) de vitamina D, y los suplementos de vitamina D de un solo ingrediente se encuentran disponibles para la suplementación adicional. La exposición al sol, la dieta, el color de piel, y el índice de masa corporal (IMC) tienen un impacto variable y sustancial sobre los niveles corporales de vitamina D. Para ajustarse a las diferencias individuales y asegurar un estatus adecuado de vitamina D corporal, el Instituto Linus Pauling recomienda apuntar hacia una concentración sérica de 25-hidroxivitamina D de por lo menos 30 ng/mL (75 nmol/L). Estudios basados en la observación sugieren que concentraciones séricas de 25-hidroxivitamina D de entre 30 ng/mL y 60 ng/mL están asociadas con riesgos menores de resultados de la salud adversos, incluyendo cánceres y enfermedades autoinmunes.
La Academia Estadounidense de Pediatría actualmente sugiere que todos los bebés, niños, y adolescentes, reciban 400 UI de vitamina D suplementaria diariamente (19). De acuerdo con las recomendaciones de la Sociedad de Endocrinología (40), el Instituto Linus Pauling recomienda ingestas diarias de 400 a 1,000 UI (10 a 25 μg) de vitamina D en infantes y 600 a 1,000 UI (15 a 25 μg) de vitamina D en niños y adolescentes. Dado el contenido promedio de vitamina D de la leche materna, la fórmula infantil, y las dietas de niños y adolescentes, puede ser necesaria la suplementación para cumplir con estas recomendaciones.
Adultos mayores (>50 años)
La suplementación diaria con 2,000 UI (50 μg) de vitamina D es especialmente importante en adultos mayores, debido a que el envejecimiento es asociado con una capacidad reducida de sintetizar vitamina D en la piel luego de su exposición al sol.
Autores y Críticos
Originalmente escrito en Marzo de 2004 por:
Jane Higdon, Ph.D.
Instituto Linus Pauling
Universidad Estatal de Oregon
Actualizado en Julio de 2014 por:
Barbara Delage, Ph.D.
Instituto Linus Pauling
Universidad Estatal de Oregon
Actualizado en Julio de 2017 por:
Barbara Delage, Ph.D.
Instituto Linus Pauling
Universidad Estatal de Oregon
Revisado en Octubre de 2017 por:
Adrian F. Gombart
Investigador Principal, Instituto Linus Pauling
Profesor Asociado, Departamento de Bioquímica y Biofísica
Universidad Estatal de Oregon
Traducido al Español en 2019 por:
Natsumi Then Shimazaki
Instituto Linus Pauling
Universidad Estatal de Oregon
La actualización de este artículo en el 2017 fue respaldada por una subvención de Pfizer Inc.
Originalmente traducido al español en 2012 por Guillermo Sandoval y editado por Andrew Quest (Ph.D.) y Lisette Leyton (Ph.D.), todos provenientes de la Universidad de Chile. Estos esfuerzos fueron patrocinados por el projecto Anillo #ACT1111, CONICYT-Chile, programa PIA.
Última actualización 5/6/21 Derechos de autoría 2000-2026 Instituto Linus Pauling
Figure Alternative Text
Figure 1. Chemical structures of vitamin D
The figure shows the chemical structures and synthesis pathway of vitamin D. In the upper layers of the skin, ultraviolet-B light converts 7-dehydrocholesterol into previtamin D3. Previtamin D3 is then non-enzymatically converted into vitamin D3 (cholecalciferol) in the lower layers of the skin. Vitamin D3 is transported to adipose tissue for storage or to the liver for activation.
In liver cells, cytochrome P450 enzymes hydroxylate vitamin D3, forming 25-hydroxyvitamin D3 (calcidiol). In the kidneys (and to a limited extent, other tissues), CYP27B1 converts 25-hydroxyvitamin D3 to the active form: 1α,25-dihydroxyvitamin D3 (calcitriol). Plant-derived vitamin D2 (ergocalciferol) follows a similar activation pathway.
Figure 2. Conversion to the active form of vitamin D and VDR-mediated gene regulation
The figure shows the conversion of vitamin D to its active form and vitamin D receptor (VDR)-mediated gene regulation. Both 25-hydroxyvitamin D and 1,25-dihydroxyvitamin D circulate in the blood bound to vitamin D-binding protein (DBP) and enter cells via the megalin/cubulin complex.
On the left: In kidney cells, CYP27B1 hydroxylates 25-hydroxyvitamin D to form the active form of vitamin D: 1,25-dihydroxyvitamin D. This reaction is stimulated by parathyroid hormone, estradiol, and low blood phosphorus, whereas the reaction is inhibited by 1,25-dihydroxyvitamin D, FGF-23, and high blood calcium.
On the right: 1,25-Dihydroxyvitamin D enters the circulation and reaches extra-renal target tissues, where it regulates gene expression. In the nucleus, 1,25-dihydroxyvitamin D binds to the VDR, which heterodimerizes with the retinoid X receptor (RXR). The VDR-RXR complex binds to vitamin D response elements (VDRE) in the promoter regions of vitamin D target genes, recruiting RNA polymerase II to initiate transcription.
Figure 3. Regulation of calcium and phosphorus homeostasis
The figure shows mechanisms of calcium and phosphorus homeostasis. When blood calcium concentration decreases, the parathyroid glands release parathyroid hormone (PTH). PTH acts on the kidney to stimulate CYP27B1 activity, which hydroxylates 25-hydroxyvitamin D to 1,25-dihydroxyvitamin D. This active form of vitamin D (1) increases reabsorption of calcium by the kidneys and stimulates phosphorus excretion, (2) increases the intestinal absorption of both calcium and phosphorus, and (3) mobilizes calcium and phosphorus from bone when dietary calcium intake is insufficient. PTH also stimulates bone resorption, releasing calcium and phosphorus into the blood. 1α,25-dihydroxyvitamin D inhibits its own production, as well as PTH synthesis, via negative feedback loops. FGF-23, secreted by bone-forming cells (osteoblasts) in response to increased phosphorus intake, inhibits the synthesis of 1α,25-dihydroxyvitamin D and promotes urinary excretion of phosphorus.
Referencias
- Holick MF. Vitamin D: importance in the prevention of cancers, type 1 diabetes, heart disease, and osteoporosis. Am J Clin Nutr. 2004;79(3):362-371. (PubMed)
- Bikle DD. Vitamin D metabolism, mechanism of action, and clinical applications. Chem Biol. 2014;21(3):319-329. (PubMed)
- Volmer DA, Mendes LR, Stokes CS. Analysis of vitamin D metabolic markers by mass spectrometry: Current techniques, limitations of the "gold standard" method, and anticipated future directions. Mass Spectrom Rev. 2015;34(1):2-23. (PubMed)
- Holick MF. Vitamin D: A millenium perspective. J Cell Biochem. 2003;88(2):296-307. (PubMed)
- Sutton AL, MacDonald PN. Vitamin D: more than a "bone-a-fide" hormone. Mol Endocrinol. 2003;17(5):777-791. (PubMed)
- Grober U, Spitz J, Reichrath J, Kisters K, Holick MF. Vitamin D: Update 2013: From rickets prophylaxis to general preventive healthcare. Dermatoendocrinol. 2013;5(3):331-347. (PubMed)
- Lieben L, Carmeliet G. The delicate balance between vitamin D, calcium and bone homeostasis: lessons learned from intestinal- and osteocyte-specific VDR null mice. J Steroid Biochem Mol Biol. 2013;136:102-106. (PubMed)
- Fukumoto S. Phosphate metabolism and vitamin D. Bonekey Rep. 2014;3:497. (PubMed)
- Lin R, White JH. The pleiotropic actions of vitamin D. Bioessays. 2004;26(1):21-28. (PubMed)
- Edfeldt K, Liu PT, Chun R, et al. T-cell cytokines differentially control human monocyte antimicrobial responses by regulating vitamin D metabolism. Proc Natl Acad Sci U S A. 2010;107(52):22593-22598. (PubMed)
- Smolders J, Thewissen M, Damoiseaux J. Control of T cell activation by vitamin D. Nat Immunol. 2011;12(1):3; author reply 3-4. (PubMed)
- Aranow C. Vitamin D and the immune system. J Investig Med. 2011;59(6):881-886. (PubMed)
- Zeitz U, Weber K, Soegiarto DW, Wolf E, Balling R, Erben RG. Impaired insulin secretory capacity in mice lacking a functional vitamin D receptor. Faseb J. 2003;17(3):509-511. (PubMed)
- Bourlon PM, Billaudel B, Faure-Dussert A. Influence of vitamin D3 deficiency and 1,25 dihydroxyvitamin D3 on de novo insulin biosynthesis in the islets of the rat endocrine pancreas. J Endocrinol. 1999;160(1):87-95. (PubMed)
- Heer M, Egert S. Nutrients other than carbohydrates: their effects on glucose homeostasis in humans. Diabetes Metab Res Rev. 2015;31(1):14-35. (PubMed)
- Sheng H-W. Sodium, chloride, and potassium. In: Stipanuk M, ed. Biochemical and Physiological Aspects of Human Nutrition. Philadelphia: W.B. Saunders Company; 2000:686-710.
- Sigmund CD. Regulation of renin expression and blood pressure by vitamin D(3). J Clin Invest. 2002;110(2):155-156. (PubMed)
- Li YC, Kong J, Wei M, Chen ZF, Liu SQ, Cao LP. 1,25-Dihydroxyvitamin D(3) is a negative endocrine regulator of the renin-angiotensin system. J Clin Invest. 2002;110(2):229-238. (PubMed)
- Wagner CL, Greer FR, American Academy of Pediatrics Section on B, American Academy of Pediatrics Committee on N. Prevention of rickets and vitamin D deficiency in infants, children, and adolescents. Pediatrics. 2008;122(5):1142-1152. (PubMed)
- Goldacre M, Hall N, Yeates DG. Hospitalisation for children with rickets in England: a historical perspective. Lancet. 2014;383(9917):597-598. (PubMed)
- Jones AN, Hansen KE. Recognizing the musculoskeletal manifestations of vitamin D deficiency. J Musculoskelet Med. 2009;26(10):389-396. (PubMed)
- Bringhurst FR, Demay MB, Kronenberg HM. Mineral Metabolism. In: Larson PR, Kronenberg HM, Melmed S, Polonsky KS, eds. Williams Textbook of Endocrinology. 10th ed. Philadelphia: Saunders Book Company; 2003:1317-1320.
- Plotnikoff GA, Quigley JM. Prevalence of severe hypovitaminosis D in patients with persistent, nonspecific musculoskeletal pain. Mayo Clin Proc. 2003;78(12):1463-1470. (PubMed)
- Deandrea S, Lucenteforte E, Bravi F, Foschi R, La Vecchia C, Negri E. Risk factors for falls in community-dwelling older people: a systematic review and meta-analysis. Epidemiology. 2010;21(5):658-668. (PubMed)
- Al-Khalidi B, Kimball SM, Rotondi MA, Ardern CI. Standardized serum 25-hydroxyvitamin D concentrations are inversely associated with cardiometabolic disease in US adults: a cross-sectional analysis of NHANES, 2001-2010. Nutr J. 2017;16(1):16. (PubMed)
- Cooper JD, Smyth DJ, Walker NM, et al. Inherited variation in vitamin D genes is associated with predisposition to autoimmune disease type 1 diabetes. Diabetes. 2011;60(5):1624-1631. (PubMed)
- Webb AR, Kline L, Holick MF. Influence of season and latitude on the cutaneous synthesis of vitamin D3: exposure to winter sunlight in Boston and Edmonton will not promote vitamin D3 synthesis in human skin. J Clin Endocrinol Metab. 1988;67(2):373-378. (PubMed)
- Nichols EK, Khatib IM, Aburto NJ, et al. Vitamin D status and determinants of deficiency among non-pregnant Jordanian women of reproductive age. Eur J Clin Nutr. 2012;66(6):751-756. (PubMed)
- Bassil D, Rahme M, Hoteit M, Fuleihan Gel H. Hypovitaminosis D in the Middle East and North Africa: prevalence, risk factors and impact on outcomes. Dermatoendocrinol. 2013;5(2):274-298. (PubMed)
- Balk SJ, Council on Environmental H, Section on D. Ultraviolet radiation: a hazard to children and adolescents. Pediatrics. 2011;127(3):e791-817. (PubMed)
- Dawodu A, Tsang RC. Maternal vitamin D status: effect on milk vitamin D content and vitamin D status of breastfeeding infants. Adv Nutr. 2012;3(3):353-361. (PubMed)
- Thiele DK, Senti JL, Anderson CM. Maternal vitamin D supplementation to meet the needs of the breastfed infant: a systematic review. J Hum Lact. 2013;29(2):163-170. (PubMed)
- Wharton B, Bishop N. Rickets. Lancet. 2003;362(9393):1389-1400. (PubMed)
- Chen TC, Chimeh F, Lu Z, et al. Factors that influence the cutaneous synthesis and dietary sources of vitamin D. Arch Biochem Biophys. 2007;460(2):213-217. (PubMed)
- Wang TJ, Zhang F, Richards JB, et al. Common genetic determinants of vitamin D insufficiency: a genome-wide association study. Lancet. 2010;376(9736):180-188. (PubMed)
- Ahn J, Yu K, Stolzenberg-Solomon R, et al. Genome-wide association study of circulating vitamin D levels. Hum Mol Genet. 2010;19(13):2739-2745. (PubMed)
- Wang W, Ingles SA, Torres-Mejia G, et al. Genetic variants and non-genetic factors predict circulating vitamin D levels in Hispanic and non-Hispanic White women: the Breast Cancer Health Disparities Study. Int J Mol Epidemiol Genet. 2014;5(1):31-46. (PubMed)
- Elkum N, Alkayal F, Noronha F, et al. Vitamin D insufficiency in Arabs and South Asians positively associates with polymorphisms in GC and CYP2R1 genes. PLoS One. 2014;9(11):e113102. (PubMed)
- Zhang Y, Yang S, Liu Y, Ren L. Relationship between polymorphisms in vitamin D metabolism-related genes and the risk of rickets in Han Chinese children. BMC Med Genet. 2013;14:101. (PubMed)
- Holick MF, Binkley NC, Bischoff-Ferrari HA, et al. Evaluation, treatment, and prevention of vitamin D deficiency: an Endocrine Society clinical practice guideline. J Clin Endocrinol Metab. 2011;96(7):1911-1930. (PubMed)
- Harris SS, Soteriades E, Coolidge JA, Mudgal S, Dawson-Hughes B. Vitamin D insufficiency and hyperparathyroidism in a low income, multiracial, elderly population. J Clin Endocrinol Metab. 2000;85(11):4125-4130. (PubMed)
- Allain TJ, Dhesi J. Hypovitaminosis D in older adults. Gerontology. 2003;49(5):273-278. (PubMed)
- Doorenbos CR, van den Born J, Navis G, de Borst MH. Possible renoprotection by vitamin D in chronic renal disease: beyond mineral metabolism. Nat Rev Nephrol. 2009;5(12):691-700. (PubMed)
- Pappa HM, Bern E, Kamin D, Grand RJ. Vitamin D status in gastrointestinal and liver disease. Curr Opin Gastroenterol. 2008;24(2):176-183. (PubMed)
- Jahnsen J, Falch JA, Mowinckel P, Aadland E. Vitamin D status, parathyroid hormone and bone mineral density in patients with inflammatory bowel disease. Scand J Gastroenterol. 2002;37(2):192-199. (PubMed)
- Arunabh S, Pollack S, Yeh J, Aloia JF. Body fat content and 25-hydroxyvitamin D levels in healthy women. J Clin Endocrinol Metab. 2003;88(1):157-161. (PubMed)
- Gallagher JC, Yalamanchili V, Smith LM. The effect of vitamin D supplementation on serum 25(OH)D in thin and obese women. J Steroid Biochem Mol Biol. 2013;136:195-200. (PubMed)
- Deng X, Song Y, Manson JE, et al. Magnesium, vitamin D status and mortality: results from US National Health and Nutrition Examination Survey (NHANES) 2001 to 2006 and NHANES III. BMC Med. 2013;11:187. (PubMed)
- Sempos CT, Durazo-Arvizu RA, Binkley N, Jones J, Merkel JM, Carter GD. Developing vitamin D dietary guidelines and the lack of 25-hydroxyvitamin D assay standardization: The ever-present past. J Steroid Biochem Mol Biol. 2016;164:115-119. (PubMed)
- Chapuy MC, Preziosi P, Maamer M, et al. Prevalence of vitamin D insufficiency in an adult normal population. Osteoporos Int. 1997;7(5):439-443. (PubMed)
- Thomas MK, Lloyd-Jones DM, Thadhani RI, et al. Hypovitaminosis D in medical inpatients. N Engl J Med. 1998;338(12):777-783. (PubMed)
- Heaney RP, Dowell MS, Hale CA, Bendich A. Calcium absorption varies within the referencia range for serum 25-hydroxyvitamin D. J Am Coll Nutr. 2003;22(2):142-146. (PubMed)
- Valcour A, Blocki F, Hawkins DM, Rao SD. Effects of age and serum 25-OH-vitamin D on serum parathyroid hormone levels. J Clin Endocrinol Metab. 2012;97(11):3989-3995. (PubMed)
- Ginde AA, Wolfe P, Camargo CA, Jr., Schwartz RS. Defining vitamin D status by secondary hyperparathyroidism in the US population. J Endocrinol Invest. 2012;35(1):42-48. (PubMed)
- Gallagher JC, Yalamanchili V, Smith LM. The effect of vitamin D on calcium absorption in older women. J Clin Endocrinol Metab. 2012;97(10):3550-3556. (PubMed)
- Looker AC, Johnson CL, Lacher DA, Pfeiffer CM, Schleicher RL, Sempos CT. Vitamin D status: United States, 2001-2006. NCHS Data Brief. 2011(59):1-8. (PubMed)
- Food and Nutrition Board, Institute of Medicine. Dietary referencia Intakes for Calcium and Vitamin D. Washington, D.C.: The National Academies Press; 2011. (The National Academies Press)
- Mithal A, Wahl DA, Bonjour JP, et al. Global vitamin D status and determinants of hypovitaminosis D. Osteoporos Int. 2009;20(11):1807-1820. (PubMed)
- Powe CE, Evans MK, Wenger J, et al. Vitamin D-binding protein and vitamin D status of black Americans and white Americans. N Engl J Med. 2013;369(21):1991-2000. (PubMed)
- Durazo-Arvizu RA, Dawson-Hughes B, Kramer H, et al. The reverse J-shaped association between serum total 25-hydroxyvitamin D concentration and all-cause mortality: the impact of assay standardization. Am J Epidemiol. 2017;185(8):720-726. (PubMed)
- Gaksch M, Jorde R, Grimnes G, et al. Vitamin D and mortality: Individual participant data meta-analysis of standardized 25-hydroxyvitamin D in 26916 individuals from a European consortium. PLoS One. 2017;12(2):e0170791. (PubMed)
- Chowdhury R, Kunutsor S, Vitezova A, et al. Vitamin D and risk of cause specific death: systematic review and meta-analysis of observational cohort and randomised intervention studies. BMJ. 2014;348:g1903. (PubMed)
- Gupta V, Walia GK, Sachdeva MP. 'Mendelian randomization': an approach for exploring causal relations in epidemiology. Public Health. 2017;145:113-119. (PubMed)
- Afzal S, Brondum-Jacobsen P, Bojesen SE, Nordestgaard BG. Genetically low vitamin D concentrations and increased mortality: Mendelian randomisation analysis in three large cohorts. BMJ. 2014;349:g6330. (PubMed)
- Bjelakovic G, Gluud LL, Nikolova D, et al. Vitamin D supplementation for prevention of mortality in adults. Cochrane Database Syst Rev. 2014(1):Cd007470. (PubMed)
- Wacker M, Holick MF. Vitamin D - effects on skeletal and extraskeletal health and the need for supplementation. Nutrients. 2013;5(1):111-148. (PubMed)
- Lips P, Hosking D, Lippuner K, et al. The prevalence of vitamin D inadequacy amongst women with osteoporosis: an international epidemiological investigation. J Intern Med. 2006;260(3):245-254. (PubMed)
- Torbergsen AC, Watne LO, Wyller TB, et al. Vitamin K1 and 25(OH)D are independently and synergistically associated with a risk for hip fracture in an elderly population: A case control study. Clin Nutr. 2015;34(1):101-106. (PubMed)
- Lips P, van Schoor NM. The effect of vitamin D on bone and osteoporosis. Best Pract Res Clin Endocrinol Metab. 2011;25(4):585-591. (PubMed)
- Reid IR, Bolland MJ, Grey A. Effects of vitamin D supplements on bone mineral density: a systematic review and meta-analysis. Lancet. 2014;383(9912):146-155. (PubMed)
- Rosen CJ. Vitamin D supplementation: bones of contention. Lancet. 2014;383(9912):108-110. (PubMed)
- Mocanu V, Vieth R. Three-year follow-up of serum 25-hydroxyvitamin D, parathyroid hormone, and bone mineral density in nursing home residents who had received 12 months of daily bread fortification with 125 mug of vitamin D3. Nutr J. 2013;12:137. (PubMed)
- Feskanich D, Willett WC, Colditz GA. Calcium, vitamin D, milk consumption, and hip fractures: a prospective study among postmenopausal women. Am J Clin Nutr. 2003;77(2):504-511. (PubMed)
- Jackson RD, LaCroix AZ, Gass M, et al. Calcium plus vitamin D supplementation and the risk of fractures. N Engl J Med. 2006;354(7):669-683. (PubMed)
- Wang Y, Wactawski-Wende J, Sucheston-Campbell LE, et al. The influence of genetic susceptibility and calcium plus vitamin D supplementation on fracture risk. Am J Clin Nutr. 2017;105(4):970-979. (PubMed)
- Gurney EP, Nachtigall MJ, Nachtigall LE, Naftolin F. The Women's Health Initiative trial and related studies: 10 years later: a clinician's view. J Steroid Biochem Mol Biol. 2014;142:4-11. (PubMed)
- Grant AM, Avenell A, Campbell MK, et al. Oral vitamin D3 and calcium for secondary prevention of low-trauma fractures in elderly people (Randomised Evaluation of Calcium Or vitamin D, RECORD): a randomised placebo-controlled trial. Lancet. 2005;365(9471):1621-1628. (PubMed)
- Bischoff-Ferrari HA, Giovannucci E, Willett WC, Dietrich T, Dawson-Hughes B. Estimation of optimal serum concentrations of 25-hydroxyvitamin D for multiple health outcomes. Am J Clin Nutr. 2006;84(1):18-28. (PubMed)
- Khaw KT, Stewart AW, Waayer D, et al. Effect of monthly high-dose vitamin D supplementation on falls and non-vertebral fractures: secondary and post-hoc outcomes from the randomised, double-blind, placebo-controlled ViDA trial. Lancet Diabetes Endocrinol. 2017;5(6):438-447. (PubMed)
- Chung M, Lee J, Terasawa T, Lau J, Trikalinos TA. Vitamin D with or without calcium supplementation for prevention of cancer and fractures: an updated meta-analysis for the US Preventive Services Task Force. Ann Intern Med. 2011;155(12):827-838. (PubMed)
- Bischoff-Ferrari HA, Willett WC, Orav EJ, et al. A pooled analysis of vitamin D dose requirements for fracture prevention. N Engl J Med. 2012;367(1):40-49. (PubMed)
- Avenell A, Mak JC, O'Connell D. Vitamin D and vitamin D analogues for preventing fractures in post-menopausal women and older men. Cochrane Database Syst Rev. 2014;4:CD000227. (PubMed)
- Annweiler C, Beauchet O. Questioning vitamin D status of elderly fallers and nonfallers: a meta-analysis to address a 'forgotten step'. J Intern Med. 2015;277(1):16-44. (PubMed)
- Cangussu LM, Nahas-Neto J, Orsatti CL, Bueloni-Dias FN, Nahas EA. Effect of vitamin D supplementation alone on muscle function in postmenopausal women: a randomized, double-blind, placebo-controlled clinical trial. Osteoporos Int. 2015;26(10):2413-2421. (PubMed)
- Cangussu LM, Nahas-Neto J, Orsatti CL, et al. Effect of isolated vitamin D supplementation on the rate of falls and postural balance in postmenopausal women fallers: a randomized, double-blind, placebo-controlled trial. Menopause. 2016;23(3):267-274. (PubMed)
- Bischoff-Ferrari HA, Dawson-Hughes B, Orav EJ, et al. Monthly high-dose vitamin D treatment for the prevention of functional decline: a randomized clinical trial. JAMA Intern Med. 2016;176(2):175-183. (PubMed)
- Murad MH, Elamin KB, Abu Elnour NO, et al. Clinical review: The effect of vitamin D on falls: a systematic review and meta-analysis. J Clin Endocrinol Metab. 2011;96(10):2997-3006. (PubMed)
- Boonen S, Lips P, Bouillon R, Bischoff-Ferrari HA, Vanderschueren D, Haentjens P. Need for additional calcium to reduce the risk of hip fracture with vitamin d supplementation: evidence from a comparative metaanalysis of randomized controlled trials. J Clin Endocrinol Metab. 2007;92(4):1415-1423. (PubMed)
- Grant WB. Update on evidence that support a role of solar ultraviolet-B irradiance in reducing cancer risk. Anticancer Agents Med Chem. 2013;13(1):140-146. (PubMed)
- Yin L, Ordonez-Mena JM, Chen T, Schottker B, Arndt V, Brenner H. Circulating 25-hydroxyvitamin D serum concentration and total cancer incidence and mortality: a systematic review and meta-analysis. Prev Med. 2013;57(6):753-764. (PubMed)
- Gandini S, Gnagnarella P, Serrano D, Pasquali E, Raimondi S. Vitamin D receptor polymorphisms and cancer. Adv Exp Med Biol. 2014;810:69-105. (PubMed)
- Vaughan-Shaw PG, O'Sullivan F, Farrington SM, et al. The impact of vitamin D pathway genetic variation and circulating 25-hydroxyvitamin D on cancer outcome: systematic review and meta-analysis. Br J Cancer. 2017;116(8):1092-1110. (PubMed)
- Gombart AF, Luong QT, Koeffler HP. Vitamin D compounds: activity against microbes and cancer. Anticancer Res. 2006;26(4A):2531-2542. (PubMed)
- Thorne J, Campbell MJ. The vitamin D receptor in cancer. Proc Nutr Soc. 2008;67(2):115-127. (PubMed)
- Garland CF, Garland FC, Gorham ED. Calcium and vitamin D. Their potential roles in colon and breast cancer prevention. Ann N Y Acad Sci. 1999;889:107-119. (PubMed)
- Choi YJ, Kim YH, Cho CH, Kim SH, Lee JE. Circulating levels of vitamin D and colorectal adenoma: A case-control study and a meta-analysis. World J Gastroenterol. 2015;21(29):8868-8877. (PubMed)
- Gandini S, Boniol M, Haukka J, et al. Meta-analysis of observational studies of serum 25-hydroxyvitamin D levels and colorectal, breast and prostate cancer and colorectal adenoma. Int J Cancer. 2011;128(6):1414-1424. (PubMed)
- Ma Y, Zhang P, Wang F, Yang J, Liu Z, Qin H. Association between vitamin D and risk of colorectal cancer: a systematic review of prospective studies. J Clin Oncol. 2011;29(28):3775-3782. (PubMed)
- Touvier M, Chan DS, Lau R, et al. Meta-analyses of vitamin D intake, 25-hydroxyvitamin D status, vitamin D receptor polymorphisms, and colorectal cancer risk. Cancer Epidemiol Biomarkers Prev. 2011;20(5):1003-1016. (PubMed)
- Ekmekcioglu C, Haluza D, Kundi M. 25-Hydroxyvitamin D status and risk for colorectal cancer and type 2 diabetes mellitus: a systematic review and meta-analysis of epidemiological studies. Int J Environ Res Public Health. 2017;14(2). (PubMed)
- Gorham ED, Garland CF, Garland FC, et al. Optimal vitamin D status for colorectal cancer prevention: a quantitative meta analysis. Am J Prev Med. 2007;32(3):210-216. (PubMed)
- Cauley JA, Chlebowski RT, Wactawski-Wende J, et al. Calcium plus vitamin D supplementation and health outcomes five years after active intervention ended: the Women's Health Initiative. J Womens Health (Larchmt). 2013;22(11):915-929. (PubMed)
- Baron JA, Barry EL, Mott LA, et al. A trial of calcium and vitamin D for the prevention of colorectal adenomas. N Engl J Med. 2015;373(16):1519-1530. (PubMed)
- Holick MF. Calcium plus vitamin D and the risk of colorectal cancer. N Engl J Med. 2006;354(21):2287-2288; author reply 2287-2288. (PubMed)
- Barry EL, Peacock JL, Rees JR, et al. Vitamin D receptor genotype, vitamin D3 supplementation, and risk of colorectal adenomas: a randomized clinical trial. JAMA Oncol. 2017;3(5):628-635. (PubMed)
- Hiraki LT, Joshi AD, Ng K, et al. Joint effects of colorectal cancer susceptibility loci, circulating 25-hydroxyvitamin D and risk of colorectal cancer. PLoS One. 2014;9(3):e92212. (PubMed)
- Vidigal VM, Silva TD, de Oliveira J, Pimenta CAM, Felipe AV, Forones NM. Genetic polymorphisms of vitamin D receptor (VDR), CYP27B1 and CYP24A1 genes and the risk of colorectal cancer. Int J Biol Markers. 2017;32(2):e224-e230. (PubMed)
- Maalmi H, Ordonez-Mena JM, Schottker B, Brenner H. Serum 25-hydroxyvitamin D levels and survival in colorectal and breast cancer patients: Systematic review and meta-analysis of prospective cohort studies. 2014;50(8):1510-1521. (PubMed)
- Mohr SB, Garland CF, Gorham ED, Grant WB, Garland FC. Relationship between low ultraviolet B irradiance and higher breast cancer risk in 107 countries. Breast J. 2008;14(3):255-260. (PubMed)
- John EM, Schwartz GG, Dreon DM, Koo J. Vitamin D and breast cancer risk: the NHANES I Epidemiologic follow-up study, 1971-1975 to 1992. National Health and Nutrition Examination Survey. Cancer Epidemiol Biomarkers Prev. 1999;8(5):399-406. (PubMed)
- Kim Y, Je Y. Vitamin D intake, blood 25(OH)D levels, and breast cancer risk or mortality: a meta-analysis. Br J Cancer. 2014;110(11):2772-2784. (PubMed)
- Wang D, Velez de-la-Paz OI, Zhai JX, Liu DW. Serum 25-hydroxyvitamin D and breast cancer risk: a meta-analysis of prospective studies. Tumour Biol. 2013;34(6):3509-3517. (PubMed)
- Rose AA, Elser C, Ennis M, Goodwin PJ. Blood levels of vitamin D and early stage breast cancer prognosis: a systematic review and meta-analysis. Breast Cancer Res Treat. 2013;141(3):331-339. (PubMed)
- Sperati F, Vici P, Maugeri-Sacca M, et al. Vitamin D supplementation and breast cancer prevention: a systematic review and meta-analysis of randomized clinical trials. PLoS One. 2013;8(7):e69269. (PubMed)
- Hu K, Callen DF, Li J, Zheng H. Circulating vitamin D and overall survival in breast cancer patients: a dose-response meta-analysis of cohort studies. Integr Cancer Ther. 2017:1534735417712007. (PubMed)
- Mohr SB, Gorham ED, Kim J, Hofflich H, Garland CF. Meta-analysis of vitamin D sufficiency for improving survival of patients with breast cancer. Anticancer Res. 2014;34(3):1163-1166. (PubMed)
- Lu D, Jing L, Zhang S. Vitamin D receptor polymorphism and breast cancer risk: a meta-analysis. Medicine (Baltimore). 2016;95(18):e3535. (PubMed)
- Mun MJ, Kim TH, Hwang JY, Jang WC. Vitamin D receptor gene polymorphisms and the risk for female reproductive cancers: A meta-analysis. Maturitas. 2015;81(2):256-265. (PubMed)
- Gilbert R, Martin RM, Beynon R, et al. Associations of circulating and dietary vitamin D with prostate cancer risk: a systematic review and dose-response meta-analysis. Cancer Causes Control. 2011;22(3):319-340. (PubMed)
- van der Rhee H, Coebergh JW, de Vries E. Is prevention of cancer by sun exposure more than just the effect of vitamin D? A systematic review of epidemiological studies. Eur J Cancer. 2013;49(6):1422-1436. (PubMed)
- Tuohimaa P, Tenkanen L, Ahonen M, et al. Both high and low levels of blood vitamin D are associated with a higher prostate cancer risk: a longitudinal, nested case-control study in the Nordic countries. Int J Cancer. 2004;108(1):104-108. (PubMed)
- Xu Y, Shao X, Yao Y, et al. Positive association between circulating 25-hydroxyvitamin D levels and prostate cancer risk: new findings from an updated meta-analysis. J Cancer Res Clin Oncol. 2014;140(9):1465-1477. (PubMed)
- Grant WB, Karras SN, Bischoff-Ferrari HA, et al. Do studies reporting 'U'-shaped serum 25-hydroxyvitamin D-health outcome relationships reflect adverse effects? Dermatoendocrinol. 2016;8(1):e1187349. (PubMed)
- Wu X, Cheng J, Yang K. Vitamin D-related gene polymorphisms, plasma 25-hydroxy-vitamin D, cigarette smoke and non-small cell lung cancer (NSCLC) Risk. Int J Mol Sci. 2016;17(10). (PubMed)
- Zhang L, Wang S, Che X, Li X. Vitamin D and lung cancer risk: a comprehensive review and meta-analysis. Cell Physiol Biochem. 2015;36(1):299-305. (PubMed)
- Liao Y, Huang JL, Qiu MX, Ma ZW. Impact of serum vitamin D level on risk of bladder cancer: a systemic review and meta-analysis. Tumour Biol. 2015;36(3):1567-1572. (PubMed)
- Zhang H, Zhang H, Wen X, Zhang Y, Wei X, Liu T. Vitamin D deficiency and increased risk of bladder carcinoma: a meta-analysis. Cell Physiol Biochem. 2015;37(5):1686-1692. (PubMed)
- Lu D, Chen J, Jin J. Vitamin D status and risk of non-Hodgkin lymphoma: a meta-analysis. Cancer Causes Control. 2014;25(11):1553-1563. (PubMed)
- Prescott J, Bertrand KA, Poole EM, Rosner BA, Tworoger SS. Surrogates of long-term vitamin d exposure and ovarian cancer risk in two prospective cohort studies. Cancers (Basel). 2013;5(4):1577-1600. (PubMed)
- Khayatzadeh S, Feizi A, Saneei P, Esmaillzadeh A. Vitamin D intake, serum Vitamin D levels, and risk of gastric cancer: A systematic review and meta-analysis. J Res Med Sci. 2015;20(8):790-796. (PubMed)
- Gandini S, Raimondi S, Gnagnarella P, Dore JF, Maisonneuve P, Testori A. Vitamin D and skin cancer: a meta-analysis. Eur J Cancer. 2009;45(4):634-641. (PubMed)
- Deluca HF, Cantorna MT. Vitamin D: its role and uses in immunology. Faseb J. 2001;15(14):2579-2585. (PubMed)
- Agmon-Levin N, Mosca M, Petri M, Shoenfeld Y. Systemic lupus erythematosus one disease or many? Autoimmun Rev. 2012;11(8):593-595. (PubMed)
- Goodin DS. The epidemiology of multiple sclerosis: insights to disease pathogenesis. Handb Clin Neurol. 2014;122:231-266. (PubMed)
- Littorin B, Blom P, Scholin A, et al. Lower levels of plasma 25-hydroxyvitamin D among young adults at diagnosis of autoimmune type 1 diabetes compared with control subjects: results from the nationwide Diabetes Incidence Study in Sweden (DISS). Diabetologia. 2006;49(12):2847-2852. (PubMed)
- Pozzilli P, Manfrini S, Crino A, et al. Low levels of 25-hydroxyvitamin D3 and 1,25-dihydroxyvitamin D3 in patients with newly diagnosed type 1 diabetes. Horm Metab Res. 2005;37(11):680-683. (PubMed)
- Raab J, Giannopoulou EZ, Schneider S, et al. Prevalence of vitamin D deficiency in pre-type 1 diabetes and its association with disease progression. Diabetologia. 2014;57(5):902-908. (PubMed)
- Hypponen E, Laara E, Reunanen A, Jarvelin MR, Virtanen SM. Intake of vitamin D and risk of type 1 diabetes: a birth-cohort study. Lancet. 2001;358(9292):1500-1503. (PubMed)
- Sorensen IM, Joner G, Jenum PA, Eskild A, Torjesen PA, Stene LC. Maternal serum levels of 25-hydroxy-vitamin D during pregnancy and risk of type 1 diabetes in the offspring. Diabetes. 2012;61(1):175-178. (PubMed)
- Brekke HK, Ludvigsson J. Vitamin D supplementation and diabetes-related autoimmunity in the ABIS study. Pediatr Diabetes. 2007;8(1):11-14. (PubMed)
- Fronczak CM, Baron AE, Chase HP, et al. In utero dietary exposures and risk of islet autoimmunity in children. Diabetes Care. 2003;26(12):3237-3242. (PubMed)
- Marjamaki L, Niinisto S, Kenward MG, et al. Maternal intake of vitamin D during pregnancy and risk of advanced beta cell autoimmunity and type 1 diabetes in offspring. Diabetologia. 2010;53(8):1599-1607. (PubMed)
- Miettinen ME, Reinert L, Kinnunen L, et al. Serum 25-hydroxyvitamin D level during early pregnancy and type 1 diabetes risk in the offspring. Diabetologia. 2012;55(5):1291-1294. (PubMed)
- Smolders J, Thewissen M, Peelen E, et al. Vitamin D status is positively correlated with regulatory T cell function in patients with multiple sclerosis. PLoS One. 2009;4(8):e6635. (PubMed)
- Mokry LE, Ross S, Ahmad OS, et al. Vitamin D and risk of multiple sclerosis: a Mendelian randomization study. PLoS Med. 2015;12(8):e1001866. (PubMed)
- Staples J, Ponsonby AL, Lim L. Low maternal exposure to ultraviolet radiation in pregnancy, month of birth, and risk of multiple sclerosis in offspring: longitudinal analysis. BMJ. 2010;340:c1640. (PubMed)
- Bjornevik K, Riise T, Casetta I, et al. Sun exposure and multiple sclerosis risk in Norway and Italy: The EnvIMS study. Mult Scler. 2014; 20(8):1042-1049. (PubMed)
- McDowell TY, Amr S, Culpepper WJ, et al. Sun exposure, vitamin D and age at disease onset in relapsing multiple sclerosis. Neuroepidemiology. 2011;36(1):39-45. (PubMed)
- Munger KL, Levin LI, Hollis BW, Howard NS, Ascherio A. Serum 25-hydroxyvitamin D levels and risk of multiple sclerosis. JAMA. 2006;296(23):2832-2838. (PubMed)
- Munger KL, Zhang SM, O'Reilly E, et al. Vitamin D intake and incidence of multiple sclerosis. Neurology. 2004;62(1):60-65. (PubMed)
- Pierrot-Deseilligny C, Rivaud-Pechoux S, Clerson P, de Paz R, Souberbielle JC. Relationship between 25-OH-D serum level and relapse rate in multiple sclerosis patients before and after vitamin D supplementation. Ther Adv Neurol Disord. 2012;5(4):187-198. (PubMed)
- Ascherio A, Munger KL, White R, et al. Vitamin d as an early predictor of multiple sclerosis activity and progression. JAMA Neurol. 2014;71(3):306-314. (PubMed)
- Muris AH, Smolders J, Rolf L, et al. Vitamin D status does not affect disability progression of patients with multiple sclerosis over three year follow-up. PLoS One. 2016;11(6):e0156122. (PubMed)
- Kampman MT, Steffensen LH, Mellgren SI, Jorgensen L. Effect of vitamin D3 supplementation on relapses, disease progression, and measures of function in persons with multiple sclerosis: exploratory outcomes from a double-blind randomised controlled trial. Mult Scler. 2012;18(8):1144-1151. (PubMed)
- Soilu-Hanninen M, Aivo J, Lindstrom BM, et al. A randomised, double blind, placebo controlled trial with vitamin D3 as an add on treatment to interferon beta-1b in patients with multiple sclerosis. J Neurol Neurosurg Psychiatry. 2012;83(5):565-571. (PubMed)
- Mrad MF, El Ayoubi NK, Esmerian MO, Kazan JM, Khoury SJ. Effect of vitamin D replacement on immunological biomarkers in patients with multiple sclerosis. Clin Immunol. 2017;181:9-15. (PubMed)
- Muris AH, Smolders J, Rolf L, Thewissen M, Hupperts R, Damoiseaux J. Immune regulatory effects of high dose vitamin D3 supplementation in a randomized controlled trial in relapsing remitting multiple sclerosis patients receiving IFNbeta; the SOLARIUM study. J Neuroimmunol. 2016;300:47-56. (PubMed)
- O'Connell K, Sulaimani J, Basdeo SA, et al. Effects of vitamin D3 in clinically isolated syndrome and healthy control participants: A double-blind randomised controlled trial. Mult Scler J Exp Transl Clin. 2017;3(3):2055217317727296. (PubMed)
- Rosjo E, Steffensen LH, Jorgensen L, et al. Vitamin D supplementation and systemic inflammation in relapsing-remitting multiple sclerosis. J Neurol. 2015;262(12):2713-2721. (PubMed)
- Sotirchos ES, Bhargava P, Eckstein C, et al. Safety and immunologic effects of high- vs low-dose cholecalciferol in multiple sclerosis. Neurology. 2016;86(4):382-390. (PubMed)
- Bruce D, Whitcomb JP, August A, McDowell MA, Cantorna MT. Elevated non-specific immunity and normal Listeria clearance in young and old vitamin D receptor knockout mice. Int Immunol. 2009;21(2):113-122. (PubMed)
- Zwerina K, Baum W, Axmann R, et al. Vitamin D receptor regulates TNF-mediated arthritis. Ann Rheum Dis. 2011;70(6):1122-1129. (PubMed)
- Hitchon CA, Sun Y, Robinson DB, et al. Vitamin D receptor polymorphism rs2228570 (Fok1) is associated with rheumatoid arthritis in North American natives. J Rheumatol. 2012;39(9):1792-1797. (PubMed)
- Lee YH, Bae SC, Choi SJ, Ji JD, Song GG. Associations between vitamin D receptor polymorphisms and susceptibility to rheumatoid arthritis and systemic lupus erythematosus: a meta-analysis. Mol Biol Rep. 2011;38(6):3643-3651. (PubMed)
- Mosaad YM, Hammad EM, Fawzy Z, et al. Vitamin D receptor gene polymorphism as possible risk factor in rheumatoid arthritis and rheumatoid related osteoporosis. Hum Immunol. 2014;75(5):452-461. (PubMed)
- Zanetti M, Harris SS, Dawson-Hughes B. Ability of vitamin D to reduce inflammation in adults without acute illness. Nutr Rev. 2014;72(2):95-98. (PubMed)
- Merlino LA, Curtis J, Mikuls TR, Cerhan JR, Criswell LA, Saag KG. Vitamin D intake is inversely associated with rheumatoid arthritis: results from the Iowa Women's Health Study. Arthritis Rheum. 2004;50(1):72-77. (PubMed)
- Costenbader KH, Feskanich D, Holmes M, Karlson EW, Benito-Garcia E. Vitamin D intake and risks of systemic lupus erythematosus and rheumatoid arthritis in women. Ann Rheum Dis. 2008;67(4):530-535. (PubMed)
- Hiraki LT, Munger KL, Costenbader KH, Karlson EW. Dietary intake of vitamin D during adolescence and risk of adult-onset systemic lupus erythematosus and rheumatoid arthritis. Arthritis Care Res (Hoboken). 2012;64(12):1829-1836. (PubMed)
- Sen D, Ranganathan P. Vitamin D in rheumatoid arthritis: panacea or placebo? Discov Med. 2012;14(78):311-319. (PubMed)
- Lee YH, Bae SC. Vitamin D level in rheumatoid arthritis and its correlation with the disease activity: a meta-analysis. Clin Exp Rheumatol. 2016;34(5):827-833. (PubMed)
- Lin J, Liu J, Davies ML, Chen W. Serum vitamin D level and rheumatoid arthritis disease activity: review and meta-analysis. PLoS One. 2016;11(1):e0146351. (PubMed)
- Hansen KE, Bartels CM, Gangnon RE, Jones AN, Gogineni J. An evaluation of high-dose vitamin D for rheumatoid arthritis. J Clin Rheumatol. 2014;20(2):112-114. (PubMed)
- Buondonno I, Rovera G, Sassi F, et al. Vitamin D and immunomodulation in early rheumatoid arthritis: A randomized double-blind placebo-controlled study. PLoS One. 2017;12(6):e0178463. (PubMed)
- Dehghan A, Rahimpour S, Soleymani-Salehabadi H, Owlia MB. Role of vitamin D in flare ups of rheumatoid arthritis. Z Rheumatol. 2014;73(5):461-464. (PubMed)
- Yang J, Liu L, Zhang Q, Li M, Wang J. Effect of vitamin D on the recurrence rate of rheumatoid arthritis. Exp Ther Med. 2015;10(5):1812-1816. (PubMed)
- Gonzalez LA, Toloza SM, McGwin G, Jr., Alarcon GS. Ethnicity in systemic lupus erythematosus (SLE): its influence on susceptibility and outcomes. Lupus. 2013;22(12):1214-1224. (PubMed)
- Hsieh CC, Lin BF. Dietary factors regulate cytokines in murine models of systemic lupus erythematosus. Autoimmun Rev. 2011;11(1):22-27. (PubMed)
- Mao S, Huang S. Association between vitamin D receptor gene BsmI, FokI, ApaI and TaqI polymorphisms and the risk of systemic lupus erythematosus: a meta-analysis. Rheumatol Int. 2014;34(3):381-388. (PubMed)
- Monticielo OA, Teixeira Tde M, Chies JA, Brenol JC, Xavier RM. Vitamin D and polymorphisms of VDR gene in patients with systemic lupus erythematosus. Clin Rheumatol. 2012;31(10):1411-1421. (PubMed)
- Ruiz-Irastorza G, Egurbide MV, Olivares N, Martinez-Berriotxoa A, Aguirre C. Vitamin D deficiency in systemic lupus erythematosus: prevalence, predictors and clinical consequences. Rheumatology (Oxford). 2008;47(6):920-923. (PubMed)
- Toloza SM, Cole DE, Gladman DD, Ibanez D, Urowitz MB. Vitamin D insufficiency in a large female SLE cohort. Lupus. 2010;19(1):13-19. (PubMed)
- Amital H, Szekanecz Z, Szucs G, et al. Serum concentrations of 25-OH vitamin D in patients with systemic lupus erythematosus (SLE) are inversely related to disease activity: is it time to routinely supplement patients with SLE with vitamin D? Ann Rheum Dis. 2010;69(6):1155-1157. (PubMed)
- Terrier B, Derian N, Schoindre Y, et al. Restoration of regulatory and effector T cell balance and B cell homeostasis in systemic lupus erythematosus patients through vitamin D supplementation. Arthritis Res Ther. 2012;14(5):R221. (PubMed)
- Cutillas-Marco E, Marquina-Vila A, Grant W, Vilata-Corell J, Morales-Suarez-Varela M. Vitamin D and cutaneous lupus erythematosus: effect of vitamin D replacement on disease severity. Lupus. 2014;23(7):615-623. (PubMed)
- Abou-Raya A, Abou-Raya S, Helmii M. The effect of vitamin D supplementation on inflammatory and hemostatic markers and disease activity in patients with systemic lupus erythematosus: a randomized placebo-controlled trial. J Rheumatol. 2013;40(3):265-272. (PubMed)
- Lima GL, Paupitz J, Aikawa NE, Takayama L, Bonfa E, Pereira RM. Vitamin D supplementation in adolescents and young adults With juvenile systemic lupus erythematosus for improvement in disease activity and fatigue scores: a randomized, double-blind, placebo-controlled trial. Arthritis Care Res (Hoboken). 2016;68(1):91-98. (PubMed)
- Andreoli L, Dall'Ara F, Piantoni S, et al. A 24-month prospective study on the efficacy and safety of two different monthly regimens of vitamin D supplementation in pre-menopausal women with systemic lupus erythematosus. Lupus. 2015;24(4-5):499-506. (PubMed)
- Karimzadeh H, Shirzadi M, Karimifar M. The effect of Vitamin D supplementation in disease activity of systemic lupus erythematosus patients with Vitamin D deficiency: A randomized clinical trial. J Res Med Sci. 2017;22:4. (PubMed)
- Antico A, Tampoia M, Tozzoli R, Bizzaro N. Can supplementation with vitamin D reduce the risk or modify the course of autoimmune diseases? A systematic review of the literature. Autoimmun Rev. 2012;12(2):127-136. (PubMed)
- Wang TJ, Pencina MJ, Booth SL, et al. Vitamin D deficiency and risk of cardiovascular disease. Circulation. 2008;117(4):503-511. (PubMed)
- van Ballegooijen AJ, Kestenbaum B, Sachs MC, et al. Association of 25-Hydroxyvitamin D and parathyroid hormone with incident hypertension: MESA (Multi-Ethnic Study of Atherosclerosis). J Am Coll Cardiol. 2014;63(12):1214-1222. (PubMed)
- Kunutsor SK, Apekey TA, Steur M. Vitamin D and risk of future hypertension: meta-analysis of 283,537 participants. Eur J Epidemiol. 2013;28(3):205-221. (PubMed)
- Burgaz A, Orsini N, Larsson SC, Wolk A. Blood 25-hydroxyvitamin D concentration and hypertension: a meta-analysis. J Hypertens. 2011;29(4):636-645. (PubMed)
- Moody WE, Edwards NC, Madhani M, et al. Endothelial dysfunction and cardiovascular disease in early-stage chronic kidney disease: cause or association? Atherosclerosis. 2012;223(1):86-94. (PubMed)
- Chitalia N, Recio-Mayoral A, Kaski JC, Banerjee D. Vitamin D deficiency and endothelial dysfunction in non-dialysis chronic kidney disease patients. Atherosclerosis. 2012;220(1):265-268. (PubMed)
- Chitalia N, Ismail T, Tooth L, et al. Impact of vitamin d supplementation on arterial vasomotion, stiffness and endothelial biomarkers in chronic kidney disease patients. PLoS One. 2014;9(3):e91363. (PubMed)
- Mazidi M, Karimi E, Rezaie P, Vatanparast H. The impact of vitamin D supplement intake on vascular endothelial function; a systematic review and meta-analysis of randomized controlled trials. Food Nutr Res. 2017;61(1):1273574. (PubMed)
- Messa P, Curreri M, Regalia A, Alfieri CM. Vitamin D and the cardiovascular system: an overview of the recent literature. Am J Cardiovasc Drugs. 2014;14(1):1-14. (PubMed)
- Brondum-Jacobsen P, Benn M, Afzal S, Nordestgaard BG. No evidence that genetically reduced 25-hydroxyvitamin D is associated with increased risk of ischaemic heart disease or myocardial infarction: a Mendelian randomization study. Int J Epidemiol. 2015;44(2):651-661. (PubMed)
- Manousaki D, Mokry LE, Ross S, Goltzman D, Richards JB. Mendelian randomization studies do not support a role for vitamin D in coronary artery disease. Circ Cardiovasc Genet. 2016;9(4):349-356. (PubMed)
- Ford JA, MacLennan GS, Avenell A, Bolland M, Grey A, Witham M. Cardiovascular disease and vitamin D supplementation: trial analysis, systematic review, and meta-analysis. Am J Clin Nutr. 2014;100(3):746-755. (PubMed)
- Chin K, Appel LJ, Michos ED. Vitamin D, calcium, and cardiovascular disease: a"D"vantageous or "D"etrimental? An era of uncertainty. Curr Atheroscler Rep. 2017;19(1):5. (PubMed)
- Pradhan AD, Manson JE. Update on the Vitamin D and OmegA-3 trial (VITAL). J Steroid Biochem Mol Biol. 2016;155(Pt B):252-256. (PubMed)
- Neale RE, Armstrong BK, Baxter C, et al. The D-Health Trial: A randomized trial of vitamin D for prevention of mortality and cancer. Contemp Clin Trials. 2016;48:83-90. (PubMed)
- Scragg R, Stewart AW, Waayer D, et al. Effect of monthly high-dose vitamin D supplementation on cardiovascular disease in the vitamin D assessment study: a randomized clinical trial. JAMA Cardiol. 2017;2(6):608-616. (PubMed)
- Thomas GN, o Hartaigh B, Bosch JA, et al. Vitamin D levels predict all-cause and cardiovascular disease mortality in subjects with the metabolic syndrome: the Ludwigshafen Risk and Cardiovascular Health (LURIC) Study. Diabetes Care. 2012;35(5):1158-1164. (PubMed)
- Chiu KC, Chu A, Go VL, Saad MF. Hypovitaminosis D is associated with insulin resistance and beta cell dysfunction. Am J Clin Nutr. 2004;79(5):820-825. (PubMed)
- Shankar A, Sabanayagam C, Kalidindi S. Serum 25-hydroxyvitamin D levels and prediabetes among subjects free of diabetes. Diabetes Care. 2011;34(5):1114-1119. (PubMed)
- Deleskog A, Hilding A, Brismar K, Hamsten A, Efendic S, Ostenson CG. Low serum 25-hydroxyvitamin D level predicts progression to type 2 diabetes in individuals with prediabetes but not with normal glucose tolerance. Diabetologia. 2012;55(6):1668-1678. (PubMed)
- Khan H, Kunutsor S, Franco OH, Chowdhury R. Vitamin D, type 2 diabetes and other metabolic outcomes: a systematic review and meta-analysis of prospective studies. Proc Nutr Soc. 2013;72(1):89-97. (PubMed)
- Lucato P, Solmi M, Maggi S, et al. Low vitamin D levels increase the risk of type 2 diabetes in older adults: A systematic review and meta-analysis. Maturitas. 2017;100:8-15. (PubMed)
- George PS, Pearson ER, Witham MD. Effect of vitamin D supplementation on glycaemic control and insulin resistance: a systematic review and meta-analysis. Diabet Med. 2012;29(8):e142-150. (PubMed)
- Gulseth HL, Wium C, Angel K, Eriksen EF, Birkeland KI. Effects of vitamin D supplementation on insulin sensitivity and insulin secretion in subjects with type 2 diabetes and vitamin D deficiency: a randomized controlled trial. Diabetes Care. 2017;40(7):872-878. (PubMed)
- Lee CJ, Iyer G, Liu Y, et al. The effect of vitamin D supplementation on glucose metabolism in type 2 diabetes mellitus: A systematic review and meta-analysis of intervention studies. J Diabetes Complications. 2017;31(7):1115-1126. (PubMed)
- Talaei A, Mohamadi M, Adgi Z. The effect of vitamin D on insulin resistance in patients with type 2 diabetes. Diabetol Metab Syndr. 2013;5(1):8. (PubMed)
- Gezen-Ak D, Yilmazer S, Dursun E. Why vitamin d in Alzheimer's disease? The hypothesis. J Alzheimers Dis. 2014;40(2):257-269. (PubMed)
- Landel V, Annweiler C, Millet P, Morello M, Feron F. Vitamin D, cognition and Alzheimer's disease: the therapeutic benefit is in the D-tails. J Alzheimers Dis. 2016;53(2):419-444. (PubMed)
- Annweiler C, Schott AM, Rolland Y, Blain H, Herrmann FR, Beauchet O. Dietary intake of vitamin D and cognition in older women: a large population-based study. Neurology. 2010;75(20):1810-1816. (PubMed)
- Annweiler C, Rolland Y, Schott AM, et al. Higher vitamin D dietary intake is associated with lower risk of Alzheimer's disease: a 7-year follow-up. J Gerontol A Biol Sci Med Sci. 2012;67(11):1205-1211. (PubMed)
- Annweiler C, Fantino B, Schott AM, Krolak-Salmon P, Allali G, Beauchet O. Vitamin D insufficiency and mild cognitive impairment: cross-sectional association. Eur J Neurol. 2012;19(7):1023-1029. (PubMed)
- Hooshmand B, Lokk J, Solomon A, et al. Vitamin D in relation to cognitive impairment, cerebrospinal fluid biomarkers, and brain volumes. J Gerontol A Biol Sci Med Sci. 2014;69(9):1132-1138. (PubMed)
- Slinin Y, Paudel ML, Taylor BC, et al. 25-Hydroxyvitamin D levels and cognitive performance and decline in elderly men. Neurology. 2010;74(1):33-41. (PubMed)
- Slinin Y, Paudel M, Taylor BC, et al. Association between serum 25(OH) vitamin D and the risk of cognitive decline in older women. J Gerontol A Biol Sci Med Sci. 2012;67(10):1092-1098. (PubMed)
- Annweiler C, Milea D, Whitson HE, et al. Vitamin D insufficiency and cognitive impairment in Asians: a multi-ethnic population-based study and meta-analysis. J Intern Med. 2016;280(3):300-311. (PubMed)
- Annweiler C, Llewellyn DJ, Beauchet O. Low serum vitamin D concentrations in Alzheimer's disease: a systematic review and meta-analysis. J Alzheimers Dis. 2013;33(3):659-674. (PubMed)
- Balion C, Griffith LE, Strifler L, et al. Vitamin D, cognition, and dementia: a systematic review and meta-analysis. Neurology. 2012;79(13):1397-1405. (PubMed)
- Lopes da Silva S, Vellas B, Elemans S, et al. Plasma nutrient status of patients with Alzheimer's disease: Systematic review and meta-analysis. Alzheimers Dement. 2014;10(4):485-502. (PubMed)
- Shen L, Ji HF. Vitamin D deficiency is associated with increased risk of Alzheimer's disease and dementia: evidence from meta-analysis. Nutr J. 2015;14:76. (PubMed)
- Sommer I, Griebler U, Kien C, et al. Vitamin D deficiency as a risk factor for dementia: a systematic review and meta-analysis. BMC Geriatr. 2017;17(1):16. (PubMed)
- Olsson E, Byberg L, Karlstrom B, et al. Vitamin D is not associated with incident dementia or cognitive impairment: an 18-y follow-up study in community-living old men. Am J Clin Nutr. 2017;105(4):936-943. (PubMed)
- Mokry LE, Ross S, Morris JA, Manousaki D, Forgetta V, Richards JB. Genetically decreased vitamin D and risk of Alzheimer disease. Neurology. 2016;87(24):2567-2574. (PubMed)
- Annweiler C, Montero-Odasso M, Llewellyn DJ, Richard-Devantoy S, Duque G, Beauchet O. Meta-analysis of memory and executive dysfunctions in relation to vitamin D. J Alzheimers Dis. 2013;37(1):147-171. (PubMed)
- Annweiler C, Fantino B, Gautier J, Beaudenon M, Thiery S, Beauchet O. Cognitive effects of vitamin D supplementation in older outpatients visiting a memory clinic: a pre-post study. J Am Geriatr Soc. 2012;60(4):793-795. (PubMed)
- Stein MS, Scherer SC, Ladd KS, Harrison LC. A randomized controlled trial of high-dose vitamin D2 followed by intranasal insulin in Alzheimer's disease. J Alzheimers Dis. 2011;26(3):477-484. (PubMed)
- Annweiler C, Karras SN, Anagnostis P, Beauchet O. Vitamin D supplements: a novel therapeutic approach for Alzheimer patients. Front Pharmacol. 2014;5:6. (PubMed)
- Sato Y, Kikuyama M, Oizumi K. High prevalence of vitamin D deficiency and reduced bone mass in Parkinson's disease. Neurology. 1997;49(5):1273-1278. (PubMed)
- Evatt ML, Delong MR, Khazai N, Rosen A, Triche S, Tangpricha V. Prevalence of vitamin D insufficiency in patients with Parkinson disease and Alzheimer disease. Arch Neurol. 2008;65(10):1348-1352. (PubMed)
- Knekt P, Kilkkinen A, Rissanen H, Marniemi J, Saaksjarvi K, Heliovaara M. Serum vitamin D and the risk of Parkinson disease. Arch Neurol. 2010;67(7):808-811. (PubMed)
- Lv Z, Qi H, Wang L, et al. Vitamin D status and Parkinson's disease: a systematic review and meta-analysis. Neurol Sci. 2014;35(11):1723-1730. (PubMed)
- Shen L, Ji HF. Associations between vitamin D status, supplementation, outdoor work and risk of Parkinson's disease: a meta-analysis assessment. Nutrients. 2015;7(6):4817-4827. (PubMed)
- Zhao Y, Sun Y, Ji HF, Shen L. Vitamin D levels in Alzheimer's and Parkinson's diseases: a meta-analysis. Nutrition. 2013;29(6):828-832. (PubMed)
- Suzuki M, Yoshioka M, Hashimoto M, et al. Randomized, double-blind, placebo-controlled trial of vitamin D supplementation in Parkinson disease. Am J Clin Nutr. 2013;97(5):1004-1013. (PubMed)
- Dobson R, Yarnall A, Noyce AJ, Giovannoni G. Bone health in chronic neurological diseases: a focus on multiple sclerosis and parkinsonian syndromes. Pract Neurol. 2013;13(2):70-79. (PubMed)
- Torsney KM, Noyce AJ, Doherty KM, Bestwick JP, Dobson R, Lees AJ. Bone health in Parkinson's disease: a systematic review and meta-analysis. J Neurol Neurosurg Psychiatry. 2014;85(10):1159-66. (PubMed)
- van den Bos F, Speelman AD, Samson M, Munneke M, Bloem BR, Verhaar HJ. Parkinson's disease and osteoporosis. Age Ageing. 2013;42(2):156-162. (PubMed)
- Sato Y, Iwamoto J, Honda Y. Amelioration of osteoporosis and hypovitaminosis D by sunlight exposure in Parkinson's disease. Parkinsonism Relat Disord. 2011;17(1):22-26. (PubMed)
- Aghajafari F, Nagulesapillai T, Ronksley PE, Tough SC, O'Beirne M, Rabi DM. Association between maternal serum 25-hydroxyvitamin D level and pregnancy and neonatal outcomes: systematic review and meta-analysis of observational studies. BMJ. 2013;346:f1169. (PubMed)
- Perez-Lopez FR, Pasupuleti V, Mezones-Holguin E, et al. Effect of vitamin D supplementation during pregnancy on maternal and neonatal outcomes: a systematic review and meta-analysis of randomized controlled trials. Fertil Steril. 2015;103(5):1278-1288.e1274. (PubMed)
- Alzaim M, Wood RJ. Vitamin D and gestational diabetes mellitus. Nutr Rev. 2013;71(3):158-167. (PubMed)
- Lacroix M, Battista MC, Doyon M, et al. Lower vitamin D levels at first trimester are associated with higher risk of developing gestational diabetes mellitus. Acta Diabetol. 2014;51(4):609-616. (PubMed)
- Parlea L, Bromberg IL, Feig DS, Vieth R, Merman E, Lipscombe LL. Association between serum 25-hydroxyvitamin D in early pregnancy and risk of gestational diabetes mellitus. Diabet Med. 2012;29(7):e25-32. (PubMed)
- Lu M, Xu Y, Lv L, Zhang M. Association between vitamin D status and the risk of gestational diabetes mellitus: a meta-analysis. Arch Gynecol Obstet. 2016;293(5):959-966. (PubMed)
- Poel YH, Hummel P, Lips P, Stam F, van der Ploeg T, Simsek S. Vitamin D and gestational diabetes: a systematic review and meta-analysis. Eur J Intern Med. 2012;23(5):465-469. (PubMed)
- Wei SQ, Qi HP, Luo ZC, Fraser WD. Maternal vitamin D status and adverse pregnancy outcomes: a systematic review and meta-analysis. J Matern Fetal Neonatal Med. 2013;26(9):889-899. (PubMed)
- Zhang MX, Pan GT, Guo JF, Li BY, Qin LQ, Zhang ZL. Vitamin D deficiency increases the risk of gestational diabetes mellitus: a meta-analysis of observational studies. Nutrients. 2015;7(10):8366-8375. (PubMed)
- Triunfo S, Lanzone A, Lindqvist PG. Low maternal circulating levels of vitamin D as potential determinant in the development of gestational diabetes mellitus. J Endocrinol Invest. 2017; May 29. doi: 10.1007/s40618-017-0696-9. [Epub ahead of print]. (PubMed)
- Asemi Z, Hashemi T, Karamali M, Samimi M, Esmaillzadeh A. Effects of vitamin D supplementation on glucose metabolism, lipid concentrations, inflammation, and oxidative stress in gestational diabetes: a double-blind randomized controlled clinical trial. Am J Clin Nutr. 2013;98(6):1425-1432. (PubMed)
- Jelsma JG, van Poppel MN, Galjaard S, et al. DALI: Vitamin D and lifestyle intervention for gestational diabetes mellitus (GDM) prevention: an European multicentre, randomised trial - study protocol. BMC Pregnancy Childbirth. 2013;13:142. (PubMed)
- Simmons D, Devlieger R, van Assche A, et al. Effect of Physical Activity and/or Healthy Eating on GDM Risk: The DALI Lifestyle Study. J Clin Endocrinol Metab. 2017;102(3):903-913. (PubMed)
- Galthen-Sorensen M, Andersen LB, Sperling L, Christesen HT. Maternal 25-hydroxyvitamin D level and fetal bone growth assessed by ultrasound: a systematic review. Ultrasound Obstet Gynecol. 2014;44(6):633-640. (PubMed)
- Shor DB, Barzel J, Tauber E, Amital H. The effects of maternal vitamin D on neonatal growth parameters. Eur J Pediatr. 2015;174(9):1169-1174. (PubMed)
- Cooper C, Harvey NC, Bishop NJ, et al. Maternal gestational vitamin D supplementation and offspring bone health (MAVIDOS): a multicentre, double-blind, randomised placebo-controlled trial. Lancet Diabetes Endocrinol. 2016;4(5):393-402. (PubMed)
- Handel MN, Frederiksen P, Osmond C, Cooper C, Abrahamsen B, Heitmann BL. Prenatal exposure to vitamin D from fortified margarine and risk of fractures in late childhood: period and cohort results from 222 000 subjects in the D-tect observational study. Br J Nutr. 2017;117(6):872-881. (PubMed)
- Rodda CP, Benson JE, Vincent AJ, Whitehead CL, Polykov A, Vollenhoven B. Maternal vitamin D supplementation during pregnancy prevents vitamin D deficiency in the newborn: an open-label randomized controlled trial. Clin Endocrinol (Oxf). 2015;83(3):363-368. (PubMed)
- Handel MN, Frederiksen P, Cohen A, Cooper C, Heitmann BL, Abrahamsen B. Neonatal vitamin D status from archived dried blood spots and future risk of fractures in childhood: results from the D-tect study, a population-based case-cohort study. Am J Clin Nutr. 2017;106(1):155-161. (PubMed)
- Bountouvi E, Douros K, Papadopoulou A. Can getting enough vitamin D during pregnancy reduce the risk of getting asthma in childhood? Front Pediatr. 2017;5:87. (PubMed)
- Goldring ST, Griffiths CJ, Martineau AR, et al. Prenatal vitamin D supplementation and child respiratory health: a randomised controlled trial. PLoS One. 2013;8(6):e66627. (PubMed)
- Chawes BL, Bonnelykke K, Stokholm J, et al. Effect of vitamin D3 supplementation during pregnancy on rsk of persistent wheeze in the offspring: a randomized clinical trial. JAMA. 2016;315(4):353-361. (PubMed)
- Litonjua AA, Carey VJ, Laranjo N, et al. Effect of prenatal supplementation with vitamin D on asthma or eecurrent wheezing in offspring by age 3 years: the VDAART randomized clinical trial. JAMA. 2016;315(4):362-370. (PubMed)
- Vahdaninia M, Mackenzie H, Helps S, Dean T. Prenatal intake of vitamins and allergic outcomes in the offspring: a systematic review and meta-analysis. J Allergy Clin Immunol Pract. 2017;5(3):771-778.e775. (PubMed)
- Weisse K, Winkler S, Hirche F, et al. Maternal and newborn vitamin D status and its impact on food allergy development in the German LINA cohort study. Allergy. 2013;68(2):220-228. (PubMed)
- Miettinen ME, Smart MC, Kinnunen L, et al. Maternal VDR variants rather than 25-hydroxyvitamin D concentration during early pregnancy are associated with type 1 diabetes in the offspring. Diabetologia. 2015;58(10):2278-2283. (PubMed)
- Sorensen IM, Joner G, Jenum PA, et al. Vitamin D-binding protein and 25-hydroxyvitamin D during pregnancy in mothers whose children later developed type 1 diabetes. Diabetes Metab Res Rev. 2016;32(8):883-890. (PubMed)
- Makela MJ, Puhakka T, Ruuskanen O, et al. Viruses and bacteria in the etiology of the common cold. J Clin Microbiol. 1998;36(2):539-542. (PubMed)
- Ginde AA, Mansbach JM, Camargo CA, Jr. Association between serum 25-hydroxyvitamin D level and upper respiratory tract infection in the Third National Health and Nutrition Examination Survey. Arch Intern Med. 2009;169(4):384-390. (PubMed)
- Murdoch DR, Slow S, Chambers ST, et al. Effect of vitamin D3 supplementation on upper respiratory tract infections in healthy adults: the VIDARIS randomized controlled trial. JAMA. 2012;308(13):1333-1339. (PubMed)
- Rees JR, Hendricks K, Barry EL, et al. Vitamin D3 supplementation and upper respiratory tract infections in a randomized, controlled trial. Clin Infect Dis. 2013;57(10):1384-1392. (PubMed)
- Tran B, Armstrong BK, Ebeling PR, et al. Effect of vitamin D supplementation on antibiotic use: a randomized controlled trial. Am J Clin Nutr. 2014;99(1):156-161. (PubMed)
- Grant CC, Kaur S, Waymouth E, et al. Reduced primary care respiratory infection visits following pregnancy and infancy vitamin D supplementation: a randomised controlled trial. Acta Paediatr. 2015;104(4):396-404. (PubMed)
- Martineau AR, Jolliffe DA, Hooper RL, et al. Vitamin D supplementation to prevent acute respiratory tract infections: systematic review and meta-analysis of individual participant data. BMJ. 2017;356:i6583. (PubMed)
- Scragg R, Waayer D, Stewart AW, et al. The Vitamin D Assessment (ViDA) study: design of a randomized controlled trial of vitamin D supplementation for the prevention of cardiovascular disease, acute respiratory infection, falls and non-vertebral fractures. J Steroid Biochem Mol Biol. 2016;164:318-325. (PubMed)
- Manson JE, Bassuk SS, Buring JE, Group VR. Principal results of the VITamin D and OmegA-3 TriaL (VITAL) and updated meta-analyses of relevant vitamin D trials. J Steroid Biochem Mol Biol.2020;198:105522. (PubMed)
- Gold DR, Litonjua AA, Carey VJ, et al. Lung VITAL: Rationale, design, and baseline characteristics of an ancillary study evaluating the effects of vitamin D and/or marine omega-3 fatty acid supplements on acute exacerbations of chronic respiratory disease, asthma control, pneumonia and lung function in adults. Contemp Clin Trials. 2016;47:185-195. (PubMed)
- Aglipay M, Birken CS, Parkin PC, et al. Effect of high-dose vs standard-dose wintertime vitamin D supplementation on viral upper respiratory tract infections in young healthy children. JAMA.2017;318(3):245-254. (PubMed)
- Hueniken K, Aglipay M, Birken CS, et al. Effect of high-dose vitamin D supplementation on upper respiratory tract infection symptom severity in healthy children. Pediatr Infect Dis J.2019;38(6):564-568. (PubMed)
- Loeb M, Dang AD, Thiem VD, et al. Effect of Vitamin D supplementation to reduce respiratory infections in children and adolescents in Vietnam: A randomized controlled trial. Influenza Other Respir Viruses.2019;13(2):176-183. (PubMed)
- Kronbichler A, Kresse D, Yoon S, Lee KH, Effenberger M, Shin JI. Asymptomatic patients as a source of COVID-19 infections: A systematic review and meta-analysis. Int J Infect Dis.2020;98:180-186. (PubMed)
- Wiersinga WJ, Rhodes A, Cheng AC, Peacock SJ, Prescott HC. Pathophysiology, transmission, diagnosis, and treatment of coronavirus disease 2019 (COVID-19): a review. JAMA.2020;324(8):782-793. (PubMed)
- Ferrari D, Locatelli M. No significant association between vitamin D and COVID-19. A retrospective study from a northern Italian hospital. Int J Vitam Nutr Res.2020:1-4. (PubMed)
- Hastie CE, Mackay DF, Ho F, et al. Vitamin D concentrations and COVID-19 infection in UK Biobank. Diabetes Metab Syndr.2020;14(4):561-565. (PubMed)
- Ma H, Zhou T, Heianza Y, Qi L. Habitual use of vitamin D supplements and risk of coronavirus disease 2019 (COVID-19) infection: a prospective study in UK Biobank. Am J Clin Nutr.2021. [Epub ahead of print] (PubMed)
- Kaufman HW, Niles JK, Kroll MH, Bi C, Holick MF. SARS-CoV-2 positivity rates associated with circulating 25-hydroxyvitamin D levels. PLoS One.2020;15(9):e0239252. (PubMed)
- Merzon E, Tworowski D, Gorohovski A, et al. Low plasma 25(OH) vitamin D level is associated with increased risk of COVID-19 infection: an Israeli population-based study. FEBS J.2020;287(17):3693-3702. (PubMed)
- Meltzer DO, Best TJ, Zhang H, Vokes T, Arora V, Solway J. Association of vitamin D status and other clinical characteristics with COVID-19 test results. JAMA Netw Open.2020;3(9):e2019722. (PubMed)
- D'Avolio A, Avataneo V, Manca A, et al. 25-Hydroxyvitamin D concentrations are lower in patients with positive PCR for SARS-CoV-2. Nutrients.2020;12(5):1359. (PubMed)
- Ye K, Tang F, Liao X, et al. Does serum vitamin D level affect COVID-19 infection and its severity?-a case-control study. J Am Coll Nutr.2020:1-8. (PubMed)
- Hernandez JL, Nan D, Fernandez-Ayala M, et al. Vitamin D status in hospitalized patients with SARS-CoV-2 infection. J Clin Endocrinol Metab.2020. [Epub ahead of print] (PubMed)
- Im JH, Je YS, Baek J, Chung MH, Kwon HY, Lee JS. Nutritional status of patients with COVID-19. Int J Infect Dis.2020;100:390-393. (PubMed)
- Abdollahi A, Kamali Sarvestani H, Rafat Z, et al. The association between the level of serum 25(OH) vitamin D, obesity, and underlying diseases with the risk of developing COVID-19 infection: A case-control study of hospitalized patients in Tehran, Iran. J Med Virol.2020. [Epub ahead of print] (PubMed)
- Liu N, Sun J, Wang X, Zhang T, Zhao M, Li H. Low vitamin D status is associated with coronavirus disease 2019 outcomes: a systematic review and meta-analysis. Int J Infect Dis.2021;104:58-64. (PubMed)
- Panagiotou G, Tee SA, Ihsan Y, et al. Low serum 25-hydroxyvitamin D (25[OH]D) levels in patients hospitalized with COVID-19 are associated with greater disease severity. Clin Endocrinol (Oxf).2020;93(4):508-511. (PubMed)
- De Smet D, De Smet K, Herroelen P, Gryspeerdt S, Martens GA. Serum 25(OH)D level on hospital admission associated with COVID-19 stage and mortality. Am J Clin Pathol.2020. [Epub ahead of print] (PubMed)
- Baktash V, Hosack T, Patel N, et al. Vitamin D status and outcomes for hospitalised older patients with COVID-19. Postgrad Med J.2020. [Epub ahead of print] (PubMed)
- Radujkovic A, Hippchen T, Tiwari-Heckler S, Dreher S, Boxberger M, Merle U. Vitamin D deficiency and outcome of COVID-19 patients. Nutrients.2020;12(9): 2757. (PubMed)
- Carpagnano GE, Di Lecce V, Quaranta VN, et al. Vitamin D deficiency as a predictor of poor prognosis in patients with acute respiratory failure due to COVID-19. J Endocrinol Invest.2020. [Epub ahead of print] (PubMed)
- Hastie CE, Pell JP, Sattar N. Vitamin D and COVID-19 infection and mortality in UK Biobank. Eur J Nutr.2020;60(1):545-548. (PubMed)
- Centers for Disease Control and Prevention. Assessing Risk Factors for Severe COVID-19 Illness. Available at: https://www.cdc.gov/coronavirus/2019-ncov/covid-data/investigations-discovery/assessing-risk-factors.html. Accessed 1/22/21.
- Annweiler G, Corvaisier M, Gautier J, et al. Vitamin D supplementation associated to better survival in hospitalized frail elderly COVID-19 patients: the GERIA-COVID quasi-experimental study. Nutrients.2020;12(11):3377. (PubMed)
- Annweiler C, Hanotte B, Grandin de l'Eprevier C, Sabatier JM, Lafaie L, Celarier T. Vitamin D and survival in COVID-19 patients: A quasi-experimental study. J Steroid Biochem Mol Biol.2020;204:105771. (PubMed)
- Mesquita Kde C, Igreja AC, Costa IM. Atopic dermatitis and vitamin D: facts and controversies. An Bras Dermatol.2013;88(6):945-953. (PubMed)
- Lee SA, Hong S, Kim HJ, Lee SH, Yum HY. Correlation between serum vitamin D level and the severity of atopic dermatitis associated with food sensitization. Allergy Asthma Immunol Res. 2013;5(4):207-210. (PubMed)
- Sudlow C, Gallacher J, Allen N, et al. UK biobank: an open access resource for identifying the causes of a wide range of complex diseases of middle and old age. PLoS Med. 2015;12(3):e1001779. (PubMed)
- Moffatt MF, Gut IG, Demenais F, et al. A large-scale, consortium-based genomewide association study of asthma. N Engl J Med. 2010;363(13):1211-1221. (PubMed)
- Paternoster L, Zhurov AI, Toma AM, et al. Genome-wide association study of three-dimensional facial morphology identifies a variant in PAX3 associated with nasion position. Am J Hum Genet. 2012;90(3):478-485. (PubMed)
- Manousaki D, Paternoster L, Standl M, et al. Vitamin D levels and susceptibility to asthma, elevated immunoglobulin E levels, and atopic dermatitis: A Mendelian randomization study. PLoS Med. 2017;14(5):e1002294. (PubMed)
- Javanbakht MH, Keshavarz SA, Djalali M, et al. Randomized controlled trial using vitamins E and D supplementation in atopic dermatitis. J Dermatolog Treat. 2011;22(3):144-150. (PubMed)
- Amestejani M, Salehi BS, Vasigh M, et al. Vitamin D supplementation in the treatment of atopic dermatitis: a clinical trial study. J Drugs Dermatol. 2012;11(3):327-330. (PubMed)
- Camargo CA, Jr., Ganmaa D, Sidbury R, Erdenedelger K, Radnaakhand N, Khandsuren B. Randomized trial of vitamin D supplementation for winter-related atopic dermatitis in children. J Allergy Clin Immunol. 2014;134(4):831-835.e831. (PubMed)
- Kim G, Bae JH. Vitamin D and atopic dermatitis: A systematic review and meta-analysis. Nutrition. 2016;32(9):913-920. (PubMed)
- Wat H, Dytoc M. Off-label uses of topical vitamin d in dermatology: a systematic review. J Cutan Med Surg. 2014;18(2):91-108. (PubMed)
- Xue LN, Xu KQ, Zhang W, Wang Q, Wu J, Wang XY. Associations between vitamin D receptor polymorphisms and susceptibility to ulcerative colitis and Crohn's disease: a meta-analysis. Inflamm Bowel Dis. 2013;19(1):54-60. (PubMed)
- Ananthakrishnan AN, Khalili H, Higuchi LM, et al. Higher predicted vitamin D status is associated with reduced risk of Crohn's disease. Gastroenterology. 2012;142(3):482-489. (PubMed)
- Sadeghian M, Saneei P, Siassi F, Esmaillzadeh A. Vitamin D status in relation to Crohn's disease: meta-analysis of observational studies. Nutrition. 2016;32(5):505-514. (PubMed)
- Jorgensen SP, Agnholt J, Glerup H, et al. Clinical trial: vitamin D3 treatment in Crohn's disease - a randomized double-blind placebo-controlled study. Aliment Pharmacol Ther. 2010;32(3):377-383. (PubMed)
- Yang L, Weaver V, Smith JP, Bingaman S, Hartman TJ, Cantorna MT. Therapeutic effect of vitamin d supplementation in a pilot study of Crohn's patients. Clin Transl Gastroenterol. 2013;4:e33. (PubMed)
- Raftery T, Martineau AR, Greiller CL, et al. Effects of vitamin D supplementation on intestinal permeability, cathelicidin and disease markers in Crohn's disease: Results from a randomised double-blind placebo-controlled study. United European Gastroenterol J. 2015;3(3):294-302. (PubMed)
- Anderson JL, May HT, Horne BD, et al. Relation of vitamin D deficiency to cardiovascular risk factors, disease status, and incident events in a general healthcare population. Am J Cardiol. 2010;106(7):963-968. (PubMed)
- Al Mheid I, Patel R, Murrow J, et al. Vitamin D status is associated with arterial stiffness and vascular dysfunction in healthy humans. J Am Coll Cardiol. 2011;58(2):186-192. (PubMed)
- Krause R, Buhring M, Hopfenmuller W, Holick MF, Sharma AM. Ultraviolet B and blood pressure. Lancet. 1998;352(9129):709-710. (PubMed)
- Kunutsor SK, Burgess S, Munroe PB, Khan H. Vitamin D and high blood pressure: causal association or epiphenomenon? Eur J Epidemiol. 2014;29(1):1-14. (PubMed)
- Pilz S, Gaksch M, Kienreich K, et al. Effects of vitamin D on blood pressure and cardiovascular risk factors: a randomized controlled trial. Hypertension. 2015;65(6):1195-1201. (PubMed)
- Arora P, Song Y, Dusek J, et al. Vitamin D therapy in individuals with prehypertension or hypertension: the DAYLIGHT trial. Circulation. 2015;131(3):254-262. (PubMed)
- Rostand SG. Ultraviolet light may contribute to geographic and racial blood pressure differences. Hypertension. 1997;30(2 Pt 1):150-156. (PubMed)
- Forman JP, Scott JB, Ng K, et al. Effect of vitamin D supplementation on blood pressure in blacks. Hypertension. 2013;61(4):779-785. (PubMed)
- Witham MD, Price RJ, Struthers AD, et al. Cholecalciferol treatment to reduce blood pressure in older patients with isolated systolic hypertension: the VitDISH randomized controlled trial. JAMA Intern Med. 2013;173(18):1672-1679. (PubMed)
- Oz F, Cizgici AY, Oflaz H, et al. Impact of vitamin D insufficiency on the epicardial coronary flow velocity and endothelial function. Coron Artery Dis. 2013;24(5):392-397. (PubMed)
- Liu LC, Voors AA, van Veldhuisen DJ, et al. Vitamin D status and outcomes in heart failure patients. Eur J Heart Fail. 2011;13(6):619-625. (PubMed)
- Shedeed SA. Vitamin D supplementation in infants with chronic congestive heart failure. Pediatr Cardiol. 2012;33(5):713-719. (PubMed)
- Boxer RS, Kenny AM, Schmotzer BJ, Vest M, Fiutem JJ, Pina IL. A randomized controlled trial of high dose vitamin D3 in patients with heart failure. JACC Heart Fail. 2013;1(1):84-90. (PubMed)
- Jiang WL, Gu HB, Zhang YF, Xia QQ, Qi J, Chen JC. Vitamin D supplementation in the treatment of chronic heart failure: a meta-analysis of randomized controlled trials. Clin Cardiol. 2016;39(1):56-61. (PubMed)
- Zittermann A, Ernst JB, Prokop S, et al. Effect of vitamin D on all-cause mortality in heart failure (EVITA): a 3-year randomized clinical trial with 4000 IU vitamin D daily. Eur Heart J. 2017;38(29):2279-2286. (PubMed)
- Norman AW, Henry HH. Vitamin D. In: Bowman BA, Russell RM, eds. Present Knowledge in Nutrition. 9th ed. Washington, D.C.: ILSI Press; 2006:198-210.
- Holick MF. Vitamin D: the underappreciated D-lightful hormone that is important for skeletal and cellular health. Curr Opin Endocrinol Diabetes. 2002;9:87-98.
- Terushkin V, Bender A, Psaty EL, Engelsen O, Wang SQ, Halpern AC. Estimated equivalency of vitamin D production from natural sun exposure versus oral vitamin D supplementation across seasons at two US latitudes. J Am Acad Dermatol. 2010;62(6):929 e921-929. (PubMed)
- Food and Nutrition Board, Institute of Medicine. Vitamin D. Dietary referencia Intakes for Calcium, Phosphorus, Magnesium, Vitamin D, and Fluoride. Washington, D.C.: National Academies Press; 1999:250-287. (National Academy Press)
- Ovesen L, Brot C, Jakobsen J. Food contents and biological activity of 25-hydroxyvitamin D: a vitamin D metabolite to be reckoned with? Ann Nutr Metab.2003;47(3-4):107-113. (PubMed)
- Jakobsen J, Christensen T. Natural vitamin D in food: to what degree does 25-hydroxyvitaminn D contribute to the vitamin D activity in food? JMBR Plus.2020: doi: 10.1002/jbm1004.10453.
- Tripkovic L, Lambert H, Hart K, et al. Comparison of vitamin D2 and vitamin D3 supplementation in raising serum 25-hydroxyvitamin D status: a systematic review and meta-analysis. Am J Clin Nutr. 2012;95(6):1357-1364. (PubMed)
- Logan VF, Gray AR, Peddie MC, Harper MJ, Houghton LA. Long-term vitamin D3 supplementation is more effective than vitamin D2 in maintaining serum 25-hydroxyvitamin D status over the winter months. Br J Nutr. 2013;109(6):1082-1088. (PubMed)
- Barger-Lux MJ, Heaney RP, Dowell S, Chen TC, Holick MF. Vitamin D and its major metabolites: serum levels after graded oral dosing in healthy men. Osteoporos Int.1998;8(3):222-230. (PubMed)
- Cashman KD, Seamans KM, Lucey AJ, et al. Relative effectiveness of oral 25-hydroxyvitamin D3 and vitamin D3 in raising wintertime serum 25-hydroxyvitamin D in older adults. Am J Clin Nutr.2012;95(6):1350-1356. (PubMed)
- Bischoff-Ferrari HA, Dawson-Hughes B, Stocklin E, et al. Oral supplementation with 25(OH)D3 versus vitamin D3: effects on 25(OH)D levels, lower extremity function, blood pressure, and markers of innate immunity. J Bone Miner Res.2012;27(1):160-169. (PubMed)
- Jetter A, Egli A, Dawson-Hughes B, et al. Pharmacokinetics of oral vitamin D(3) and calcifediol. Bone.2014;59:14-19. (PubMed)
- Navarro-Valverde C, Sosa-Henriquez M, Alhambra-Exposito MR, Quesada-Gomez JM. Vitamin D3 and calcidiol are not equipotent. J Steroid Biochem Mol Biol.2016;164:205-208. (PubMed)
- Shieh A, Ma C, Chun RF, et al. Effects of cholecalciferol vs calcifediol on total and free 25-hydroxyvitamin D and parathyroid hormone. J Clin Endocrinol Metab.2017;102(4):1133-1140. (PubMed)
- Vaes AMM, Tieland M, de Regt MF, Wittwer J, van Loon LJC, de Groot L. Dose-response effects of supplementation with calcifediol on serum 25-hydroxyvitamin D status and its metabolites: A randomized controlled trial in older adults. Clin Nutr.2018;37(3):808-814. (PubMed)
- Graeff-Armas LA, Bendik I, Kunz I, Schoop R, Hull S, Beck M. Supplemental 25-hydroxycholecalciferol is more effective than cholecalciferol in raising serum 25-hydroxyvitamin D concentrations in older adults. J Nutr 2020;150(1):73-81. (PubMed)
- Quesada-Gomez JM, Bouillon R. Is calcifediol better than cholecalciferol for vitamin D supplementation? Osteoporos Int.2018;29(8):1697-1711. (PubMed)
- Holick MF. Vitamin D deficiency. N Engl J Med. 2007;357(3):266-281. (PubMed)
- Vieth R. Vitamin D supplementation, 25-hydroxyvitamin D concentrations, and safety. Am J Clin Nutr. 1999;69(5):842-856. (PubMed)
- Heaney RP, Davies KM, Chen TC, Holick MF, Barger-Lux MJ. Human serum 25-hydroxycholecalciferol response to extended oral dosing with cholecalciferol. Am J Clin Nutr. 2003;77(1):204-210. (PubMed)
- Vieth R, Chan PC, MacFarlane GD. Efficacy and safety of vitamin D3 intake exceeding the lowest observed adverse effect level. Am J Clin Nutr. 2001;73(2):288-294. (PubMed)
- Knodel LC, Talbert RL. Adverse effects of hypolipidaemic drugs. Med Toxicol. 1987;2(1):10-32. (PubMed)
- McDuffie JR, Calis KA, Booth SL, Uwaifo GI, Yanovski JA. Effects of orlistat on fat-soluble vitamins in obese adolescents. Pharmacotherapy. 2002;22(7):814-822. (PubMed)
- Natural Medicines. Vitamin D. Professional handout/Drug interactions. Available at: https://naturalmedicines.therapeuticresearch.com. Accessed 6/11/17.
- Panday K, Gona A, Humphrey MB. Medication-induced osteoporosis: screening and treatment strategies. Ther Adv Musculoskelet Dis. 2014;6(5):185-202. (PubMed)
- Glass AR, Eil C. Ketoconazole-induced reduction in serum 1,25-dihydroxyvitamin D. J Clin Endocrinol Metab. 1986;63(3):766-769. (PubMed)
Exclusión de Responsabilidades
El Centro de Informaciones sobre Micronutrientes del Instituto Linus Pauling entrega información científica relacionado con aspectos de importancia en salud pública de factores dietéticos, suplementos, comestibles y bebidas para el público en general. Esta información se entrega con el entendimiento que ni el autor ni la imprenta están entregando consejos de naturaleza médica, psicológica o nutricional. La información no debe ser usada para reemplazar la consulta con profesionales competentes en el área de cuidado de salud o de nutrición.
La información entregada con relación a factores y suplementos dietéticos, comestibles, y bebestibles, contenida en este sitio web, no cubre todos los usos, acciones, precauciones, efectos secundarios, e interacciones posibles. No debe ser considerado como consejo nutricional o médico para resolver problemas individuales. La responsabilidad legal por las acciones individuales u omisiones que se derivan del uso de este sitio está expresamente excluida.
No se puede copiar, modificar, distribuir, transmitir, realizar, publicar o vender ninguno de los materiales sujetos a derechos de autoría de este sitio web. Puede enlazar a este sitio web, pero debe incluir la siguiente declaración:
"Este enlace lleva a un sitio web proporcionado por el Instituto Linus Pauling en la Universidad Estatal de Oregon. [Su nombre] no está afiliado ni respaldado por el Instituto Linus Pauling o la Universidad Estatal de Oregon."