Resumen
- El ácido pantoténico — también conocido como vitamina B5 — es una vitamina hidrosoluble que a su vez es un precursor en la síntesis de la coenzima A. La coenzima A es esencial para muchas reacciones bioquímicas que sostienen la vida. También, el grupo funcional fosfopanteteinilo de la coenzima A es requerido para la actividad biológica de varias proteínas, incluyendo la proteína portadora de acilo involucrada en la síntesis de ácidos grasos. (Más información)
- El ácido pantoténico es esencial para todas las formas de vida. Se encuentra de forma ubicua en alimentos de origen vegetal y animal, y una deficiencia dietaría es bastante rara. (Más información)
- La Junta de Alimentos y Nutrición del Instituto de Medicina de los EE.UU. estableció una ingesta adecuada (IA) de 5 miligramos (mg)/día para adultos basándose en la ingesta diaria promedio del ácido pantoténico. (Más información)
- Evidencia proveniente de estudios de intervención limitados sugiere que el ácido pantoténico y/o el pantotenol (alcohol análogo) podrían mejorar el proceso de curación de heridas de la piel. Sin embargo, estudios de mayor escala son requeridos. (Más información)
- Se ha demostrado que el tratamiento con altas dosis de pantetina — un derivado del ácido pantoténico — disminuye las concentraciones de colesterol y lípidos del suero. Aunque la terapia con pantetina parece ser bien tolerada, supervisión médica es indispensable. (Más información)
- Alimentos ricos en acido pantoténico incluyen órganos animales (hígado y riñones), pescado, mariscos, productos lácteos, huevos, aguacates, legumbres, champiñones, y camotes. (Más información)
- Poca o ninguna toxicidad ha sido asociada con el ácido pantoténico dietario y suplementario tanto que ningún nivel máximo de ingesta tolerable (NM) ha sido establecido. (Más información)
El ácido pantoténico, también conocido como vitamina B5, es esencial para todas las formas de vida (1). El ácido pantoténico se encuentra a través de todas las ramificaciones de la vida en la forma de coenzima A, una coenzima vital en numerosas reacciones químicas (2).
Función
Síntesis de los cofactores del ácido pantoténico
Coenzima A
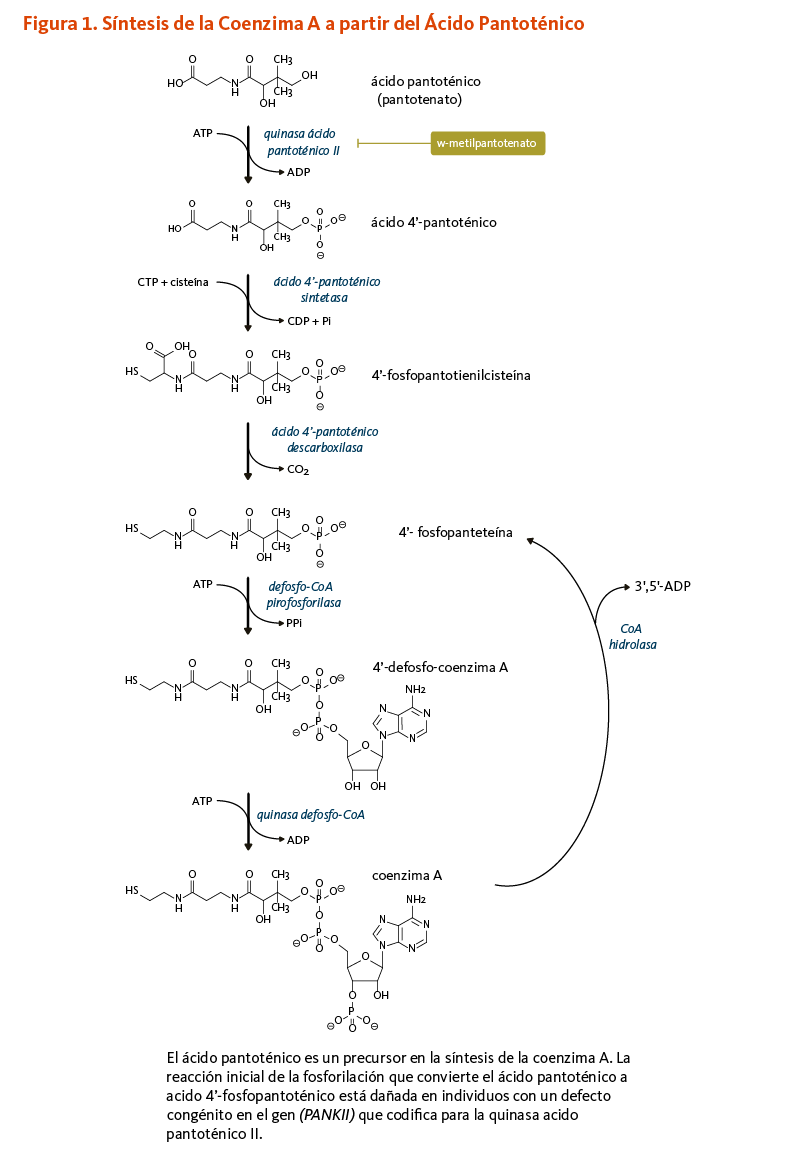
El ácido pantoténico es un precursor en la biosíntesis de la coenzima A (CoA) (Figura 1), una coenzima esencial en una variedad de reacciones bioquímicas que soportan la vida (véase abajo). La quinasa ácido pantoténico II (PANKII) cataliza el paso inicial para la fosforilación del ácido pantoténico a ácido 4’-fosfopantoténico. La coenzima A y sus derivados inhiben la síntesis del ácido 4’-fosfopantoténico, pero la inhibición puede ser revertida por la carnitina, requerida para el transporte de ácidos grasos en la mitocondria (3). Las reacciones subsecuentes en esta ruta biosintetica incluyen la síntesis del intermedio 4'-fosfopanteteína, como también el reciclaje de la coenzima A a 4'-fosfopanteteína (Figura 1).
4’-fosfopanteteína
El grupo funcional 4'-fosfopanteteinilo de la coenzima A puede ser transferido a enzimas en las cuales 4'-fosfopanteteína es un cofactor esencial para sus actividades biológicas (véase 4'-fosfopanteteinilación).
[Figura 1 - Clic para Agrandar]
Función de cofactor y co-sustrato
Coenzima A
La coenzima A reacciona con los grupos acilo, dando lugar a derivados tioéster, como la acetil-CoA, succinil-CoA, malonil-CoA, y 3-hidroxi-3-metilglutaril (HMG)-CoA. La coenzima A y sus derivados de acilo son requeridos para reacciones que generan energía a partir de la degradación de grasas, carbohidratos y proteínas dietarías. Además, la coenzima A en la forma de acetil-CoA y succinil-CoA está involucrada en el ciclo del ácido cítrico, en la síntesis de grasas esenciales, colesterol, hormonas esteroidales, vitamina A y D, el neurotransmisor acetilcolina, y en la ruta de β-oxidación de ácidos grasos. Los derivados de la coenzima A son también requeridos para la síntesis de la hormona melatonina, y para un componente de la hemoglobina llamado hemo. Además, el metabolismo de un cierto número de drogas y toxinas por el hígado requieren de la coenzima A (4).
La coenzima A fue nombrada por su papel en las reacciones de acetilación. La mayoría de las proteínas acetiladas en el cuerpo han sido modificadas por la adición de un grupo acetato que fue donando por el derivado tioéster de la coenzima A, la acetil-CoA. La acetilación de las proteínas altera la carga general de las proteínas, modificando su estructura tridimensional y, alterando potencialmente su función. Por ejemplo, la acetilación es un mecanismo que regula la actividad de hormonas peptídicas, incluyendo aquellas producidas por la glándula pituitaria (5). También, se ha mostrado que la acetilación proteínica, como otras modificaciones postraduccionales, regula la localización subcelular, la función, y el periodo de semidesintegración de muchas moléculas de señalización, factores de transcripción y enzimas. Notablemente, la acetilación de histonas juega un papel en la regulación de la expresión de genes al facilitar la transcripción de (es decir, ARNm síntesis), mientras que las histonas desacetiladas son usualmente asociadas con la compactación de la cromatina y el silenciamiento de genes. Se encontró que la acetilación de histonas resulta en cambios estructurales de la cromatina, que afectan tanto la interacción ADN-proteína como las interacciones proteína-proteína. La diafonía entre marcas de acetilación y otras modificaciones postranscripcionales de las histonas también facilitan el reclutamiento de reguladores transcripcionales para el promotor de los genes que son posteriormente transcritos (revisado en 6).
Finalmente, un cierto número de moléculas de señalización son modificadas por la unión de ácidos grasos de cadena larga donados por la coenzima A. Estas modificaciones son conocidas como acilación de proteínas y tienen papeles centrales en las rutas de señalización celular (4).
4’-fosfopanteteinilación
Complejos multi-enzimáticos específicos, que necesitan llevar a cabo varias reacciones en una manera ordenada, pueden requerir del enlace covalente de un brazo de 4'-fosfopanteteína a un dominio "portador" (o proteína). Este dominio portador mantiene sustratos o intermedios de reacción durante la progresión a través de varias reacciones enzimáticas. En los mamíferos, la transferencia del grupo funcional 4'-fosfopanteteinil proveniente de la coenzima A a un residuo de serina conservado de un dominio portador especifico es catalizado por una única fosfopanteteinil transferasa (7). La 4’-fosfopanteteinilación es necesaria para la conversión de apoenzimas a holoenzimas completamente activas (véase abajo).
Proteína transportadora de grupos acilo
Los lípidos son moléculas grasas esenciales para la función fisiológica normal, y entre otros tipos, incluyen los esfingolípidos (componentes esenciales de la vaina de mielina que mejora la transmisión nerviosa), los fosfolípidos (componentes estructurales importantes de las membranas celulares), y los ácidos grasos. La ácido graso sintasa (FAS) es un complejo multi-enzimático que cataliza la síntesis de ácidos grasos. Dentro del complejo de la FAS, la proteína transportadora de grupos acilo (ACP) requiere de ácido pantoténico en la forma de 4'-fosfopanteteína para su actividad como proteína transportadora (3). Un grupo, como lo es el grupo funcional 4'-fosfopanteteinilo para la ACP, es llamado un grupo prostético, el grupo prostético no está compuesto de aminoácidos y es un cofactor estrechamente unido requerido para la actividad biológica de ciertas proteínas (Figura 2). La acetil-CoA, malonil-CoA, y ACP son todos requeridos para la síntesis de ácidos grasos en el citosol. Durante la síntesis de ácidos grasos, los grupos acilo de la acetil-CoA y malonil-CoA son transferidos al grupo sulfhidrilo (-SH) del grupo funcional 4'-fosfopanteteinilo de la ACP. El grupo prostético es usado como un brazo flexible para transferir la cadena de ácidos grasos creciente a cada uno de los centros enzimáticos del complejo FAS tipo I. En la mitocondria, la 4'-fosfopanteteína también sirve como un grupo prostético para un homólogo de la ACP presente en el complejo FAS tipo II mitocondrial (8).
[Figura 2 - Clic para Agrandar]
10-formiltetrahidrofolato deshidrogenasa
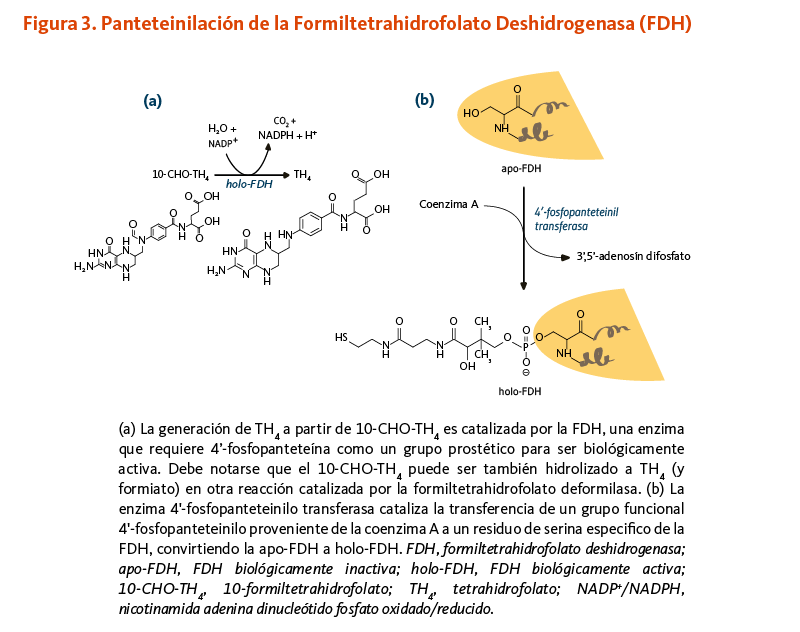
La enzima 10-formiltetrahidrofolato deshidrogenasa (FDH) cataliza la conversión de 10-formiltetrahidrofolato a tetrahidrofolato, un cofactor esencial en el metabolismo de ácidos nucleicos y aminoácidos (Figura 3). Similar a la ACP, la FDH requiere de un grupo prostético 4'-fosfopanteteína para su actividad biológica. El grupo prostético actúa como un brazo oscilante para acoplar las actividades de los dos dominios catalíticos de la FDH (9, 10). Un homólogo de la FDH en la mitocondria también requiere de 4’-fosfopanteteinilación para ser biológicamente activo (11).
[Figura 3 - Clic para Agrandar]
α-Aminoadipato semialdehído sintasa
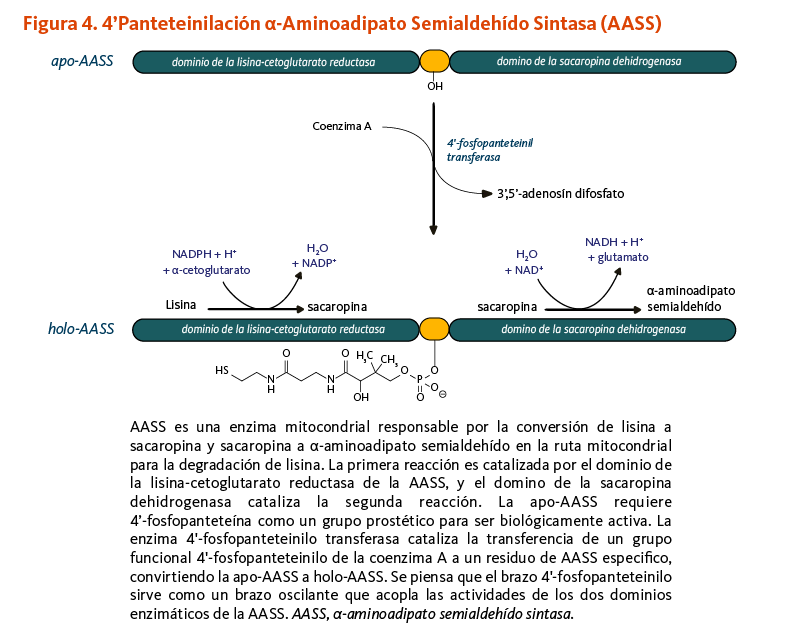
La 4’-fosfopanteteinilación es requerida para la actividad biológica de la apoenzima α-aminoadipato semialdehído sintasa (AASS). AASS cataliza las reacciones iniciales en la ruta mitocondrial para la degradación de lisina — un aminoácido esencial para los humanos. AASS está hecha de dos dominios catalíticos. El dominio de la lisina-cetoglutarato reductasa primero cataliza la conversión de lisina a sacaropina. La sacaropina es convertida adicionalmente a α-aminoadipato semialdehído en una reacción catalizada por el dominio de la sacaropina deshidrogenasa (Figura 4).
[Figura 4 - Clic para Agrandar]
Deficiencia
Una deficiencia de ácido pantoténico de origen natural en seres humanos es muy rara y sólo ha sido observada en casos de desnutrición severa. Los prisioneros de la Segunda Guerra Mundial en las Filipinas, Birmania, y Japón experimentaron entumecimiento y ardor doloroso y hormigueo en los pies; estos síntomas fueron aliviados específicamente con la suplementación con ácido pantoténico (4). La deficiencia de ácido pantoténico en los humanos ha sido inducida experimentalmente co-administrando un inhibidor de la quinasa del ácido pantoténico (w-metilpantotenato; vease Figura 1 arriba) y una dieta deficiente de ácido pantoténico. Los participantes en este experimento se quejaron de dolor de cabeza, fatiga, insomnio, molestias intestinales, y entumecimiento y cosquilleo en manos y pies (12). En otro estudio, los participantes alimentados con solo una dieta libre de ácido pantoténico no desarrollaron signos clínicos de deficiencia, aunque algunos parecían apáticos y se quejaban de fatiga (13).
El homopantotenato de calcio (o homopantotenato) es un antagonista del ácido pantoténico con efectos colinérgicos (es decir, similar a aquellos del neurotransmisor, acetilcolina). Este compuesto es usado en Japón para mejorar la función mental, especialmente en la enfermedad de Alzheimer. Un efecto secundario raro fue el desarrollo de encefalopatía hepática, una condición de funcionamiento anormal del cerebro producto de una falla en la eliminación de toxinas por parte del hígado. La encefalopatía fue revertida por la suplementación con ácido pantoténico, sugiriendo que se debió a una deficiencia de ácido pantoténico inducida por el homopantotenato (14). Debe notarse, que mutaciones en el gen humano PANKII, el cual codifica para la quinasa ácido pantoténico II (véase Figura 1 arriba), resultan en la síntesis alterada de la 4'-fosfopanteteína y de la coenzima A (véase Función). Este desorden, llamado neurodegeneración asociada a pantotenato quinasa, está caracterizado por alteraciones visuales e intelectuales, distonía, anomalías del habla, dificultades del comportamiento, y desordenes de personalidad (15).
Sin embargo, debido a que el ácido pantoténico es ampliamente distribuido en la naturaleza y la deficiencia es extremadamente rara en humanos, la mayoría de la información con respecto a las consecuencias de la deficiencia ha sido recolectada de investigación experimental en animales (revisada en 3). La deficiencia de ácido pantoténico en ratas desarrollo daño a las glándulas adrenales, mientras que monos desarrollaron anemia debido a la síntesis disminuida de grupos hemo, un componente de la hemoglobina. Perros con deficiencia de ácido pantoténico desarrollaron niveles bajos de glucosa, respiración y frecuencia cardiaca aceleradas y convulsiones. Los pollos desarrollaron irritación de la piel, anomalías en el plumaje y daño en nervios espinales asociado con la degeneración de la vaina de mielina. Los ratones con deficiencia de ácido pantoténico mostraron tolerancia disminuida al ejercicio y almacenaje reducido de glucosa (en la forma de glicógeno) en músculos e hígado. Los ratones también desarrollaron irritación de la piel y canosidad del pelaje, que fueron revertidos por la administración de ácido pantoténico.
La diversidad de los síntomas enfatiza las numerosas funciones del ácido pantoténico en sus formas de coenzima.
La IA
Debido a que existe poca información sobre los requerimientos de ácido pantoténico en humanos, la Junta de Nutrición y Alimentos del Instituto de Medicina estableció un nivel de ingesta adecuada (IA) basado en las ingestas dietarías observadas en grupos saludables de la población (Tabla 1) (16).
| Etapa de la Vida | Edad | Machos (mg/día) | Hembras (mg/día) |
|---|---|---|---|
| Infantes | 0-6 meses | 1.7 | 1.7 |
| Infantes | 7-12 meses | 1.8 | 1.8 |
| Niños | 1-3 años | 2 | 2 |
| Niños | 4-8 años | 3 | 3 |
| Niños | 9-13 años | 4 | 4 |
| Adolescentes | 14-18 años | 5 | 5 |
| Adultos | 19 años y más | 5 | 5 |
| Embarazo | todas las edades | - | 6 |
| Período de lactancia | todas las edades | - | 7 |
Tratamiento de Enfermedades
Cicatrización de heridas
Se encontró que la adición de D-pantotenato de calcio y/o pantotenol (Figura 5) al medio de cultivo de fibroblastos cutáneos con una herida artificial aumentó la proliferación y migración celular, acelerando así el proceso de cicatrización in vitro (17, 18). De la misma manera, la deficiencia in vitro de ácido pantoténico indujo la expresión de marcadores de diferenciación en la proliferación de fibroblastos cutáneos e inhibió la proliferación en queratinocitos humanos (19). La aplicación de ungüentos que contienen calcio D-pantotenato o pantotenol — también conocido como D-pantenol o dexpantenol — sobre la piel ha mostrado que acelera el cierre de las heridas de la piel y aumentan la fuerza del tejido cicatricial en animales (3).
Los efectos del dexpantenol en la cicatrización de heridas no están claros. En un estudio controlado con placebo que incluyo 12 voluntarios sanos, la aplicación de un ungüento que contenía dexpantenol (cada 12 horas por 1 a 6 días) en un modelo de cicatrización de herida cutánea fue asociada con una expresión mejorada de los marcadores de proliferación, inflamación, y reparación de tejidos (20). Sin embargo, el estudio fallo en reportar si estos cambios en respuesta al dexpantenol tópico mejoro el proceso de reparación de la herida en comparación al placebo (20). Algunos estudios no han mostrado efectos. Ensayos controlados aleatorios tempranos en pacientes sometidos a cirugía de remoción de tatuajes encontraron que la suplementación diaria con 1 gramo o 3 gramos de vitamina C y 200 mg o 900 mg de ácido pantoténico por 21 días no mejoraron significantemente el proceso de cicatrización (21, 22). A pesar de todo, en un reciente estudio aleatorio, doble ciego, controlado con placebo, el uso de pastillas de dexpantenol (300 mg/día por hasta 14 días post-cirugía) se encontró que acelero la cicatrización de la mucosa después de una amigdalectomía en niños (23).
Colesterol alto
Estudios tempranos sugieren que dosis farmacológicas de pantetina, un derivado del ácido pantoténico, podrían tener un efecto hipocolesterolemiante (24, 25). La pantetina está hecha por dos moléculas de panteteína unidas por un enlace disulfuro (un enlace químico entre dos átomos de azufre) (Figura 5). La pantetina está estructuralmente relacionada a la coenzima A y se encuentra en el grupo prostético que es requerido para la función biológica de la proteína transportadora de acilo, formiltetrahidrofolato dehidrogenasa, y de la α-aminoadipato semialdehído sintasa (véase Función). En un estudio aleatorio, doble ciego, controlado con placebo de 16 semanas, la suplementación diaria con pantetina (600 mg/día por 8 semanas, seguido por 900 mg/día por otras 8 semanas) significantemente mejoró el perfil de los parámetros lípidos en 120 individuos en bajo a moderado riego de enfermedades cardiovasculares (ECV). Después de ajustarse al valor basal, se encontró que la pantetina era significantemente más efectiva que el placebo en la disminución de las concentraciones de colesterol de lipoproteínas de baja densidad (LDL-C) y apolipoproteína B (apoB), como también en la reducción de la proporción de triglicéridos a colesterol de lipoproteínas de alta densidad (TG:HDL-C) (26). Aunque parece ser bien tolerada y potencialmente beneficial en el mejoramiento del metabolismo del colesterol, la pantetina no es una vitamina, y la decisión de usar dosis farmacológicas de pantetina para tratar el colesterol sanguíneo elevado o los triglicéridos deber ser hecha solo en colaboración con proveedores de la salud cualificados que proveen seguimiento adecuado.
[Figura 5 - Clic para Agrandar]
Encanecimiento del cabello
Ratones deficientes de ácido pantoténico desarrollan irritación cutánea y encanecimiento del pelaje, que es revertido por la administración de ácido pantoténico. No existe evidencia en humanos de que tomando suplementos de ácido pantoténico o usando champú que contengan ácido pantoténico pueda prevenir o restaurar el color del cabello.
Fuentes
Fuentes alimenticias
El ácido pantoténico está disponible en una variedad de alimentos, usualmente como un componente de la coenzima A (CoA) y 4’-fosfopanteteína (véase Figura 1 arriba). Tras ingerirse, la coenzima A dietaría y la fosfopanteteína son hidrolizadas a ácido pantoténico antes de la absorción intestinal (3). El hígado y riñones de animales, pescado, mariscos, carne de cerdo, pollo, yema de huevo, leche, yogurt, legumbres, setas, aguacates, brócoli, y camotes son buenas fuentes de ácido pantoténico. Granos enteros son también buenas fuentes de ácido pantoténico, pero el procesamiento y refinamiento de los granos podría resultar en una pérdida del 35 a 75%. Congelado y enlatado de alimentos resulta en pérdidas similares (16). Encuestas nutricionales nacionales de gran envergadura fallaron en estimar la ingesta de ácido pantoténico, principalmente debido a la escasez de información sobre el contenido de ácido pantoténico de los alimentos (16). Estudios más pequeños estimaron ingestas diarias promedio de ácido pantoténico de entre 4 a 7 mg/día en adultos. La Tabla 2 lista algunas fuentes ricas en ácido pantoténico, junto a su contenido en miligramos (mg). Para mayor información sobre el contenido de nutrientes de los alimentos, revise la base de datos de composición de los alimentos del USDA.
| Alimento | Porción | Ácido Pantoténico (mg) |
|---|---|---|
| Hígado de res (cocido, frito) | 3 onzas* | 5.6 |
| Semillas de girasol (tostadas) | 1 onza | 2.0 |
| Pescado, trucha (especies mixtas, cocidas, secado al calor) | 3 onzas* | 1.9 |
| Yogurt (plano, sin grasa) | 8 onzas | 1.6 |
| Langosta (cocida) | 3 onzas | 1.4 |
| Aguacate (crudo, California) | ½ fruto | 1.0 |
| Camote (cocido, con piel) | 1 mediano (½ taza) | 1.0 |
| Leche | 1 taza (8 onzas fluidas) | 0.87 |
| Carne de cerdo (filete de lomo, magra, cocida, rostizada) | 3 onzas* | 0.86 |
| Pollo (carne blanca, cocido, rostizado) | 3 onzas* | 0.83 |
| Huevos (cocidos, hervidos) | 1 grande | 0.70 |
| Queso, feta | ½ taza (desmoronado) | 0.70 |
| Lentejas (semillas maduras, cocidas, hervidas) | ½ taza | 0.63 |
| Guisantes partidos (semillas maduras, cocidas, hervidas) | ½ taza | 0.58 |
| Champiñones (blancos, crudos) | ½ taza (picados) | 0.52 |
| Cacahuates | 1 onza | 0.50 |
| Brócoli (cocido, hervido) | ½ taza (picado) | 0.48 |
| Naranja | 1 entera | 0.30 |
| Pan integral | 1 rebanda | 0.21 |
| *Una porción de tres onzas de carne o pescado es aproximadamente el tamaño de un mazo de cartas. | ||
Bacterias intestinales
Las bacterias que normalmente colonizan el colon (intestino grueso) son capaces de sintetizar ácido pantoténico. Un transportador especializado para la ingesta de biotina y ácido pantoténico fue identificado en células cultivadas derivadas del revestimiento del colon, sugiriendo que los humanos pueden ser capaces de absorber el ácido pantoténico y biotina producidos por las bacterias intestinales (27). Sin embargo, el grado al cual la síntesis bacteriana contribuye a la ingesta de ácido pantoténico en humanos es aún desconocido.
Suplementos
Pantotenol y pantotenato
Los suplementos comúnmente contienen pantotenol (pantenol), un alcohol análogo estable del ácido pantoténico, el cual puede ser rápidamente convertido a ácido pantoténico por los humanos. El calcio y el D-pantotenato de sodio, las sales de calcio y sodio del ácido pantoténico, están también disponibles como suplementos.
Pantetina
La pantetina es utilizada como un agente hipocolesterolemiante en Japón y se encuentra disponible en los EE.UU. como un suplemento dietario (29).
Seguridad
Toxicidad
El ácido pantoténico no es conocido por ser toxico en los humanos. El único efecto adverso observado fue diarrea, resultado de ingestas muy altas de 10 a 20 g/día de D-pantotenato de calcio (30). Sin embargo, existe un reporte de caso de derrame pleuropericárdico eosinofílico con riesgo vital en una mujer de edad avanzada, que tomó una combinación de 10 mg/día de biotina y 300 mg/día de ácido pantoténico por dos meses (31). Debido a la falta de reportes de efectos adversos cuándo se estableció la ingesta diaria recomendada (IDR) de ácido pantoténico en 1998, la Junta de Nutrición y Alimentos del Instituto de Medicina no estableció un nivel máximo de ingesta tolerable (NM) para el ácido pantoténico (16). La pantetina es generalmente bien tolerada en dosis de hasta 1,200 mg/día. Sin embargo, los efectos secundarios gastrointestinales, como las náuseas y agruras, han sido reportadas (29). También, las formulaciones tópicas que contienen hasta un 5% de dexpantenol (D-pantenol) han sido usadas de forma segura por hasta un mes. Sin embargo, algunos casos de irritación de la piel, dermatitis de contacto, y eczema han sido reportados con el uso de ungüentos que contienen dexpantenol (32, 33).
Interacción con nutrientes
Altas dosis de ácido pantoténico tienen el potencial de competir con la biotina por la absorción intestinal y celular por el transportador multivitamínico dependiente de sodio humano (hSMVT) (27, 34).
Interacción con fármacos/drogas
Anticonceptivos orales (pastillas anticonceptivas) que contienen estrógeno y progestina pueden incrementar el requerimiento de ácido pantoténico (30). El uso de pantetina en combinación con medicamentos que disminuyen el colesterol llamados estatinas (inhibidores de HMG-CoA reductasa) o con ácido nicotínico (véase el artículo en Niacina) pueden producir efectos aditivos en los lípidos sanguíneos (29).
Recomendación del LPI
Más datos son necesarios para definir la cantidad de ácido pantoténico dietario necesario para promover la salud optima o prevenir enfermedades crónicas. El Instituto Linus Pauling (LPI) apoya la recomendación dada por la Junta de Nutrición y Alimentos de 5 mg/día de ácido pantoténico para adultos. Una dieta variada debería proveer ácido pantoténico suficiente para la mayor parte de la gente. Siguiendo la recomendación del Instituto Linus Pauling de tomar un suplemento multivitamínico-mineral diariamente, que contenga el 100% del Valor Diario (VD) de ácido pantoténico asegurará una ingesta de al menos 5 mg/día.
Adultos mayores (>50 años)
Actualmente existe poca evidencia de que adultos mayores difieren en su ingesta de o en su requerimiento de ácido pantoténico. La mayoría de suplementos multivitamínicos-minerales proveen de por lo menos 5 mg/día de ácido pantoténico.
Autores y Críticos
Escrito en Mayo de 2004 por:
Jane Higdon, Ph.D.
Instituto Linus Pauling
Universidad Estatal de Oregon
Actualizado en Abril de 2008 por:
Victoria J. Drake, Ph.D.
Instituto Linus Pauling
Universidad Estatal de Oregon
Actualizado en Abril de 2015 por:
Barbara Delage, Ph.D.
Instituto Linus Pauling
Universidad Estatal de Oregon
Revisado en Julio de 2015 por:
Robert B. Rucker, Ph.D.
Distinguido Profesor Emeritus
Departamento de Nutrición y Escuela de Medicina
Universidad de California, Davis
Traducido al Español en 2017 por:
Silvia Vazquez Lima
Instituto Linus Pauling
Universidad Estatal de Oregon
Originalmente traducido al español en 2012 por Guillermo Sandoval y editado por Andrew Quest (Ph.D.) y Lisette Leyton (Ph.D.), todos provenientes de la Universidad de Chile. Estos esfuerzos fueron patrocinados por el projecto Anillo #ACT1111, CONICYT-Chile, programa PIA.
Derechos de autoría 2000-2026 Instituto Linus Pauling
Figure Alternative Text
Figure 1. Coenzyme A synthesis from pantothenic acid
The figure illustrates the biochemical pathway that converts pantothenic acid (pantothenate) into coenzyme A, showing chemical structures of intermediates and the enzymes involved.
At the top of the figure, pantothenic acid is phosphorylated by pantothenic acid kinase 2 (PANK2) using ATP, and releasing ADP, to form 4’-phosphopantothenic acid. This step is impaired in individuals with PANK2 gene mutations.
Next, 4’-phosphopantothenic acid is converted to 4’-phosphopantothenoylcysteine with 4-phosphopantothenic acid synthetase requiring CTP and cysteine and releasing CDP and inorganic phosphate.
Then 4’-phosphopantothenic acid decarboxylase removes CO2 to produce 4’-phosphopantetheine.
Using ATP, dephospho-CoA pyrophosphorylase converts 4’-phosphopantetheine into 4’-dephospho-coenzyme A, releasing pyrophosphate.
Finally, dephospho-CoA kinase phosphorylates 4’-dephospho-coenzyme using ATP, forming coenzyme A and releasing ADP.
The figure also shows the CoA hydrolase reaction, which converts coenzyme A back into 4’-phosphopantetheine, releasing 3’,5’-ADP.
Figure 2. 4’-Pantetheinylation of acyl-carrier protein (ACP)
The figure illustrates the post-translational modification of ACP called 4’-pantetheinylation. This process adds a 4’-phosphopantetheinyl moiety, a prosthetic group required for ACP’s biological activity.
The enzyme 4’-phosphopantetheinyl transferase catalyzes the hydrolysis of coenzyme A to 3’,5’-adenosine diphosphate and 4’-phosphopantetheine, and the transfer of the 4’-phosphopantetheinyl moiety to a serine residue at the active site of ACP, converting biologically inactive apo-ACP into active holo-ACP.
Figure 3. 4’-Pantetheinylation of formyltetrahydrofolate dehydrogenase (FDH)
The figure shows two reactions involving FDH:
Panel A: Holo-FDH (the biologically active FDH) catalyzes the conversion of 10-formyltetrahydrofolate into tetrahydrofolate using water and NADP+, releasing CO2, NADPH, and a proton (H+). FDH requires a prosthetic group, a 4’-phosphopantetheinyl moiety, for biological activity.
Panel B: In a post-translational modification called 4’-pantetheinylation, the enzyme 4’-phosphopantetheinyl transferase catalyzes the hydrolysis of coenzyme A into 3’,5’-adenosine diphosphate and 4’-phosphopantetheine and the transfer of the 4’-phosphopantetheinyl moiety to a specific serine residue of FDH. This converts biologically inactive apo-FDH to active holo-FDH.
Figure 4. 4’-Pantetheinylation of α-aminoadipate semialdehyde synthase (AASS)
The figure illustrates the mitochondrial enzyme AASS that has two domains: the lysine-ketoglutarate reductase domain and the saccharopine dehydrogenase domain. These domains catalyze two reactions once AASS is biologically active (holo-AASS).
The main part of the figure shows 4’-pantetheinylation of AASS, the post-translational modification required for its biological activity. 4’-Phosphopantetheinyl transferase catalyzes the transfer of a 4’-phosphopantetheinyl moiety from coenzyme A to a specific residue of AASS, converting apo-AASS to holo-AASS.
First reaction: Holo-AASS converts lysine to saccharopine, using NADPH, a proton (H+), and α-ketoglutarate, releasing H2O and NADP+.
Second reaction: Holo-AASS converts saccharopine into α-aminoadipate semialdehyde using H2O and NAD+, releasing NADH, H+, and glutamate.
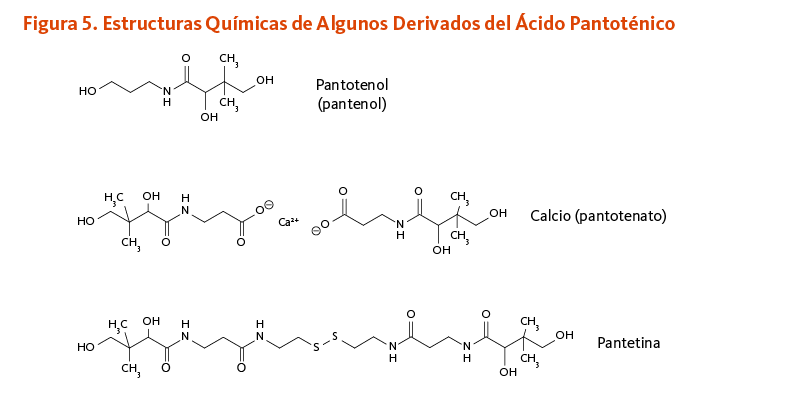
Figure 5. Chemical structures of some pantothenic acid derivatives
The figure shows the chemical structures of the pantothenic acid derivatives: pantothenol (panthenol), calcium pantothenate, and pantethine.
Referencias
- Trumbo PR. Pantothenic acid. In: Ross AC, Caballero B, Cousins RJ, Tucker KL, Ziegler TR, eds. Modern Nutrition in Health and Disease. 11th ed. Baltimore: Lippincott Williams & Wilkins; 2014:351-357.
- Martinez DL, Tsuchiya Y, Gout I. Coenzyme A biosynthetic machinery in mammalian cells. Biochem Soc Trans. 2014;42(4):1112-1117. (PubMed)
- Miller JW, Rucker RB. Pantothenic acid. In: Erdman JWJ, Macdonald IA, Zeisel SH, eds. Present Knowledge in Nutrition. 10th ed. Ames: Wiley-Blackwell; 2012:375-390.
- Bauerly K, Rucker RB. Pantothenic acid. In: Zempleni J, Rucker RB, McCormick DB, Suttie JW, eds. Handbook of vitamins. 4th ed. Boca Raton: CRC Press; 2007:289-314.
- Takahashi A, Mizusawa K. Posttranslational modifications of proopiomelanocortin in vertebrates and their biological significance. Front Endocrinol (Lausanne). 2013;4:143. (PubMed)
- Choudhary C, Weinert BT, Nishida Y, Verdin E, Mann M. The growing landscape of lysine acetylation links metabolism and cell signalling. Nat Rev Mol Cell Biol. 2014;15(8):536-550. (PubMed)
- Beld J, Sonnenschein EC, Vickery CR, Noel JP, Burkart MD. The phosphopantetheinyl transferases: catalysis of a post-translational modification crucial for life. Nat Prod Rep. 2014;31(1):61-108. (PubMed)
- Bunkoczi G, Pasta S, Joshi A, et al. Mechanism and substrate recognition of human holo ACP synthase. Chem Biol. 2007;14(11):1243-1253. (PubMed)
- Donato H, Krupenko NI, Tsybovsky Y, Krupenko SA. 10-formyltetrahydrofolate dehydrogenase requires a 4'-phosphopantetheine prosthetic group for catalysis. J Biol Chem. 2007;282(47):34159-34166. (PubMed)
- Strickland KC, Hoeferlin LA, Oleinik NV, Krupenko NI, Krupenko SA. Acyl carrier protein-specific 4'-phosphopantetheinyl transferase activates 10-formyltetrahydrofolate dehydrogenase. J Biol Chem. 2010;285(3):1627-1633. (PubMed)
- Strickland KC, Krupenko NI, Dubard ME, Hu CJ, Tsybovsky Y, Krupenko SA. Enzymatic properties of ALDH1L2, a mitochondrial 10-formyltetrahydrofolate dehydrogenase. Chem Biol Interact. 2011;191(1-3):129-136. (PubMed)
- Hodges RE, Ohlson MA, Bean WB. Pantothenic acid deficiency in man. J Clin Invest. 1958;37(11):1642-1657. (PubMed)
- Fry PC, Fox HM, Tao HG. Metabolic response to a pantothenic acid deficient diet in humans. J Nutr Sci Vitaminol (Tokyo). 1976;22(4):339-346. (PubMed)
- Bender DA. Optimum nutrition: thiamin, biotin and pantothenate. Proc Nutr Soc. 1999;58(2):427-433. (PubMed)
- Kurian MA, Hayflick SJ. Pantothenate kinase-associated neurodegeneration (PKAN) and PLA2G6-associated neurodegeneration (PLAN): review of two major neurodegeneration with brain iron accumulation (NBIA) phenotypes. Int Rev Neurobiol. 2013;110:49-71. (PubMed)
- Food and Nutrition Board, Institute of Medicine. Pantothenic acid. Dietary Reference Intakes: Thiamin, Riboflavin, Niacin, Vitamin B6, Vitamin B12, Pantothenic Acid, Biotin, and Choline. Washington, D.C.: National Academy Press; 1998:357-373. (National Academy Press)
- Weimann BI, Hermann D. Studies on wound healing: effects of calcium D-pantothenate on the migration, proliferation and protein synthesis of human dermal fibroblasts in culture. Int J Vitam Nutr Res. 1999;69(2):113-119. (PubMed)
- Wiederholt T, Heise R, Skazik C, et al. Calcium pantothenate modulates gene expression in proliferating human dermal fibroblasts. Exp Dermatol. 2009;18(11):969-978. (PubMed)
- Kobayashi D, Kusama M, Onda M, Nakahata N. The effect of pantothenic acid deficiency on keratinocyte proliferation and the synthesis of keratinocyte growth factor and collagen in fibroblasts. J Pharmacol Sci. 2011;115(2):230-234. (PubMed)
- Heise R, Skazik C, Marquardt Y, et al. Dexpanthenol modulates gene expression in skin wound healing in vivo. Skin Pharmacol Physiol. 2012;25(5):241-248. (PubMed)
- Vaxman F, Olender S, Lambert A, et al. Effect of pantothenic acid and ascorbic acid supplementation on human skin wound healing process. A double-blind, prospective and randomized trial. Eur Surg Res. 1995;27(3):158-166. (PubMed)
- Vaxman F, Olender S, Lambert A, Nisand G, Grenier JF. Can the wound healing process be improved by vitamin supplementation? Experimental study on humans. Eur Surg Res. 1996;28(4):306-314. (PubMed)
- Celebi S, Tepe C, Yelken K, Celik O. Efficacy of dexpanthenol for pediatric post-tonsillectomy pain and wound healing. Ann Otol Rhinol Laryngol. 2013;122(7):464-467. (PubMed)
- Coronel F, Tornero F, Torrente J, et al. Treatment of hyperlipemia in diabetic patients on dialysis with a physiological substance. Am J Nephrol. 1991;11(1):32-36. (PubMed)
- Gaddi A, Descovich GC, Noseda G, et al. Controlled evaluation of pantethine, a natural hypolipidemic compound, in patients with different forms of hyperlipoproteinemia. Atherosclerosis. 1984;50(1):73-83. (PubMed)
- Rumberger JA, Napolitano J, Azumano I, Kamiya T, Evans M. Pantethine, a derivative of vitamin B(5) used as a nutritional supplement, favorably alters low-density lipoprotein cholesterol metabolism in low- to moderate-cardiovascular risk North American subjects: a triple-blinded placebo and diet-controlled investigation. Nutr Res. 2011;31(8):608-615. (PubMed)
- Said HM, Ortiz A, McCloud E, Dyer D, Moyer MP, Rubin S. Biotin uptake by human colonic epithelial NCM460 cells: a carrier-mediated process shared with pantothenic acid. Am J Physiol. 1998;275(5 Pt 1):C1365-1371. (PubMed)
- Said HM. Intestinal absorption of water-soluble vitamins in health and disease. Biochem J. 2011;437(3):357-372. (PubMed)
- Hendler SS, Rorvik DR, eds. PDR for Nutritional Supplements. 2nd ed. Montvale: Thomson Reuters; 2008.
- Flodin N. Pharmacology of micronutrients. New York: Alan R. Liss, Inc.; 1988.
- Debourdeau PM, Djezzar S, Estival JL, Zammit CM, Richard RC, Castot AC. Life-threatening eosinophilic pleuropericardial effusion related to vitamins B5 and H. Ann Pharmacother. 2001;35(4):424-426. (PubMed)
- Herbst RA, Uter W, Pirker C, Geier J, Frosch PJ. Allergic and non-allergic periorbital dermatitis: patch test results of the Information Network of the Departments of Dermatology during a 5-year period. Contact Dermatitis. 2004;51(1):13-19. (PubMed)
- Schmuth M, Wimmer MA, Hofer S, et al. Topical corticosteroid therapy for acute radiation dermatitis: a prospective, randomized, double-blind study. Br J Dermatol. 2002;146(6):983-991. (PubMed)
- Chirapu SR, Rotter CJ, Miller EL, Varma MV, Dow RL, Finn MG. High specificity in response of the sodium-dependent multivitamin transporter to derivatives of pantothenic acid. Curr Top Med Chem. 2013;13(7):837-842. (PubMed)
Exclusión de Responsabilidades
El Centro de Informaciones sobre Micronutrientes del Instituto Linus Pauling entrega información científica relacionado con aspectos de importancia en salud pública de factores dietéticos, suplementos, comestibles y bebidas para el público en general. Esta información se entrega con el entendimiento que ni el autor ni la imprenta están entregando consejos de naturaleza médica, psicológica o nutricional. La información no debe ser usada para reemplazar la consulta con profesionales competentes en el área de cuidado de salud o de nutrición.
La información entregada con relación a factores y suplementos dietéticos, comestibles, y bebestibles, contenida en este sitio web, no cubre todos los usos, acciones, precauciones, efectos secundarios, e interacciones posibles. No debe ser considerado como consejo nutricional o médico para resolver problemas individuales. La responsabilidad legal por las acciones individuales u omisiones que se derivan del uso de este sitio está expresamente excluida.
No se puede copiar, modificar, distribuir, transmitir, realizar, publicar o vender ninguno de los materiales sujetos a derechos de autoría de este sitio web. Puede enlazar a este sitio web, pero debe incluir la siguiente declaración:
"Este enlace lleva a un sitio web proporcionado por el Instituto Linus Pauling en la Universidad Estatal de Oregon. [Su nombre] no está afiliado ni respaldado por el Instituto Linus Pauling o la Universidad Estatal de Oregon."