要約
- フラボノイド類(以下、単にフラボノイドとする)は植物によって合成される多数のポリフェノール化合物である。(詳細はこちら)
- 果物や野菜の豊富な食事に関連するフラボノイドの健康への潜在的有益性に関心が持たれている。(詳細はこちら)
- フラボノイドの生物学的効果の多くは、その抗酸化活性よりも細胞シグナル伝達経路の調整能力に関係しているようである。(詳細はこちら)
- フラボノイドの豊富な食品の高摂取は心血管疾患のリスク低下と関連があるものの、フラボノイドそのものに心臓保護効果があるのかどうかはわかっていない。(詳細はこちら)
- 動物研究では有望な結果になっているが、フラボノイドの高摂取がヒトのがん予防に役立つかどうかは不明である。(詳細はこちら)
- フラボノイドの摂取がヒトの神経変性疾患のリスクにどのように影響するのか不明である。(詳細はこちら)
- フラボノイドの豊富な食品の高摂取は、いくつかの研究で慢性疾患のリスク減少と関連があるものの、単離されたフラボノイドのサプリメントや抽出物がフラボノイドの豊富な食品と同じ効果をもたらすかどうかはわからない。
序説
フラボノイドは植物によって合成される多数のポリフェノール化合物で、共通の化学構造を持つ(図1)。フラボノイドは複数の下位クラスにさらに分類されることもある(表1)。過去10年で、果物や野菜の豊富な食事に関連する健康効果のいくつかを説明する様々な食事性フラボノイドの可能性への関心が高まった。本項では、食事中のフラボノイドが健康を促進しヒトの病気を予防するという仮説に対する科学的エビデンスについて概説する。エストロゲン様活性のあるフラボノイド類であるイソフラボン類の健康効果に関する詳細は、「大豆イソフラボン類」の項の記事を参照されたい。フラボノイドの豊富な食品の健康効果の詳細は、別項の「果物および野菜」 および「茶飲料」の記載内容を参照されたい。

| フラボノイドの下位クラス | 食事中のフラボノイド | 一般的な食品源 |
|---|---|---|
| アントシアニジン類 | シアニジン、デルフィニジン、マルビジン、ペラルゴニジン、ペオニジン、ペツニジン | 赤、青、および紫のベリー類、赤および紫のぶどう、赤ワイン |
| 単量体(カテキン)類: カテキン、エピカテキン、エピガロカテキン、エピカテキンガレート、エピガロカテキンガレート 二量体および重合体: テアフラビン類、, テアルビジン類、プロアントシアニジン類 |
カテキン類: 茶(特に緑茶、白茶)、チョコレート、ぶどう、ベリー類、りんご |
|
| フラバノン類 | ヘスペレチン、ナリンゲニン、エリオジクチオール | オレンジ、グレープフルーツ、レモンなどの柑橘類およびそのジュース |
| フラボノール類 | ケルセチン、ケンプフェロール、ミリセチン、イソラムネチン | 黄タマネギ、わけぎ、ケール、ブロッコリ、りんご、ベリー類、茶などに広く分布 |
| フラボン類 | アピゲニン、ルテオリン | パセリ、タイム、セロリ、唐辛子 |
| イソフラボン類 | ダイゼイン、ゲニステイン、グリシテイン | 大豆、大豆食品、豆類 |






代謝と生物学的利用能
1つまたはそれ以上の糖分子に結合したフラボノイドはフラボノイド配糖体(グリコシド)として知られ、糖分子に結合していないものはアグリコンと呼ばれる。フラバノール類(カテキン類とプロアントシアニジン類)を除いて、フラボノイドは植物およびほとんどの食品でグリコシドとして存在する(2)。調理の後でも、ほとんどのフラボノイドのグリコシドは小腸にそのまま到達する。フラボノイドアグリコンとフラボノイドグルコシド(グルコースに結合したもの)だけが小腸で吸収され、急速に代謝されてメチル化物、グルクロン酸抱合体、または硫酸化物となる(3)。通常は結腸に住み着いているバクテリアも、フラボノイドの代謝と吸収に重要な役割を果たす。結腸に到達したフラボノイドまたはフラボノイド代謝物は、バクテリアの酵素によってさらに代謝され吸収されることもある。特定のフラボノイド代謝物を生成できる能力は個人によって異なり、結腸の微生物叢環境に依るのかもしれない(4,5)。フラボノイドの吸収が限られることや急速に排出されることから、一般にフラボノイドの生物学的利用能は比較的低い。生物学的利用能は、様々なフラボノイドによって異なる。イソフラボン類は最も生物学的に利用性の高いグループのフラボノイドであるが、フラバノール類(プロアントシアニジン類および茶のカテキン類)とアントシアニン類の吸収は非常に悪い(6)。フラボノイドは急速かつ広範囲に代謝されるので、フラボノイド代謝物の生物学的活性は元の化合物のそれと同じであるとは限らない((7)の文献で概説)。培養細胞におけるフラボノイドの研究からのデータを評価する際には、フラボノイドの濃度と使用されたフラボノイド代謝物が生理学的に妥当かどうかを考慮することが大切である(8)。ヒトでは、大豆イソフラボン類および柑橘類フラバノン類の血漿濃度の最大値は、経口摂取後に10マイクロモル/リットルを超えたことがない。アントシアニン類、フラバノール類、およびフラボノール類(茶由来のものを含む)の摂取後の血漿濃度の最大値は、一般に1マイクロモル/リットル未満である(3)。
生物学的活性
直接的抗酸化活性
フラボノイドは、試験管内(インビトロ)ではフリーラジカル(遊離基)を効果的に除去する(9,10)。しかし、フラボノイドを非常にたくさん摂取しても、ヒトの血漿および細胞内フラボノイド濃度は、アスコルビン酸(ビタミンC)、尿酸、またはグルタチオンといったその他の抗酸化物質の100~1000分の1以下であろう。しかもほとんどの血液循環中のフラボノイドは、実際はフラボノイド代謝物であり、そのいくつかはもとのフラボノイドよりも抗酸化活性が低い。これらの理由から、生体内の血漿および組織内での抗酸化機能に食事由来のフラボノイドが果たす相対的な貢献度は、非常に小さいか無視できる程度であろう(7,11,12)。
金属キレート化
鉄や銅といった金属のイオンは、フリーラジカルの生成に触媒として機能する。フラボノイドが金属イオンをキレート化する(結合する)性質は、インビトロでの抗酸化活性に寄与しているようである(13,14)。生物体内ではほとんどの鉄および銅はタンパク質と結合し、フリーラジカルを生成する反応への関与は限られている。フラボノイドの金属キレート化活性は、鉄または銅が過剰な病的状態では有益であるかもしれないが、フラボノイドまたはその代謝物が生体内で有効な金属キレート剤として機能するかどうかは不明である(11)。
細胞シグナル伝達経路への効果
細胞は特定のタンパク質の利用性を増やしたり減らしたりすることで、様々なストレスやシグナルに対して応答することができる。特定の遺伝子の発現に変化をもたらす複雑な一連の事象は,細胞シグナル伝達経路またはシグナル伝達経路として知られている。これらの経路は、成長、増殖、および死(アポトーシス)を含む多数の細胞プロセスを調整している。フラボノイドの生物学的効果は、その抗酸化活性に関係すると初めは仮定されていた。しかし培養細胞での実験によるエビデンスから、フラボノイドの生物学的効果の多くは、その細胞シグナル伝達経路を調整する能力に関係するということが示唆されている(7)。細胞シグナル伝達経路に影響するのに必要なフラボノイドの細胞内濃度は、細胞の抗酸化能力に影響するのに必要な濃度よりもかなり低い。フラボノイドの代謝物は、その抗酸化活性がなくなっても細胞シグナル伝達タンパク質と反応する性質を保持している可能性がある(15,16)。シグナル伝達が有効に行われるには、特定の部位で標的タンパク質のリン酸化を促すキナーゼというタンパク質が必要である。シグナル伝達タンパク質の特定のリン酸化や脱リン酸化の一連の反応は、DNAの特定の応答エレメントと結びつき様々な遺伝子の転写を促進あるいは抑制するタンパク質である転写因子の活性に最終的に影響する。多数の培養細胞での研究結果から、選択的にキナーゼを抑制することでフラボノイドが慢性疾患に影響を及ぼしている可能性があることが示唆されている(7,17)。細胞の成長や増殖も成長因子によって調整されており、成長因子は細胞膜の特定の受容体と結合することで細胞シグナル伝達反応を起こす。フラボノイドは受容体のリン酸化の抑制、または成長因子と受容体の結合を妨げることで、成長因子のシグナル伝達を変えるのかもしれない(18)。
フラボノイドが細胞シグナル伝達経路を調整することで、がん予防に役立つかもしれない。それには以下のような方法がある。
- 第二相解毒酵素の活性を刺激する(19,20):第二相解毒酵素は、有害な可能性のある化合物または発がん性のある化合物の排泄を促進する反応の触媒作用をする。
- 正常な細胞周期の調整を保持する(21,22):細胞は一度分裂すると、細胞周期として知られる一連の段階を経てから再び分裂する。DNA損傷の後、細胞周期は損傷チェックポイントにおいて一時的に停止し、DNA修復をしたり、損傷が修復不能な場合の細胞死(アポトーシス)に至る経路を活性化させたりする(23)。細胞周期の調整に不具合があると、がんの発症に寄与する突然変異が伝播してしまう可能性がある。
- 細胞増殖を抑制しアポトーシスへと導く(24-26):正常な細胞と違って、がん細胞は急速に増殖し、アポトーシスを起こす細胞死のシグナルに応答する能力を失う。
- 腫瘍浸潤および血管新生の抑制(27,28):がん細胞は、マトリックスメタロプロテアーゼと呼ばれる酵素の助けを借りて、正常な組織に浸潤していく。その急速な成長を促進するため、浸潤する腫瘍は血管新生として知られるプロセスによって新たな血管を作らねばならない。
- 炎症を減らす(29-31):炎症は炎症性酵素によるフリーラジカルの生成を局所的に増やしたり、細胞増殖や血管新生を促してアポトーシスを抑制する炎症メディエーター(仲介物質)の放出に至ったりする可能性がある(32)。
- フラボノイドによって細胞シグナル伝達経路を調整することは、以下のように心臓血管疾患の予防に役立つ可能性がある。
- 炎症の減少(29-31):アテローム性動脈硬化症は、現在では炎症性疾患として認識されており、炎症に関するいくつかの測定値が心筋梗塞(心臓発作)のリスク増加と関連している(33)。
- 血管細胞接着分子の発現の低下(34,35):アテローム性動脈硬化症の発症における初期の事象の一つが、炎症性の白血球が血液から動脈壁に移動することである。この事象は、血管の内壁を形成する血管内皮細胞による接着分子の発現に依存している(36)。
- 内皮型一酸化窒素合成酵素(eNOS)活性の上昇(37):eNOSは、血管内皮細胞による一酸化窒素生成の触媒作用をする酵素である。一酸化窒素は、動脈弛緩(血管拡張)を維持するのに必要である。一酸化窒素による血管拡張が損なわれることは、心臓血管疾患のリスク上昇と関連がある(38)。
- 血小板凝集の減少(39,40):血小板凝集は冠状動脈や大脳動脈を詰まらせることもある血餅の形成における第一段階の一つであり、それぞれ心筋梗塞や脳卒中に至る。血小板凝集の抑制は、心臓血管疾患の一次予防および二次予防における重要な方策であると考えられている(41)。
疾病予防
心臓血管疾患
疫学的エビデンス
米国およびヨーロッパで行われたいくつかの前向きコホート研究で、食事からのフラボノイド摂取量の値と冠動脈心疾患(CHD)リスクの関係が調べられた(42-49)。フラボノイドの高摂取がCHDリスクの大きな減少と関連しているとする研究もあった(42-46,50)が、何の関係もないとする研究もあった(47-49,51)。一般にこれらの研究集団でフラボノイド全体の摂取の大部分を占める食品は、紅茶、りんご、およびタマネギであった。オランダのある研究では、ココアも食事由来のフラボノイドの重要な食品源であることがわかった。食事由来ラボノイドの摂取量と脳卒中リスクとの関係を調べた7つの前向きコホート研究のうち、2つだけがフラボノイドの高摂取は脳卒中リスクの有意な減少と関連があるとしている(45,52)が、その他の5つでは何の関係も見い出せなかった(46,49,50,53,54)。前向きコホート研究のデータは、フラボノイドの豊富な食品の高摂取がCHDから体を守るのに役立つかもしれないと示唆しているが、しかしながら、そのような保護性がフラボノイドによるのか、フラボノイドの豊富な食品に含まれるその他の栄養素や植物性化学物質によるものなのか、それとも食品全体によるものなのかは決定できていない(55)。
血管内皮機能
血管内皮細胞は、動脈弛緩(血管拡張)を促進する化合物である一酸化窒素を生成することによって、心臓血管の健康を維持するのに重要な役割を果たしている(56)。血管内皮の一酸化窒素生成による動脈の血管拡張は、内皮依存性血管拡張と呼ばれる。フラボノイドの豊富な食品および飲料が内皮依存性血管拡張に及ぼす効果を調べた臨床試験がいくつかある。2つの対照臨床試験では、4~5杯(900~1,250ml)の紅茶を4週間毎日摂取したところ、同量のカフェインのみ、または、お湯の場合と比べて、冠動脈疾患の患者(57)および血清コレステロール濃度がやや高い患者(58)の内皮依存性血管拡張が有意に改善した。その他の小規模臨床試験でも、約3杯(640ml)の紫ぶどうジュース(59)またはフラボノイドが多いビターの板チョコレート(60)を2週間毎日摂取したところ、同様の内皮依存性血管拡張の改善が見られた。もっと最近では、コレステロール濃度の高い32人の閉経後の女性にココアを6週間飲んでもらう介入試験で、ココアを毎日摂取することで内皮機能に有意な向上が見られた(61)。内皮機能の向上は、従来の投薬を受けている2型糖尿病患者がフラバノールの豊富なココアを30日間補給した後でも見られた(62)。フラバノールのエピカテキンが、フラバノールの豊富なココアに含まれる血管拡張効果の元になる化合物の一つであるようだ(63)。興味深いことに、44人の年配の成人による最近の無作為化対照試験では、フラボノイドの豊富なビターチョコレートを少量(6.3g/日を18週間。30カロリーに相当)与えたところ、フラボノイドの入っていないホワイトチョコレートに比べて、一酸化窒素生成の指標である血漿Sニトロソグルタチオン濃度が高くなった(64)。
内皮の一酸化窒素生成は、血餅形成の第一段階の一つである血小板の接着や凝集も抑制する(56)。フラボノイドの高摂取が、体外(ex vivo)での血小板凝集を示す様々な測定値を減少させる可能性については、多数の臨床試験で調べられており、そのような試験ではまちまちの結果が報告されている。一般に、果物および/または野菜の摂取を増やしてフラボノイドの摂取を増やしても、体外での血小板凝集に大きな影響はない(41,65,66)し、紅茶の摂取を増やしても同様である(67,68)。しかしながら、健康な成人によるいくつかの小規模臨床試験では、ぶどうジュース(約500ml/日)を7~14日間摂取後に、血小板凝集の体外での測定値が有意に減少した(69-71)。同様の血小板凝集の抑制が急激または短期間のビターチョコレートの摂取後(72)やフラボノイドの豊富なココア飲料の急激な摂取後(73,74)に報告されている。加えて、32人の健康な成人によるプラセボ対照試験では、ココアからのフラバノールおよびプロシアニジンの4週間にわたる摂取によって、血小板の凝集と機能が抑制されたことがわかった(75)。いくつかの対照臨床試験の結果で、紅茶、紫ぶどうジュース、およびココアを含むフラボノイドの豊富な食品や飲料の比較的高い摂取が、血管内皮機能を向上させる可能性があることが示唆された。しかし、これらの短期間での向上が、心臓血管疾患リスクの長期にわたる減少に至るのか不明である。
がん
肺がん(76)、口腔がん(77)、食道がん(78)、胃がん(79)、結腸がん(80)、皮膚がん(81)、前立腺がん(82,83)、および乳がん(84)の動物モデルで、化学的に誘発されたがんの発症を様々なフラボノイドが抑制することが知られているが、疫学的研究では食事由来のフラボノイドの高摂取がヒトのがんリスクの大幅な減少と関連しているという説得力のあるエビデンスは示されていない。食品の摂取頻度を質問して食事由来のフラボノイドの摂取量を評価するほとんどの前向きコホート研究では、フラボノイドの摂取ががんリスクと逆相関があるとはわかっていない(85)。ヨーロッパでの2つの前向きコホート研究では、フラボン類およびフラボノール類(86,87)、カテキン類(88)、または茶(89)の食事からの摂取と様々ながんのリスクには何の関係もなかった。米国の閉経後の女性群では、果物や野菜からではなく茶からのカテキンの摂取が直腸がんのリスクと逆相関があったが、その他のがんでは関係がなかった(90)。平均的なフラボノイド摂取が比較的低いフィンランドでの2つの前向きコホート研究で、フラボノール類とフラボン類の食事からの摂取が最も多い男性は、摂取が最も少ない男性よりも肺がん発症のリスクが有意に低いことがわかった(44,45)。個々の食事由来フラボノイドについて分析をすると、主にりんごからの食事由来ケルセチンの摂取が肺がんリスクと逆相関があり、ミリセチンの摂取が前立腺がんのリスクと逆相関があった(45)。ある集団では茶はフラボノイド(フラバノール類およびフラボノール類)の重要な摂取源であるが、ほとんどの前向きコホート研究では茶の摂取ががんのリスクと逆相関があるという結果は見つかっていない((91)の文献で概説)。症例対照研究の結果は、食べたものを思い出す際の偏りにより影響を受けやすいが、この結果もまちまちであった。いくつかの研究では、肺がん(92)、胃がん(93,94)、および乳がん(95)と診断された人々にフラボノイド摂取が少なかったが、その他の多くの研究では、がんの患者と対照群の間にフラボノイド摂取の大きな差は見られなかった(96,97)。食品からのフラボノイドの摂取が少ないと特定のがんリスクが上昇するというエビデンスは限定されているが、それがフラボノイド摂取不足に関係するのか、それともフラボノイドの豊富な食品に含まれるその他の栄養素や植物性化学物質に関係するのかは不明である。フラボノイドの豊富な食品とがんとの関係の詳細については、「果物と野菜」、および「茶飲料」の項の記事を参照されたい。特定のフラボノイドががんの予防や治療に有益であるかを決定する臨床試験が必要であるが、いくつかの臨床試験が進行中である。(詳細はhttp://www.cancer.gov/about-cancer/treatment/clinical-trialsを参照のこと)
神経変性疾患
炎症、酸化ストレス、および遷移金属の蓄積が、パーキンソン病およびアルツハイマー病を含むいくつかの神経変性疾患の病理に関わっているようである(98)。フラボノイドは抗炎症特性、抗酸化特性、および金属キレート化特性があるので、フラボノイドの豊富な食事または個々のフラボノイドが神経を保護する可能性に興味が持たれる。現在のところ、様々な食事に由来するフラボノイドやフラボノイド代謝物のどれがヒトの血液脳関門を超えることができるのかといったところまではわかっていない(99,100)。フラボノイドの豊富な食事やフラボノイドの投与が、いくつかの動物を用いた研究で、老化および炎症に伴う認知障害を予防することはわかっている(101-104)が、前向きコホート研究では、フラボノイドの摂取とヒトの認知症または神経変性疾患のリスクとの間に一貫した逆相関は見出されていない(105-109)。日系アメリカ人男性の集団を25~30年間追跡した結果では、中年の頃に茶からフラボノイド摂取をしても、晩年のアルツハイマー病やその他の認知症リスクとの相関はなかった(105)。驚いたことに、中年の頃にイソフラボンの豊富な豆腐の摂取が多いと、晩年の認知障害や脳萎縮と関連があった(「大豆イソフラボン」の項の記事参照)(106)。オランダの成人による前向き研究では、毎日のフラボノイド摂取が12mg増えるごとにアルツハイマー病のリスクが50%低下した現在喫煙中の者以外は、食事由来の全フラボノイド摂取量はパーキンソン病の発症リスク(107)またはアルツハイマー病の発症リスク(108)と関連がなかった。対照的に、年配のフランス人男性および女性の研究では、フラボノイド摂取が最も少ない者はその後の5年間に認知症を発症するリスクが、最も高摂取な者に比べて50%高いことがわかった(109)。より最近では1,640人の年配の男女の研究で、食事由来フラボノイドの摂取が多い(13.6mg/日より多い)者は、フラボノイド摂取の少ない(0~10.4mg/日)者に比べて、研究開始時の認知行動能力がより高く、10年間にわたって加齢に関連する認知機能低下が有意に少なかった(110)。加えて、202人の閉経後の女性を対象にした無作為化二重盲検プラセボ対照臨床試験では、25.6gの大豆タンパク質(イソフラボンを99mg含有)を1年間毎日補給しても、認知機能の向上は見られなかったと報告された(111)。しかし、77人の閉経後の女性による無作為化二重盲検プラセボ対照交差試験では、60mg/日のイソフラボンを6ヶ月にわたって補給したところ、認知行動能力の測定値がいくつか向上した(112)。加齢化する脳を保護するかもしれないフラボノイドに関心が持たれているが、フラボノイドの摂取がヒトの神経変性疾患リスクにどのように影響するのか不明である。
摂取源
食品源
フラボノイドの食事からの摂取源には、茶、赤ワイン、果物、野菜、および豆類がある。個々のフラボノイドの摂取は、茶、赤ワイン、大豆製品、または果物や野菜が一般的に摂取されているかどうかでかなり異なる可能性がある((3)の文献で概説)。個々のフラボノイドの摂取は異なっても、西洋諸国でのフラボノイド全体の摂取は平均で約150~200mg/日のようである(3,113)。いくつかのフラボノイドが豊富な食品のフラボノイド含有量を表2と3に示す。農業のやり方、環境要因、熟成、処理方法、貯蔵、および調理などの様々な要因が食品のフラボノイド含有量に影響する可能性があるので、これらの値は近似値とみなされるべきである。食品のフラボノイド含有量についての詳細は、特定の食品についてのフラボノイドおよびプロアントシアニジン含有量に関するUSDAのデータベースを参照されたい。大豆食品のイソフラボン含有量に関しては、「大豆イソフラボン」の項の記事を参照するか、特定の食品についてのイソフラボン含有量に関するUSDAのデータベースを参照されたい。
| アントシアニンが豊富な食品 | アントシアニン類 | フラバノール類 | プロアントシアニジン類 |
|---|---|---|---|
| ブラックベリー | 89-211 | 13-19 | 6-47 |
| ブルーベリー | 67-183 | 1 | 88-261 |
| 赤ぶどう | 25-92 | 2 | 44-76 |
| 赤ラズベリー | 10-84 | 9 | 5-59 |
| いちご | 15-75 | - | 97-183 |
| 赤ワイン | 1-35 | 1-55 | 24-70 |
| セイヨウスモモ | 2-25 | 1-6 | 106-334 |
| 紫(赤)キャベツ | 25 | 0 | - |
| 紫タマネギ | 13- 25 | - | - |
| 果肉の赤いオレンジのジュース | 3-10 | - | - |
| フラバノールの豊富な食品 | アントシアニン類 | フラバノール類 | プロアントシアニジン類 |
| 緑茶 | - | 24-216 | - |
| 紅茶 | - | 5-158 | 4 |
| ビターチョコレート | - | 43-63 | 90-322 |
| 皮付きレッドデリシャスりんご | 1-4 | 2-12 | 89-148 |
| アンズ | - | 10-25 | 8-13 |
| フラボンの豊富な食品 | アントシアニン類 | フラバノール類 | プロアントシアニジン類 |
| 生のパセリ | - | - | - |
| 生のタイム | - | - | - |
| 緑色のセロリの芯 | - | - | - |
| セロリ | - | - | - |
| 生のオレガノ | - | - | - |
| 緑色の唐辛子 | - | - | - |
| フラバノンの豊富な食品 | アントシアニン類 | フラバノール類 | プロアントシアニジン類 |
| 生のレモンジュース | - | - | - |
| 生のグレープフルーツジュース | - | - | - |
| 生のオレンジジュース | - | - | - |
| 生のグレープフルーツ | - | - | - |
| 生のオレンジ | - | - | - |
| フラボノールの豊富な食品 | アントシアニン類 | フラバノール類 | プロアントシアニジン類 |
| 黄タマネギ | - | 0 | - |
| ケール | - | - | - |
| ネギ | - | 0 | - |
| ブロッコリ | - | 0 | - |
| *生の食品の重さ100gまたは液体100mlについての含有量。100gは約3.5オンス、100mlは約3.5液量オンス。 | |||
| アントシアニンの豊富な食品 | フラボン類 | フラボノール類 | フラバノン類 |
|---|---|---|---|
| ブラックベリー | - | 0-2 | - |
| ブルーベリー | - | 2-16 | - |
| 赤ぶどう | - | 3-4 | - |
| 赤ラズベリー | - | 1 | - |
| いちご | - | 1-4 | - |
| 赤ワイン | 0 | 2-30 | - |
| セイヨウスモモ | 0 | 1-2 | - |
| 紫(赤)キャベツ | 0-1 | 0-1 | - |
| 紫タマネギ | 0 | 4-100 | - |
| 果肉の赤いオレンジのジュース | - | - | 10-22 |
| フラバノールの豊富な食品 | フラボン類 | フラボノール類 | フラバノン類 |
| 緑茶 | 0-1 | 3-9 | - |
| 紅茶 | 0 | 1-7 | - |
| ビターチョコレート | - | - | - |
| 皮付きレッドデリシャスりんご | 0 | 2-6 | - |
| アンズ | 0 | 2-5 | - |
| フラボンの豊富な食品 | フラボン類 | フラボノール類 | フラバノン類 |
| 生のパセリ | 24-634 | 8-10 | - |
| 生のタイム | 56 | 0 | - |
| 緑色のセロリの芯 | 23 | - | - |
| セロリ | 0-15 | 4 | - |
| 生のオレガノ | 2-7 | 0 | - |
| 緑色の唐辛子 | 5 | 13-21 | - |
| フラバノンの豊富な食品 | >フラボン類 | フラボノール類 | フラバノン類 |
| 生のレモンジュース | 0 | 0-2 | 2-175 |
| 生のグレープフルーツジュース | 0 | 0 | 10-104 |
| 生のオレンジジュース | 0-1 | 0 | 5-47 |
| 生のグレープフルーツ | - | 1 | 55 |
| 生のオレンジ | - | - | 42-53 |
| フラボノールの豊富な食品 | フラボン類 | フラボノール類 | フラバノン類 |
| 黄タマネギ | 0 | 3-120 | - |
| ケール | 0 | 30-60 | - |
| ネギ | 0 | 3-22 | - |
| ブロッコリ | 0 | 4-13 | - |
| *生の食品の重さ100gまたは液体100mlについての含有量。100gは約3.5オンス、100mlは約3.5液量オンス。 | |||
サプリメント
アントシアニン類
アントシアニンの豊富なビルベリー、エルダーベリー、黒すぐり、ブルーベリー、赤ぶどう、およびベリー類の抽出物は、米国では処方箋なしで栄養補助食品として入手可能である。これらの製品のアントシアニンの含有量は、かなり異なる可能性がある。用量ごとのアントシアニンの量のリストを示した規格化された抽出物が入手可能である。
フラバノール類
米国では多数の茶抽出物が栄養補助食品として入手可能で、茶カテキンまたは茶ポリフェノールというラベルが付いていることもある。緑茶の抽出物は最も一般的に市販されているが、紅茶やウーロン茶の抽出物も入手可能である。緑茶抽出物は一般的にカテキン(フラバノール単量体)の量が多く、紅茶抽出物はテアフラビンやテアルビジン(茶に含まれるフラバノール重合体)が豊富である。ウーロン茶の抽出物は、フラバノール含有量では緑茶と紅茶の抽出物の中間にあたる。茶の抽出物にはカフェインを含むものも、カフェイン抜きのものもある。フラバノールとカフェインの含有量は製品によってかなり異なるので、各サプリメントを毎日摂取することによるフラバノールやカフェインの量を決めるには、ラベルをチェックするか、メーカーに問い合わせることが大切である。茶のフラバノールについての詳細は、「茶飲料」の項の記事を参照されたい。
フラバノン類
柑橘類のバイオフラボノイドサプリメントは、ヘスペレチンのグリコシド(ヘスペリジン)、ナリンゲニンのグリコシド(ナリンジン)、およびエリオジクチオールのグリコシド(エリオシトリン)を含む可能性がある。ヘスペリジンはヘスペリジン複合体サプリメントとしても入手可能である(114)。
フラボン類
柑橘類の皮は、タンゲレチン、ノビレチン、およびシネンセチンといったポリメトキシフラボンが豊富である(3)。これらの天然起源フラボン類の食事からの摂取は一般に低いものの、柑橘類のバイオフラボノイドサプリメントにはしばしば含まれている。
フラボノール類
フラボノールアグリコンであるケルセチンおよびそのグリコシドであるルチンは、米国では処方箋なしで栄養補助食品として入手可能である。ルチンにはルチノシド、ケルセチン-3-ルチノシド、およびソフォリンなどという名称もある(114)。柑橘類のバイオフラボノイドサプリメントもケルセチンやルチンを含んでいる可能性がある。
安全性
悪影響
植物性食品に由来するフラボノイド類の高摂取に関連する悪影響はない。悪影響がないことは、ほとんどのフラボノイドの生物学的利用能が比較的低いことと、急速に代謝および除去されることで説明ができるかもしれない。
ケルセチン
ケルセチンのサプリメント(1,000mg/日を1ヶ月)を摂取した何人かの男性が、吐き気、頭痛、または四肢の刺痛を報告した(115)。第一相臨床試験でケルセチンを静脈投与された何名かのがん患者が、吐き気、嘔吐、発汗、のぼせ、および呼吸困難を報告した(116)。その試験では、945mg/m2、あるいはそれ以上の用量のケルセチンの静脈投与は腎毒性に関連があった。
茶抽出物
茶(学名Camellia sinensis)抽出物のサプリメントを摂取した後の肝毒性の報告がいくつかある(117,118)。カフェイン入りの緑茶抽出物の臨床試験で、6g/日を3~6回に分けて摂取したがん患者は、吐き気、嘔吐、腹痛、および下痢を含む軽度から中度の胃腸の副作用を報告した(119,120)。激越(興奮)、不穏状態、不眠、震え、めまい、および錯乱を含む中枢神経系の症状も報告されている。あるケースでは、入院を必要とするくらい錯乱が重篤であった(119)。これらの副作用は、緑茶抽出物に含まれるカフェインに関連しているようである(120)。健康な個人でカフェイン抜きの緑茶抽出物(800mg/日のEGCG)の安全性を評価する4週間の臨床試験で、参加者の何人かが軽度の吐き気、胃のむかつき、めまい、または筋肉痛を訴えた(121)。
妊娠期および授乳期
妊娠期および授乳期におけるフラボノイドサプリメント摂取の安全性は確立されていない(114)。
薬物相互作用
グレープフルーツジュースとフラボノイドによるCYP3A4の阻害
たった200ml(7液量オンス)のグレープフルーツジュースでも、腸の薬物代謝酵素であるシトクロムP450(CYP)3A4を不可逆的に阻害することがわかっている(122)。グレープフルーツの最も強力なCYP3A4阻害物質はフラノクマリン類、特にジヒドロキシベルガモチンであると考えられるが、フラボノイドのナリンゲニンとケルセチンも、試験管内でCYP3A4を阻害することがわかっている。腸のCYP3A4を阻害すると、HMG-CoA還元酵素阻害薬(アトルバスタチン、ロバスタチン、およびシンバスタチン)、カルシウムチャネル拮抗薬(フェロジピン、ニカルジピン、ニソルジピン、ニトレンジピン、およびベラパミル)、抗不整脈薬(アミオダロン)、HIVプロテアーゼ阻害薬(サキナビル)、免疫抑制剤(シクロスポリン)、抗ヒスタミン薬(テルフェナジン)、胃腸刺激薬(シサプリド)、ベンゾジアゼピン(ジアゼパム、ミダゾラム、およびトリアゾラム)、抗けいれん薬(カルバマゼピン)、抗不安薬(ブスピロン)、選択的セロトニン再取込阻害薬(セルトラリン)、および勃起不全治療薬(シルデナフィル)などの多くの薬物の生物学的利用能および毒性のリスクを上げる可能性がある(123)。グレープフルーツジュースは、アンジオテンシンII受容体拮抗薬であるロサルタンの治療効果を下げる可能性がある。薬物相互作用の悪影響の可能性があるので、臨床医の中にはCYP3A4による広範な前全身的代謝を受ける薬を服用している患者は、潜在的毒性を避けるためにグレープフルーツジュースをまったく飲まないようにアドバイスする者もいる(122)。
グレープフルーツジュースとフラボノイドによるP糖タンパク質の阻害
P糖タンパク質は、多数の薬物の吸収を減らす排出輸送体である。グレープフルーツジュースの摂取がP糖タンパク質の活性を抑制するというエビデンスがある(122)。ケルセチン、ナリンゲニン、および緑茶フラバノールであるエピガロカテキンガレート(EGCG)は、培養細胞でP糖タンパク質の排出活性を抑制することがわかっている(124)。したがって、これらのフラボノイドを非常に多く摂取したり補給したりするとフラボノイドの生物学的利用性が上昇し、P糖タンパク質の基質である薬物の毒性を高める可能性がある。P糖タンパク質の基質であることがわかっている薬物は、ジゴキシン、抗高血圧症薬、抗不整脈薬、化学療法薬(抗がん剤)、抗真菌薬、HIVプロテアーゼ阻害薬、免疫抑制剤、H2受容体拮抗薬、およびいくつかの抗生物質や、その他などである((125)の文献で概説)。
抗凝固薬および血小板凝集阻害薬
紫ぶどうジュース(500ml/日)やビターチョコレート(235mg/日のフラバノール類)からフラボノイドを高摂取すると、体外での試験では血小板凝集を阻害することがわかっている(69-71,75)。理論的には、ワルファリン(クマジン)などの抗凝固薬、クロピドグレル(プラビックス)、ジピリダモール(ペルサンチン)などの血小板凝集阻害薬、非ステロイド系抗炎症薬(NSAID)、およびアスピリンなどと一緒に摂取すると、(サプリメントなどからの)フラボノイドの高摂取が出血のリスクを高める可能性がある。
他の栄養素との相互作用
非ヘム鉄
フラボノイドは、非ヘム鉄と結びついて腸での鉄の吸収を阻害することがある。非ヘム鉄は、植物性食品、乳製品、および鉄のサプリメントに含まれる鉄の主要な形態である。食事と一緒に1杯の紅茶やココアを摂取すると、食事に含まれる非ヘム鉄の吸収を約70%減らすことがわかっている(126,127)。食事や鉄サプリメントからの鉄の吸収を最大化するには、フラボノイドの豊富な飲料やフラボノイドのサプリメントを同時に摂取するべきではない。
ビタミンC
培養細胞での研究で、多くのフラボノイドが細胞へのビタミンCの輸送を阻害することが示され、ケルセチンとビタミンCを補給したラットは腸でのビタミンCの吸収が減った(128)。これらの発見のヒトにおける重要性を決定するさらなる研究が必要である。
Authors and Reviewers
Originally written in 2005 by:
Jane Higdon, Ph.D.
Linus Pauling Institute
Oregon State University
Updated in June 2008 by:
Victoria J. Drake, Ph.D.
Linus Pauling Institute
Oregon State University
Reviewed in June 2008 by:
Roderick H. Dashwood, Ph.D.
Director, Cancer Chemoprotection Program, Linus Pauling Institute
Professor of Environmental & Molecular Toxicology
Leader, Environmental Mutagenesis & Carcinogenesis Core, Environmental Health Sciences Center
Oregon State University
Copyright 2005-2026 Linus Pauling Institute
Figure Alternative Text
Figure 1. Basic structure of a flavonoid
The figure shows the basic general structure of a flavonoid, with three rings.
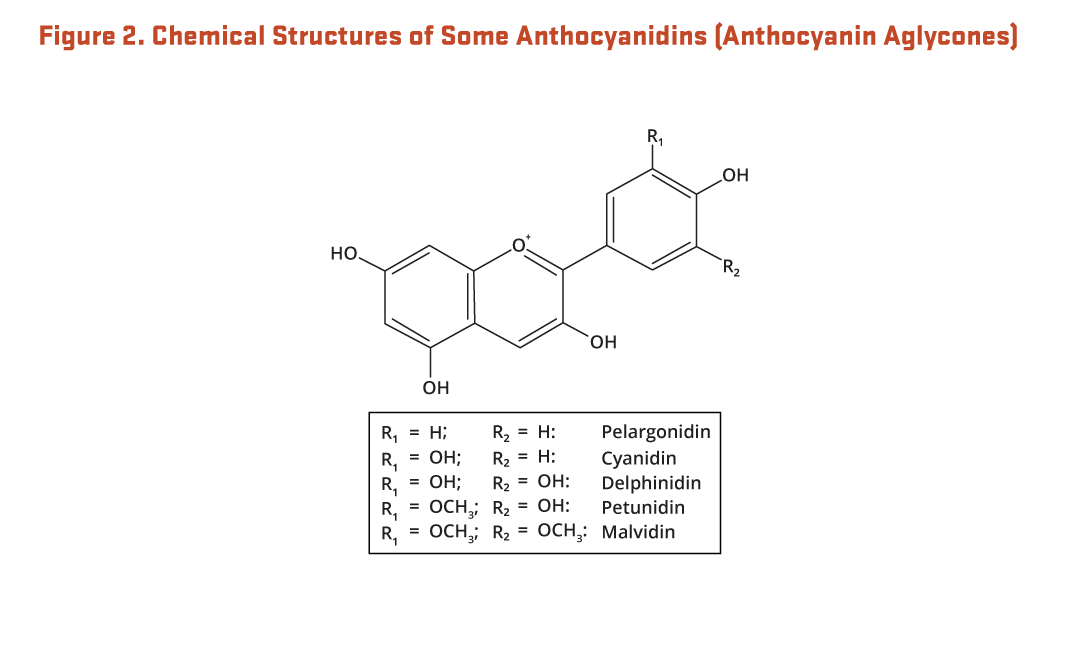
Figure 2. Chemical structures of some anthocyanidins (anthocyanin aglycones)
The figure shows a general structure of an anthocyanidin molecule, with two variable positions labeled R1 and R2. An inset lists the R-groups and resulting compounds:
- Pelargonidin: R1= H, R2=H
- Cyanidin: R1=OH, R2=H
- Delphinidin: R1=OH, R2=OH
- Petunidin: R1=OCH3, R2=OH
- Malvidin: R1=OCH3, R2=OCH3
Figure 3. Chemical structures of some flavanol monomers (catechins)
The figure shows the chemical structures of several flavanol monomers, known collectively as catechins. (+)-catechin, (+)-gallocatechin, (-)-epicatechin, (-)-epigallocatechin, (-)-epicatechin gallate, and (-)-epigallocatechin gallate.
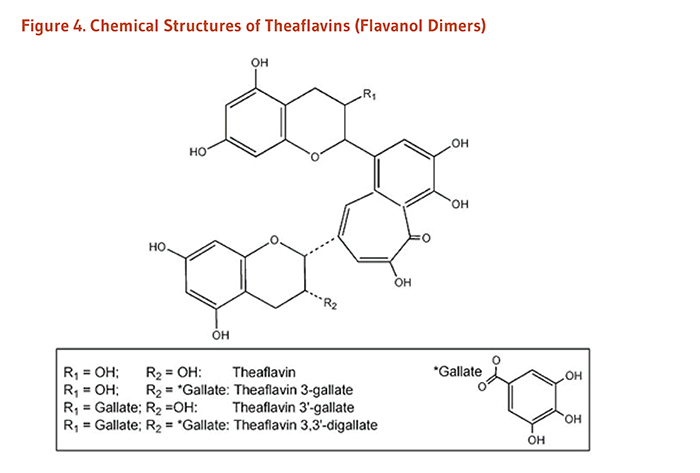
Figure 4. Chemical structures of theaflavins (flavanol dimers)
The figure shows a general structure of a theaflavin molecule, with two variable positions labeled R1 and R2. A separate structure of the gallate group is also shown. A key lists the R-groups and resulting compounds:
- Theaflavin: R1=OH, R2=OH
- Theaflavin-3-gallate: R1=OH, R2=gallate group
- Theaflavin-3’-gallate: R1=gallate group, R2=OH
- Theaflavin-3,3’-digallate: R1=gallate group, R2=gallate group
Figure 5. Chemical structures of proanthocyanidins (flavanol dimers and polymers)
The figure shows the chemical structures of proanthocyanidins, including flavanol dimers and polymers. On the left is a general repeating-unit structure of polymeric proanthocyanidins. Two variable R-groups are shown, with the accompanying key defining each subclass:
- Procyanidins: R1=H, R2=OH
- Prodelphinidins: R1=OH, R2=OH
- Propelargonidins: R1=H, R2=H
On the right is the structure of a procyanidin dimer.
Figure 6. Chemical structures of some flavanones
The figure shows a general structure of a flavanone molecule, with two variable positions labeled R1 and R2. A key lists the R-groups and resulting compounds:
- Naringenin: R1=H, R2=OH
- Eriodictyol: R1=OH, R2=OH
- Hesperetin: R1=OH, R2=OCH3
Figure 7. Chemical structures of flavonols
The figure shows a general structure of a flavonol molecule, with two variable positions labeled R1 and R2. A key lists the R-groups and resulting compounds:
- Kaempferol: R1=H, R2=H
- Quercetin: R1=OH, R2=H
- Myricetin: R1=OH, R2=OH
- Isorhamnetin: R1=OCH3, R2=H
Figure 8. Chemical structures of some flavones
The figure shows a general structure of a flavone molecule, with one variable position labeled R1. A key lists the R-groups and resulting two compounds:
- Apigenin: R1=H
- Luteolin: R1=OH
Figure 9. Chemical structures of some isoflavones
The figure shows chemical structures of three isoflavones: daidzein, genistein, and glycitein.
References
- Beecher GR. Overview of dietary flavonoids: nomenclature, occurrence and intake. J Nutr. 2003;133(10):3248S-3254S. (PubMed)
- Williamson G. Common features in the pathways of absorption and metabolism of flavonoids. In: Meskin MS, R. BW, Davies AJ, Lewis DS, Randolph RK, eds. Phytochemicals: Mechanisms of Action. Boca Raton: CRC Press; 2004:21-33.
- Manach C, Scalbert A, Morand C, Remesy C, Jimenez L. Polyphenols: food sources and bioavailability. Am J Clin Nutr. 2004;79(5):727-747. (PubMed)
- Setchell KD, Brown NM, Lydeking-Olsen E. The clinical importance of the metabolite equol-a clue to the effectiveness of soy and its isoflavones. J Nutr. 2002;132(12):3577-3584. (PubMed)
- Yuan JP, Wang JH, Liu X. Metabolism of dietary soy isoflavones to equol by human intestinal microflora--implications for health. Mol Nutr Food Res. 2007;51(7):765-781. (PubMed)
- Manach C, Williamson G, Morand C, Scalbert A, Remesy C. Bioavailability and bioefficacy of polyphenols in humans. I. Review of 97 bioavailability studies. Am J Clin Nutr. 2005;81(1 Suppl):230S-242S. (PubMed)
- Williams RJ, Spencer JP, Rice-Evans C. Flavonoids: antioxidants or signalling molecules? Free Radic Biol Med. 2004;36(7):838-849. (PubMed)
- Kroon PA, Clifford MN, Crozier A, et al. How should we assess the effects of exposure to dietary polyphenols in vitro? Am J Clin Nutr. 2004;80(1):15-21. (PubMed)
- Heijnen CG, Haenen GR, van Acker FA, van der Vijgh WJ, Bast A. Flavonoids as peroxynitrite scavengers: the role of the hydroxyl groups. Toxicol In Vitro. 2001;15(1):3-6. (PubMed)
- Chun OK, Kim DO, Lee CY. Superoxide radical scavenging activity of the major polyphenols in fresh plums. J Agric Food Chem. 2003;51(27):8067-8072. (PubMed)
- Frei B, Higdon JV. Antioxidant activity of tea polyphenols in vivo: evidence from animal studies. J Nutr. 2003;133(10):3275S-3284S. (PubMed)
- Lotito SB, Frei B. Consumption of flavonoid-rich foods and increased plasma antioxidant capacity in humans: cause, consequence, or epiphenomenon? Free Radic Biol Med. 2006;41(12):1727-1746. (PubMed)
- Mira L, Fernandez MT, Santos M, Rocha R, Florencio MH, Jennings KR. Interactions of flavonoids with iron and copper ions: a mechanism for their antioxidant activity. Free Radic Res. 2002;36(11):1199-1208. (PubMed)
- Cheng IF, Breen K. On the ability of four flavonoids, baicilein, luteolin, naringenin, and quercetin, to suppress the Fenton reaction of the iron-ATP complex. Biometals. 2000;13(1):77-83. (PubMed)
- Spencer JP, Rice-Evans C, Williams RJ. Modulation of pro-survival Akt/protein kinase B and ERK1/2 signaling cascades by quercetin and its in vivo metabolites underlie their action on neuronal viability. J Biol Chem. 2003;278(37):34783-34793. (PubMed)
- Spencer JP, Schroeter H, Crossthwaithe AJ, Kuhnle G, Williams RJ, Rice-Evans C. Contrasting influences of glucuronidation and O-methylation of epicatechin on hydrogen peroxide-induced cell death in neurons and fibroblasts. Free Radic Biol Med. 2001;31(9):1139-1146. (PubMed)
- Hou Z, Lambert JD, Chin KV, Yang CS. Effects of tea polyphenols on signal transduction pathways related to cancer chemoprevention. Mutat Res. 2004;555(1-2):3-19. (PubMed)
- Lambert JD, Yang CS. Mechanisms of cancer prevention by tea constituents. J Nutr. 2003;133(10):3262S-3267S. (PubMed)
- Kong AN, Owuor E, Yu R, et al. Induction of xenobiotic enzymes by the MAP kinase pathway and the antioxidant or electrophile response element (ARE/EpRE). Drug Metab Rev. 2001;33(3-4):255-271. (PubMed)
- Walle UK, Walle T. Induction of human UDP-glucuronosyltransferase UGT1A1 by flavonoids-structural requirements. Drug Metab Dispos. 2002;30(5):564-569. (PubMed)
- Chen JJ, Ye ZQ, Koo MW. Growth inhibition and cell cycle arrest effects of epigallocatechin gallate in the NBT-II bladder tumour cell line. BJU Int. 2004;93(7):1082-1086. (PubMed)
- Wang W, VanAlstyne PC, Irons KA, Chen S, Stewart JW, Birt DF. Individual and interactive effects of apigenin analogs on G2/M cell-cycle arrest in human colon carcinoma cell lines. Nutr Cancer. 2004;48(1):106-114. (PubMed)
- Stewart ZA, Westfall MD, Pietenpol JA. Cell-cycle dysregulation and anticancer therapy. Trends Pharmacol Sci. 2003;24(3):139-145. (PubMed)
- Sah JF, Balasubramanian S, Eckert RL, Rorke EA. Epigallocatechin-3-gallate inhibits epidermal growth factor receptor signaling pathway. Evidence for direct inhibition of ERK1/2 and AKT kinases. J Biol Chem. 2004;279(13):12755-12762. (PubMed)
- Kavanagh KT, Hafer LJ, Kim DW, et al. Green tea extracts decrease carcinogen-induced mammary tumor burden in rats and rate of breast cancer cell proliferation in culture. J Cell Biochem. 2001;82(3):387-398. (PubMed)
- Ramos S. Effects of dietary flavonoids on apoptotic pathways related to cancer chemoprevention. J Nutr Biochem. 2007;18(7):427-442. (PubMed)
- Bagli E, Stefaniotou M, Morbidelli L, et al. Luteolin inhibits vascular endothelial growth factor-induced angiogenesis; inhibition of endothelial cell survival and proliferation by targeting phosphatidylinositol 3'-kinase activity. Cancer Res. 2004;64(21):7936-7946. (PubMed)
- Kim MH. Flavonoids inhibit VEGF/bFGF-induced angiogenesis in vitro by inhibiting the matrix-degrading proteases. J Cell Biochem. 2003;89(3):529-538. (PubMed)
- O'Leary KA, de Pascual-Tereasa S, Needs PW, Bao YP, O'Brien NM, Williamson G. Effect of flavonoids and vitamin E on cyclooxygenase-2 (COX-2) transcription. Mutat Res. 2004;551(1-2):245-254. (PubMed)
- Sakata K, Hirose Y, Qiao Z, Tanaka T, Mori H. Inhibition of inducible isoforms of cyclooxygenase and nitric oxide synthase by flavonoid hesperidin in mouse macrophage cell line. Cancer Lett. 2003;199(2):139-145. (PubMed)
- Cho SY, Park SJ, Kwon MJ, et al. Quercetin suppresses proinflammatory cytokines production through MAP kinases andNF-kappaB pathway in lipopolysaccharide-stimulated macrophage. Mol Cell Biochem. 2003;243(1-2):153-160. (PubMed)
- Steele VE, Hawk ET, Viner JL, Lubet RA. Mechanisms and applications of non-steroidal anti-inflammatory drugs in the chemoprevention of cancer. Mutat Res. 2003;523-524:137-144. (PubMed)
- Blake GJ, Ridker PM. C-reactive protein and other inflammatory risk markers in acute coronary syndromes. J Am Coll Cardiol. 2003;41(4 Suppl S):37S-42S. (PubMed)
- Choi JS, Choi YJ, Park SH, Kang JS, Kang YH. Flavones mitigate tumor necrosis factor-alpha-induced adhesion molecule upregulation in cultured human endothelial cells: role of nuclear factor-kappa B. J Nutr. 2004;134(5):1013-1019. (PubMed)
- Ludwig A, Lorenz M, Grimbo N, et al. The tea flavonoid epigallocatechin-3-gallate reduces cytokine-induced VCAM-1 expression and monocyte adhesion to endothelial cells. Biochem Biophys Res Commun. 2004;316(3):659-665. (PubMed)
- Stocker R, Keaney JF, Jr. Role of oxidative modifications in atherosclerosis. Physiol Rev. 2004;84(4):1381-1478. (PubMed)
- Anter E, Thomas SR, Schulz E, Shapira OM, Vita JA, Keaney JF, Jr. Activation of endothelial nitric-oxide synthase by the p38 MAPK in response to black tea polyphenols. J Biol Chem. 2004;279(45):46637-46643. (PubMed)
- Duffy SJ, Vita JA. Effects of phenolics on vascular endothelial function. Curr Opin Lipidol. 2003;14(1):21-27. (PubMed)
- Deana R, Turetta L, Donella-Deana A, et al. Green tea epigallocatechin-3-gallate inhibits platelet signalling pathways triggered by both proteolytic and non-proteolytic agonists. Thromb Haemost. 2003;89(5):866-874. (PubMed)
- Bucki R, Pastore JJ, Giraud F, Sulpice JC, Janmey PA. Flavonoid inhibition of platelet procoagulant activity and phosphoinositide synthesis. J Thromb Haemost. 2003;1(8):1820-1828. (PubMed)
- Hubbard GP, Wolffram S, Lovegrove JA, Gibbins JM. The role of polyphenolic compounds in the diet as inhibitors of platelet function. Proc Nutr Soc. 2003;62(2):469-478. (PubMed)
- Geleijnse JM, Launer LJ, Van der Kuip DA, Hofman A, Witteman JC. Inverse association of tea and flavonoid intakes with incident myocardial infarction: the Rotterdam Study. Am J Clin Nutr. 2002;75(5):880-886. (PubMed)
- Hertog MG, Feskens EJ, Kromhout D. Antioxidant flavonols and coronary heart disease risk. Lancet. 1997;349(9053):699. (PubMed)
- Hirvonen T, Pietinen P, Virtanen M, et al. Intake of flavonols and flavones and risk of coronary heart disease in male smokers. Epidemiology. 2001;12(1):62-67. (PubMed)
- Knekt P, Kumpulainen J, Jarvinen R, et al. Flavonoid intake and risk of chronic diseases. Am J Clin Nutr. 2002;76(3):560-568. (PubMed)
- Yochum L, Kushi LH, Meyer K, Folsom AR. Dietary flavonoid intake and risk of cardiovascular disease in postmenopausal women. Am J Epidemiol. 1999;149(10):943-949. (PubMed)
- Hertog MG, Sweetnam PM, Fehily AM, Elwood PC, Kromhout D. Antioxidant flavonols and ischemic heart disease in a Welsh population of men: the Caerphilly Study. Am J Clin Nutr. 1997;65(5):1489-1494. (PubMed)
- Rimm EB, Katan MB, Ascherio A, Stampfer MJ, Willett WC. Relation between intake of flavonoids and risk for coronary heart disease in male health professionals. Ann Intern Med. 1996;125(5):384-389. (PubMed)
- Sesso HD, Gaziano JM, Liu S, Buring JE. Flavonoid intake and the risk of cardiovascular disease in women. Am J Clin Nutr. 2003;77(6):1400-1408. (PubMed)
- Mink PJ, Scrafford CG, Barraj LM, et al. Flavonoid intake and cardiovascular disease mortality: a prospective study in postmenopausal women. Am J Clin Nutr. 2007;85(3):895-909. (PubMed)
- Lin J, Rexrode KM, Hu F, et al. Dietary intakes of flavonols and flavones and coronary heart disease in US women. Am J Epidemiol. 2007;165(11):1305-1313. (PubMed)
- Keli SO, Hertog MG, Feskens EJ, Kromhout D. Dietary flavonoids, antioxidant vitamins, and incidence of stroke: the Zutphen study. Arch Intern Med. 1996;156(6):637-642. (PubMed)
- Hirvonen T, Virtamo J, Korhonen P, Albanes D, Pietinen P. Intake of flavonoids, carotenoids, vitamins C and E, and risk of stroke in male smokers. Stroke. 2000;31(10):2301-2306. (PubMed)
- Knekt P, Isotupa S, Rissanen H, et al. Quercetin intake and the incidence of cerebrovascular disease. Eur J Clin Nutr. 2000;54(5):415-417. (PubMed)
- Liu RH. Health benefits of fruit and vegetables are from additive and synergistic combinations of phytochemicals. Am J Clin Nutr. 2003;78(3 Suppl):517S-520S. (PubMed)
- Vita JA. Tea consumption and cardiovascular disease: effects on endothelial function. J Nutr. 2003;133(10):3293S-3297S. (PubMed)
- Duffy SJ, Keaney JF, Jr., Holbrook M, et al. Short- and long-term black tea consumption reverses endothelial dysfunction in patients with coronary artery disease. Circulation. 2001;104(2):151-156. (PubMed)
- Hodgson JM, Puddey IB, Burke V, Watts GF, Beilin LJ. Regular ingestion of black tea improves brachial artery vasodilator function. Clin Sci (Lond). 2002;102(2):195-201. (PubMed)
- Stein JH, Keevil JG, Wiebe DA, Aeschlimann S, Folts JD. Purple grape juice improves endothelial function and reduces the susceptibility of LDL cholesterol to oxidation in patients with coronary artery disease. Circulation. 1999;100(10):1050-1055. (PubMed)
- Engler MB, Engler MM, Chen CY, et al. Flavonoid-rich dark chocolate improves endothelial function and increases plasma epicatechin concentrations in healthy adults. J Am Coll Nutr. 2004;23(3):197-204. (PubMed)
- Wang-Polagruto JF, Villablanca AC, Polagruto JA, et al. Chronic consumption of flavanol-rich cocoa improves endothelial function and decreases vascular cell adhesion molecule in hypercholesterolemic postmenopausal women. J Cardiovasc Pharmacol. 2006;47 Suppl 2:S177-186; discussion S206-179. (PubMed)
- Balzer J, Rassaf T, Heiss C, et al. Sustained benefits in vascular function through flavanol-containing cocoa in medicated diabetic patients a double-masked, randomized, controlled trial. J Am Coll Cardiol. 2008;51(22):2141-2149. (PubMed)
- Schroeter H, Heiss C, Balzer J, et al. (-)-Epicatechin mediates beneficial effects of flavanol-rich cocoa on vascular function in humans. Proc Natl Acad Sci U S A. 2006;103(4):1024-1029. (PubMed)
- Taubert D, Roesen R, Lehmann C, Jung N, Schomig E. Effects of low habitual cocoa intake on blood pressure and bioactive nitric oxide: a randomized controlled trial. JAMA. 2007;298(1):49-60. (PubMed)
- Freese R, Vaarala O, Turpeinen AM, Mutanen M. No difference in platelet activation or inflammation markers after diets rich or poor in vegetables, berries and apple in healthy subjects. Eur J Nutr. 2004;43(3):175-182. (PubMed)
- Janssen K, Mensink RP, Cox FJ, et al. Effects of the flavonoids quercetin and apigenin on hemostasis in healthy volunteers: results from an in vitro and a dietary supplement study. Am J Clin Nutr. 1998;67(2):255-262. (PubMed)
- Duffy SJ, Vita JA, Holbrook M, Swerdloff PL, Keaney JF, Jr. Effect of acute and chronic tea consumption on platelet aggregation in patients with coronary artery disease. Arterioscler Thromb Vasc Biol. 2001;21(6):1084-1089. (PubMed)
- Hodgson JM, Puddey IB, Burke V, Beilin LJ, Mori TA, Chan SY. Acute effects of ingestion of black tea on postprandial platelet aggregation in human subjects. Br J Nutr. 2002;87(2):141-145. (PubMed)
- Freedman JE, Parker C, 3rd, Li L, et al. Select flavonoids and whole juice from purple grapes inhibit platelet function and enhance nitric oxide release. Circulation. 2001;103(23):2792-2798. (PubMed)
- Keevil JG, Osman HE, Reed JD, Folts JD. Grape juice, but not orange juice or grapefruit juice, inhibits human platelet aggregation. J Nutr. 2000;130(1):53-56. (PubMed)
- Polagruto JA, Schramm DD, Wang-Polagruto JF, Lee L, Keen CL. Effects of flavonoid-rich beverages on prostacyclin synthesis in humans and human aortic endothelial cells: association with ex vivo platelet function. J Med Food. 2003;6(4):301-308. (PubMed)
- Innes AJ, Kennedy G, McLaren M, Bancroft AJ, Belch JJ. Dark chocolate inhibits platelet aggregation in healthy volunteers. Platelets. 2003;14(5):325-327. (PubMed)
- Rein D, Paglieroni TG, Pearson DA, et al. Cocoa and wine polyphenols modulate platelet activation and function. J Nutr. 2000;130(8S Suppl):2120S-2126S. (PubMed)
- Rein D, Paglieroni TG, Wun T, et al. Cocoa inhibits platelet activation and function. Am J Clin Nutr. 2000;72(1):30-35. (PubMed)
- Murphy KJ, Chronopoulos AK, Singh I, et al. Dietary flavanols and procyanidin oligomers from cocoa (Theobroma cacao) inhibit platelet function. Am J Clin Nutr. 2003;77(6):1466-1473. (PubMed)
- Yang CS, Yang GY, Landau JM, Kim S, Liao J. Tea and tea polyphenols inhibit cell hyperproliferation, lung tumorigenesis, and tumor progression. Exp Lung Res. 1998;24(4):629-639. (PubMed)
- Balasubramanian S, Govindasamy S. Inhibitory effect of dietary flavonol quercetin on 7,12-dimethylbenz[a]anthracene-induced hamster buccal pouch carcinogenesis. Carcinogenesis. 1996;17(4):877-879. (PubMed)
- Li ZG, Shimada Y, Sato F, et al. Inhibitory effects of epigallocatechin-3-gallate on N-nitrosomethylbenzylamine-induced esophageal tumorigenesis in F344 rats. Int J Oncol. 2002;21(6):1275-1283. (PubMed)
- Yamane T, Nakatani H, Kikuoka N, et al. Inhibitory effects and toxicity of green tea polyphenols for gastrointestinal carcinogenesis. Cancer. 1996;77(8 Suppl):1662-1667. (PubMed)
- Guo JY, Li X, Browning JD, Jr., et al. Dietary soy isoflavones and estrone protect ovariectomized ERalphaKO and wild-type mice from carcinogen-induced colon cancer. J Nutr. 2004;134(1):179-182. (PubMed)
- Huang MT, Xie JG, Wang ZY, et al. Effects of tea, decaffeinated tea, and caffeine on UVB light-induced complete carcinogenesis in SKH-1 mice: demonstration of caffeine as a biologically important constituent of tea. Cancer Res. 1997;57(13):2623-2629. (PubMed)
- Gupta S, Hastak K, Ahmad N, Lewin JS, Mukhtar H. Inhibition of prostate carcinogenesis in TRAMP mice by oral infusion of green tea polyphenols. Proc Natl Acad Sci U S A. 2001;98(18):10350-10355. (PubMed)
- Haddad AQ, Venkateswaran V, Viswanathan L, Teahan SJ, Fleshner NE, Klotz LH. Novel antiproliferative flavonoids induce cell cycle arrest in human prostate cancer cell lines. Prostate Cancer Prostatic Dis. 2006;9(1):68-76. (PubMed)
- Yamagishi M, Natsume M, Osakabe N, et al. Effects of cacao liquor proanthocyanidins on PhIP-induced mutagenesis in vitro, and in vivo mammary and pancreatic tumorigenesis in female Sprague-Dawley rats. Cancer Lett. 2002;185(2):123-130. (PubMed)
- Ross JA, Kasum CM. Dietary flavonoids: bioavailability, metabolic effects, and safety. Annu Rev Nutr. 2002;22:19-34. (PubMed)
- Goldbohm RA, Van den Brandt PA, Hertog MG, Brants HA, Van Poppel G. Flavonoid intake and risk of cancer: a prospective cohort study. Am J Epidemiol. 1995;41:s61.
- Hertog MG, Feskens EJ, Hollman PC, Katan MB, Kromhout D. Dietary flavonoids and cancer risk in the Zutphen Elderly Study. Nutr Cancer. 1994;22(2):175-184. (PubMed)
- Arts IC, Hollman PC, Bueno De Mesquita HB, Feskens EJ, Kromhout D. Dietary catechins and epithelial cancer incidence: the Zutphen elderly study. Int J Cancer. 2001;92(2):298-302. (PubMed)
- Goldbohm RA, Hertog MG, Brants HA, van Poppel G, van den Brandt PA. Consumption of black tea and cancer risk: a prospective cohort study. J Natl Cancer Inst. 1996;88(2):93-100. (PubMed)
- Arts IC, Jacobs DR, Jr., Gross M, Harnack LJ, Folsom AR. Dietary catechins and cancer incidence among postmenopausal women: the Iowa Women's Health Study (United States). Cancer Causes Control. 2002;13(4):373-382. (PubMed)
- Higdon JV, Frei B. Tea catechins and polyphenols: health effects, metabolism, and antioxidant functions. Crit Rev Food Sci Nutr. 2003;43(1):89-143. (PubMed)
- De Stefani E, Ronco A, Mendilaharsu M, Deneo-Pellegrini H. Diet and risk of cancer of the upper aerodigestive tract--II. Nutrients. Oral Oncol. 1999;35(1):22-26. (PubMed)
- Garcia-Closas R, Gonzalez CA, Agudo A, Riboli E. Intake of specific carotenoids and flavonoids and the risk of gastric cancer in Spain. Cancer Causes Control. 1999;10(1):71-75. (PubMed)
- Lagiou P, Samoli E, Lagiou A, et al. Flavonoids, vitamin C and adenocarcinoma of the stomach. Cancer Causes Control. 2004;15(1):67-72. (PubMed)
- Peterson J, Lagiou P, Samoli E, et al. Flavonoid intake and breast cancer risk: a case--control study in Greece. Br J Cancer. 2003;89(7):1255-1259. (PubMed)
- Garcia R, Gonzalez CA, Agudo A, Riboli E. High intake of specific carotenoids and flavonoids does not reduce the risk of bladder cancer. Nutr Cancer. 1999;35(2):212-214. (PubMed)
- Garcia-Closas R, Agudo A, Gonzalez CA, Riboli E. Intake of specific carotenoids and flavonoids and the risk of lung cancer in women in Barcelona, Spain. Nutr Cancer. 1998;32(3):154-158. (PubMed)
- Ramassamy C. Emerging role of polyphenolic compounds in the treatment of neurodegenerative diseases: a review of their intracellular targets. Eur J Pharmacol. 2006;545(1):51-64. (PubMed)
- Youdim KA, Qaiser MZ, Begley DJ, Rice-Evans CA, Abbott NJ. Flavonoid permeability across an in situ model of the blood-brain barrier. Free Radic Biol Med. 2004;36(5):592-604. (PubMed)
- Schmitt-Schillig S, Schaffer S, Weber CC, Eckert GP, Muller WE. Flavonoids and the aging brain. J Physiol Pharmacol. 2005;56 Suppl 1:23-36. (PubMed)
- Goyarzu P, Malin DH, Lau FC, et al. Blueberry supplemented diet: effects on object recognition memory and nuclear factor-kappa B levels in aged rats. Nutr Neurosci. 2004;7(2):75-83. (PubMed)
- Joseph JA, Denisova NA, Arendash G, et al. Blueberry supplementation enhances signaling and prevents behavioral deficits in an Alzheimer disease model. Nutr Neurosci. 2003;6(3):153-162. (PubMed)
- Joseph JA, Shukitt-Hale B, Denisova NA, et al. Reversals of age-related declines in neuronal signal transduction, cognitive, and motor behavioral deficits with blueberry, spinach, or strawberry dietary supplementation. J Neurosci. 1999;19(18):8114-8121. (PubMed)
- Patil CS, Singh VP, Satyanarayan PS, Jain NK, Singh A, Kulkarni SK. Protective effect of flavonoids against aging- and lipopolysaccharide-induced cognitive impairment in mice. Pharmacology. 2003;69(2):59-67. (PubMed)
- Laurin D, Masaki KH, Foley DJ, White LR, Launer LJ. Midlife dietary intake of antioxidants and risk of late-life incident dementia: the Honolulu-Asia Aging Study. Am J Epidemiol. 2004;159(10):959-967. (PubMed)
- White LR, Petrovitch H, Ross GW, et al. Brain aging and midlife tofu consumption. J Am Coll Nutr. 2000;19(2):242-255. (PubMed)
- de Rijk MC, Breteler MM, den Breeijen JH, et al. Dietary antioxidants and Parkinson disease. The Rotterdam Study. Arch Neurol. 1997;54(6):762-765. (PubMed)
- Engelhart MJ, Geerlings MI, Ruitenberg A, et al. Dietary intake of antioxidants and risk of Alzheimer disease. JAMA. 2002;287(24):3223-3229. (PubMed)
- Commenges D, Scotet V, Renaud S, Jacqmin-Gadda H, Barberger-Gateau P, Dartigues JF. Intake of flavonoids and risk of dementia. Eur J Epidemiol. 2000;16(4):357-363. (PubMed)
- Letenneur L, Proust-Lima C, Le Gouge A, Dartigues JF, Barberger-Gateau P. Flavonoid intake and cognitive decline over a 10-year period. Am J Epidemiol. 2007;165(12):1364-1371. (PubMed)
- Kreijkamp-Kaspers S, Kok L, Grobbee DE, et al. Effect of soy protein containing isoflavones on cognitive function, bone mineral density, and plasma lipids in postmenopausal women: a randomized controlled trial. JAMA. 2004;292(1):65-74. (PubMed)
- Casini ML, Marelli G, Papaleo E, Ferrari A, D'Ambrosio F, Unfer V. Psychological assessment of the effects of treatment with phytoestrogens on postmenopausal women: a randomized, double-blind, crossover, placebo-controlled study. Fertil Steril. 2006;85(4):972-978. (PubMed)
- Gu L, Kelm MA, Hammerstone JF, et al. Concentrations of proanthocyanidins in common foods and estimations of normal consumption. J Nutr. 2004;134(3):613-617. (PubMed)
- Hendler SS, Rorvik DR, eds. PDR for Nutritional Supplements. Montvale: Medical Economics Company, Inc; 2001.
- Shoskes DA, Zeitlin SI, Shahed A, Rajfer J. Quercetin in men with category III chronic prostatitis: a preliminary prospective, double-blind, placebo-controlled trial. Urology. 1999;54(6):960-963. (PubMed)
- Ferry DR, Smith A, Malkhandi J, et al. Phase I clinical trial of the flavonoid quercetin: pharmacokinetics and evidence for in vivo tyrosine kinase inhibition. Clin Cancer Res. 1996;2(4):659-668. (PubMed)
- Bonkovsky HL. Hepatotoxicity associated with supplements containing Chinese green tea (Camellia sinensis). Ann Intern Med. 2006;144(1):68-71. (PubMed)
- Javaid A, Bonkovsky HL. Hepatotoxicity due to extracts of Chinese green tea (Camellia sinensis): a growing concern. J Hepatol. 2006;45(2):334-335; author reply 335-336. (PubMed)
- Jatoi A, Ellison N, Burch PA, et al. A phase II trial of green tea in the treatment of patients with androgen independent metastatic prostate carcinoma. Cancer. 2003;97(6):1442-1446. (PubMed)
- Pisters KM, Newman RA, Coldman B, et al. Phase I trial of oral green tea extract in adult patients with solid tumors. J Clin Oncol. 2001;19(6):1830-1838. (PubMed)
- Chow HH, Cai Y, Hakim IA, et al. Pharmacokinetics and safety of green tea polyphenols after multiple-dose administration of epigallocatechin gallate and polyphenon E in healthy individuals. Clin Cancer Res. 2003;9(9):3312-3319. (PubMed)
- Bailey DG, Dresser GK. Interactions between grapefruit juice and cardiovascular drugs. Am J Cardiovasc Drugs. 2004;4(5):281-297. (PubMed)
- Dahan A, Altman H. Food-drug interaction: grapefruit juice augments drug bioavailability--mechanism, extent and relevance. Eur J Clin Nutr. 2004;58(1):1-9. (PubMed)
- Zhou S, Lim LY, Chowbay B. Herbal modulation of P-glycoprotein. Drug Metab Rev. 2004;36(1):57-104. (PubMed)
- Marzolini C, Paus E, Buclin T, Kim RB. Polymorphisms in human MDR1 (P-glycoprotein): recent advances and clinical relevance. Clin Pharmacol Ther. 2004;75(1):13-33. (PubMed)
- Hurrell RF, Reddy M, Cook JD. Inhibition of non-haem iron absorption in man by polyphenolic-containing beverages. Br J Nutr. 1999;81(4):289-295. (PubMed)
- Zijp IM, Korver O, Tijburg LB. Effect of tea and other dietary factors on iron absorption. Crit Rev Food Sci Nutr. 2000;40(5):371-398. (PubMed)
- Song J, Kwon O, Chen S, et al. Flavonoid inhibition of sodium-dependent vitamin C transporter 1 (SVCT1) and glucose transporter isoform 2 (GLUT2), intestinal transporters for vitamin C and Glucose. J Biol Chem. 2002;277(18):15252-15260. (PubMed)
- US Department of Agriculture. USDA database for the flavonoid content of selected foods. Available at: http://www.nal.usda.gov/fnic/foodcomp/Data/Flav/flav.html. Accessed 9/13/04.
- US Department of Agriculture. USDA database for the proanthocyanidin content of selected foods. Available at: http://www.nal.usda.gov/fnic/foodcomp/Data/PA/PA.html. Accessed 9/13/04.
- Vrhovsek U, Rigo A, Tonon D, Mattivi F. Quantitation of polyphenols in different apple varieties. J Agric Food Chem. 2004;52(21):6532-6538. (PubMed)
- Moyer RA, Hummer KE, Finn CE, Frei B, Wrolstad RE. Anthocyanins, phenolics, and antioxidant capacity in diverse small fruit: vaccinium, rubus, and ribes. J Agric Food Chem. 2002;50(3):519-525. (PubMed)
- Lee HS. Characterization of major anthocyanins and the color of red-fleshed Budd Blood orange (Citrus sinensis). J Agric Food Chem. 2002;50(5):1243-1246. (PubMed)
- Ryan JM, Revilla E. Anthocyanin composition of Cabernet Sauvignon and Tempranillo grapes at different stages of ripening. J Agric Food Chem. 2003;51(11):3372-3378. (PubMed)
- Henning SM, Fajardo-Lira C, Lee HW, Youssefian AA, Go VL, Heber D. Catechin content of 18 teas and a green tea extract supplement correlates with the antioxidant capacity. Nutr Cancer. 2003;45(2):226-235. (PubMed)
免責事項
ライナスポーリング研究所微量栄養素情報センターは、一般向けの食事要因、健康面、栄養補助食品、食品および飲料に関する科学的情報を提供する。著者および出版社は、本サイト上の医学的、心理学的、栄養学的カウンセリングサービスを利用しないことを合意した上で、本情報を利用することができる。本情報は、有資格の医療従事者または栄養士への相談の代わりとして利用することはできない。
本ウェブサイトに掲載されている食事要因、栄養補助食品、食品および飲料に含まれる情報は、実施可能なすべての使用法、行為、使用上の注意、副作用、および相互作用を網羅するものではない。本ウェブサイトは、個々の問題についての栄養学的、医学的助言をすることは意図していない。本サイトの電子的に利用可能な情報に基づく個人的な行為、または不作為に対する責任は、明示的に否認される。
本ウェブサイトにおける著作権を有する資料のいずれも、複製、修正、配布、表示、発信、実行、公開または販売をおこなってはならない。本ウェブサイトにハイパーリンクを貼ることは可能であるが、その際には以下の文言を付記することとする。
「本リンクは、オレゴン州立大学ライナスポーリング研究所の提供するウェブサイトへ移動します。<<名前>>は、オレゴン州立大学ライナスポーリング研究所のアフィリエイトではなく、認証されたリンクでもありません」