概要
- 植物ステロールとは、コレステロールに構造や機能が似た植物由来の化合物である。(詳細はこちら)
- 初期の人類の食事は1g/日くらいまで植物ステロールが豊富だったが、今日の西欧風の典型的な食事は、植物ステロールが比較的少ない。(詳細はこちら)
- 植物ステロールは腸でのコレステロール吸収を抑制する。(詳細はこちら)
- 多くの臨床試験で、少なくとも0.8gの植物性ステロールまたはスタノールを強化した食品を毎日摂取すると、血清LDLコレステロールが低下することが実証された。(詳細はこちら)
- いくつかの疫学研究で植物ステロールを含む植物性の食品を高摂取するとがんのリスクが減少するという関連がわかったが、植物性の食品に含まれる植物ステロールまたはその他の化合物が予防的要因なのかどうかは明らかでない。(詳細はこちら)
- いくつかの臨床試験の結果で、比較的低用量の植物ステロールの補給が良性前立腺過形成の尿路症状を改善することができると示唆されたが、この発見を確認するさらなる研究が必要である。(詳細はこちら)
- 植物ステロールを豊富に含む食品は、未精製の植物油、全粒穀物、ナッツ、および豆類などである。(詳細はこちら)
- 植物性ステロールまたはスタノールを添加された食品や飲料は、今では世界中の多くの国で市販されている。また、多くの国がそのような商品の健康強調表示を認めている。(詳細はこちら)
序説
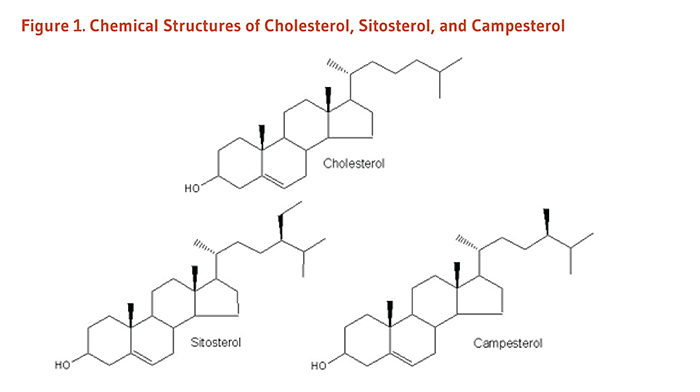
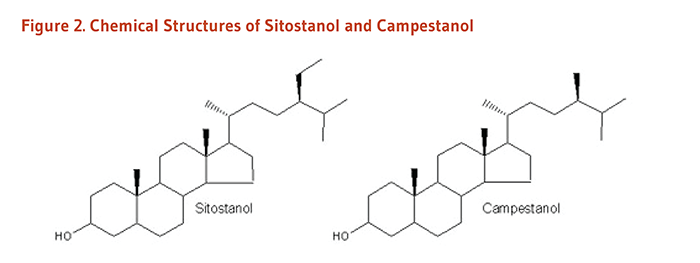
ヒトの進化の大部分で、大量の植物性食品が消費されたことであろう(1)。食物繊維や植物性タンパク質が豊富なことに加えて、我々の祖先の食事はコレステロールに似た構造と機能を持つ植物由来のステロールである植物ステロールが豊富であった。現代の食事に植物ステロールを含む植物性食品を再導入することで、血清脂質(コレステロール)プロフィールを改善し心血管疾患リスクを減少させることができるというエビデンスがどんどん増えてきている(2)。コレステロールはヒトを含む動物の体内での主要なステロールであるが、植物には様々なステロールが見られる(3)。栄養学者は2つのグループの植物ステロールを把握している。それらは(1)ステロールの環状構造部分に二重結合を持つステロール(図1参照)、および(2)ステロールの環状構造部分に二重結合がないスタノール(図2参照)である。植物やヒトの食事に最も豊富なステロールは、シトステロールとカンペステロールである。スタノールも植物には含まれるが、食事性の植物ステロール全体のわずか10%くらいでしかない。ヒトの血液や組織中のコレステロールは、食事や内因性のコレステロール合成に由来するものである。対照的に、ヒトの血液や組織中のすべての植物ステロールは食事由来である。なぜならばヒトは植物ステロールを合成できないからだ(4)。
定義
植物ステロール:植物由来のステロールやスタノールの総称。
植物性ステロールまたはスタノール:植物由来のステロールまたはスタノールに一般的に使用される用語で、これらの植物性化学物質は食品やサプリメントに添加される。
植物ステロールもしくはスタノール・エステル:脂肪酸とステロールまたはスタノールとの間にエステル結合を作ることによってエステル化した植物性ステロールまたはスタノールのこと。エステル化は腸の細胞内や工業的プロセスで起こる。エステル化は植物性ステロールやスタノールをより脂溶性にするので、マーガリンやサラダドレッシングなどの脂肪を含む食品に溶けやすくなる。本記事では、植物ステロールやスタノール・エステルの重さを、それに相当するエステル化されていないステロールやスタノールの重さで表す。
代謝と生物学的利用性
食事性コレステロールの吸収と代謝
食事性のコレステロールは、腸の内面に並ぶ細胞(腸細胞)によって吸収されるために、混合ミセルに混ざり込まなければならない(5)。混合ミセルは、脂肪を含む食事をした後に小腸で作られる胆汁塩、脂質(脂肪)、およびステロールの混合物である。腸細胞の内部では、コレステロールがエステル化されカイロミクロンとして知られる中性脂肪(トリグリセリド)が豊富なリポタンパク質に取り込まれ、これが体内を循環していく(6)。循環中のカイロミクロンから中性脂肪がなくなるにつれ、それらはカイロミクロンレムナントになり肝臓で吸収される。肝臓ではカイロミクロンレムナント由来のコレステロールが他のリポタンパク質に作り戻されて体内を循環して輸送されたり、小腸へと分泌される胆汁になったりする。
食事性植物ステロールの吸収と代謝
様々な食事には似たような量の植物ステロールとコレステロールが含まれていることが典型的であるが、ヒトでは血清植物ステロール濃度は血清コレステロール濃度よりも数百倍低いことが通常である(7)。食事性植物ステロールの10%未満が体内で吸収されるのに対して、食事性コレステロールは50~60%が吸収される(8)。コレステロールと同様に、植物ステロールも腸細胞で吸収される前に混合ミセルに組み込まれなければならない。いったん腸細胞に入ると、ABCG5とABCG8として知られるATP結合カセット(ABC)タンパク質のペアから成る排出輸送体の活性によって植物ステロールの体内吸収は阻害される(4)。ABCG5とABCG8は互いに輸送体の半分ずつを構成し、輸送体は植物ステロールと非エステル化されたコレステロールを腸細胞から腸管腔へと染み出させる。植物ステロールはABCG5/G8輸送体によってコレステロールよりもずっと多く腸に戻されるので、食事性の植物ステロールはコレステロールよりも腸での吸収がずっと少なくなる。腸細胞の内部では、植物ステロールはコレステロールほどたやすくエステル化されないので、コレステロールよりもずっと低い濃度でカイロミクロンに組み込まれる。カイロミクロンに組み込まれたこれらの植物ステロールは体内循環にのり、肝臓で吸収される。いったん肝臓内に入ってしまうと、植物ステロールは肝臓のABCG5/G8輸送体によって急速に胆汁の中に分泌される。コレステロールも胆汁に分泌されるかもしれないが、植物ステロールが胆汁に分泌される割合のほうがコレステロールの分泌よりもずっと高い(9)。したがって、植物ステロールの血清濃度がコレステロールよりも相対的に低いことは、腸での吸収が減ることと植物ステロールの胆汁への分泌が増えることで説明ができる。
生物学的活性
コレステロール吸収とリポタンパク質代謝への効果
植物性ステロールまたはスタノールを高摂取すると、ヒトの血清総LDLコレステロール濃度を減らせることはよくわかっている(「心血管疾患」の項参照)(10,11)。腸管腔では、植物ステロールは混合ミセルからコレステロールを分離しコレステロールの吸収を抑制する(12)。1.5~1.8g/日の植物性ステロールまたはスタノールの摂取で、ヒトのコレステロール吸収が30~40%減る(13,14)。より高用量(2.2g/日の植物性ステロール)では、コレステロール吸収は60%減った(15)。コレステロール吸収が減ることで、組織でのLDL受容体の発現が増え、その結果として血中のLDLの除去が進む(16)。コレステロールの吸収が減ることは、コレステロールの合成が増えることとも関連している。また、植物ステロール摂取を増加させると、ヒトの内因性コレステロール合成が増えることもわかっている(13)。植物ステロール摂取の増加によってコレステロール合成が増加するにもかかわらず、血清LDLコレステロール濃度が正味では減ることになる。
その他の生物学的活性
培養細胞や動物モデルの実験では、植物ステロールはコレステロール低下とは無関係の生物学的活性があるかもしれないことが示唆される。しかし、ヒトにおけるそれらの重要性は未知である。
細胞膜特性の変化
コレステロールは哺乳類の細胞膜の重要な構造成分である(17)。コレステロールを植物ステロールで置換すると、ガラス容器内(in vitro)では細胞膜の物性が変わることがわかっており、これはシグナル伝達または膜結合酵素の活性に影響する可能性がある「19,20)。出血性脳卒中の動物モデルからの限定的なエビデンスでは、植物性ステロールまたはスタノールを非常に多く摂取すると、赤血球の細胞膜のコレステロールが移動されて血球の変形能が下がり壊れやすくなる可能性が高くなることが示された(21,22)。しかし、植物ステロール(1g/1,000kcal)を4週間毎日補給しても、ヒトの赤血球の壊れやすさは変わらなかった(23)。
テストステロン代謝の変化
動物モデルからの限定的なエビデンスで、植物ステロールを非常に多く摂取すると、テストステロンをより強力な代謝物であるジヒドロテストステロンに変換する膜結合酵素である5αレダクターゼ(5α還元酵素、5αリダクターゼ)を抑制することによって、テストステロンの代謝が変わってしまう可能性があると示唆された(24,25)。植物ステロールの摂取がヒトでテストステロンの代謝を変えるのかどうかは不明である。1.6g/日の植物ステロールエステルを1年間摂取した男性の遊離テストステロンまたは血清総テストステロン濃度に大きな変化は見られなかった(26)。
がん細胞のアポトーシスの誘発
正常な細胞と異なり、がん細胞はアポトーシス(プログラム化された細胞死)を開始させる細胞死シグナルに反応する能力がない。培養されたヒトの前立腺がん(27)、乳がん(28)、および結腸がん(29)にシトステロールを加えると、アポトーシスを誘発することがわかっている。
抗炎症作用
培養細胞や動物研究からの限定的なデータでは、植物ステロールはマクロファージや好中球といった免疫細胞の炎症活性を減衰させるかもしれないことが示唆されている(30,31)。
疾病予防
心血管疾患
植物性ステロールまたはスタノールを強化した食品
LDLコレステロール
遊離またはエステル化された植物性ステロールまたはスタノールを強化した食品を毎日摂取することで、血清総コレステロール濃度および血清LDLコレステロール濃度が下がることが多くの臨床試験でわかっている(10,32-35)。18の対照臨床試験の結果をまとめたメタ解析で、平均2g/日の植物性ステロールまたはスタノールを含むスプレッドの摂取によって、血清LDLコレステロール濃度が9~14%下がったことがわかった(36)。23の対照臨床試験の結果をまとめたより最近のメタ解析で、平均3.4g/日の植物性ステロールまたはスタノールを含む植物性食品の摂取で、LDLコレステロール濃度が約11%減ったことがわかった(37)。別のメタ解析では、植物性ステロール強化食品の23の臨床試験および植物性スタノール強化食品の27の臨床試験の結果を別々に調べた(11)。少なくとも2g/日の用量で、植物ステロールおよびスタノールのどちらもLDLコレステロール濃度を約10%減らした。2g/日よりも高用量だと、植物性ステロールまたはスタノールのコレステロール低減効果を大きく向上させることはなかった。直近では、59の無作為化対照試験の結果を分析したメタ解析で、試験開始時のLDLコレステロール濃度が高い者の方がLDLコレステロール濃度が大きく低下したことがわかった(38)。より少ない用量の植物性ステロールまたはスタノールの研究結果では、臨床的に有意義な少なくとも5%のLDLコレステロール低下が、0.8~1.0g/日の用量で起きることが示唆された(39-43)。一般的に、植物性ステロールと植物性スタノールのコレステロール低下の効能を比べた試験では、これらはどちらも同等であるとわかった(44-46)。これらの研究では4週間よりも長く行われたものはほとんどないが、植物性ステロールおよびスタノールのコレステロール低減効果は1年までも続くことが、少なくとも2つの研究でわかった(26,47)。対照臨床試験からのデータに加えて、自由に生活している状態での植物ステロール/スタノールを強化したマーガリンの習慣的摂取について調べた5年間の研究でも、コレステロール濃度に有益な効果が見られた(48)。最近では、長期間のLDLコレステロール低減効果を維持するのに植物性ステロールはスタノールほど効果的でないのではないかという懸念が持ち上がった(49-51)。これらの懸念に対処する植物性ステロールと植物性スタノールの効能を直接比べる長期間の試験が必要である(11)。
冠動脈性心疾患のリスク
植物性ステロールまたはスタノールを強化した食品の長期摂取が冠動脈性心疾患(CHD)のリスクに与える効果は不明である。多くの介入試験の結果は、薬物治療や食事の変更による10%のLDLコレステロール低下はCHDリスクを20%も下げる可能性を示唆している(52)。米国のコレステロール教育プログラムの成人治療委員会IIIは、植物ステロールもしくはスタノール・エステル(2g/日)の摂取をLDLコレステロールが高い者への最大限の食事療法の一部に含めた(53)。飽和脂肪が少なく、果物や野菜、全粒穀物、および食物繊維が豊富な心臓に良い食事に植物性ステロールまたはスタノールを強化した食品を足すことで、CHDリスクの低減にさらに効果的になる可能性がある。たとえば、飽和脂肪を一価不飽和脂肪や多価不飽和脂肪で置き換えた食事にすると、30日後に血清LDLコレステロールが9%減ったが、同じ食事に1.7g/日の植物性ステロールを追加すると24%の減少となった(54)。より最近の結果では、植物性ステロール(1g/1,000kcal)、大豆タンパク、アーモンド、および粘性食物繊維を含むコレステロール低下食品の組み合わせの食事を1ヶ月続けると血清LDLコレステロール濃度が平均で30%低下し、これはスタチン(HMG-CoA還元酵素を抑制する薬物)によってもたらさらる低減と大きく変わらなかった(55)。しかし、1年間そのようなコレステロール低減食をした個人の解析で、LDLコレステロールの減少は平均で13%でしかなかったものの、ほぼ3分の1の参加者ではLDLコレステロール低下が20%より大きかった(56)。植物性ステロールは、観察されたコレステロール濃度の低減に寄与したこの食事の主要成分であった(57)。米国食品医薬品局(FDA)は、植物ステロールもしくはスタノール・エステルを強化した食品の定期的な摂取は心疾患のリスクを低減させるかもしれないという健康強調表示を食品のラベルに使用することを認めている(58)。
食物性植物ステロール
植物性ステロールまたはスタノールを強化した食品の毎日の摂取がLDLコレステロール濃度を大きく減らす可能性があることを発見した臨床試験は、食事に天然に含まれている植物ステロールを考慮していない(59)。血清LDLコレステロール濃度に対する食物性植物ステロール摂取の影響を考慮した研究は比較的少ない。食物性植物ステロール摂取は、様々な集団で約150~450mg/日にわたると推定されている(60)。限定的なエビデンスでは、食物性植物ステロールはコレステロールの吸収を減らすのに重要な役割を果たしているかもしれないことが示唆されている。英国での横断研究で、食物性植物ステロール摂取は、飽和脂肪や食物繊維摂取についての調整をした後ですら血清総コレステロール濃度および血清LDLコレステロール濃度と逆相関があった(61)。同様に、スウェーデンの集団の解析で、食物性植物ステロール摂取は男女の総コレステロールと女性のLDLコレステロールとの間に逆相関があることがわかった(62)。1回の食事によるテストで、コーンオイルから150mgの植物ステロールを除去すると、コレステロール吸収が38%増え(63)、小麦胚芽から328mgの植物ステロールを除去するとコレステロール吸収が43%増えた(64)。さらなる研究が必要ではあるが、これらの発見は植物性食品由来の食物性植物ステロールの摂取が心血管の健康に重大な影響がある可能性を示唆している。
がん
動物研究からの限定的なデータで、非常に多量の植物ステロール摂取、特にシトステロールの摂取は乳がんや前立腺がんの成長を抑制するかもしれないことが示唆された(65-67)。ヒトの食事性植物ステロール摂取とがんのリスクの関連を調べた疫学研究はわずかである。これは、一般的に食べられている食品の植物ステロール含有量に関するデータベースが最近になってやっと開発されてきたからである。ウルグアイでの一連の症例対照研究で、食事性植物ステロール摂取は、胃がん、肺がん、または乳がんと診断された者の方ががんのない対照群の者よりも低いことがわかった(68-70)。米国での症例対照研究で、乳がんまたは子宮内膜がん(子宮がん)と診断された女性は、がんのない女性よりも食事性植物ステロール摂取が少なかったことがわかった(71,72)。対照的に米国での別の症例対照研究では、前立腺がんと診断された男性はがんのない男性よりも食事性カンペステロール摂取が多かったことがわかったが、植物ステロール全体の摂取は前立腺がんリスクと関連がなかった(73)。植物ステロールを含む植物性食品の高摂取とがんリスクの低下との関連がわかったとする疫学研究もあるものの、その防護的要因が植物性食品の植物ステロールなのかその他の化合物なのかは不明である。
疾病治療
良性前立腺過形成(BPH)
良性前立腺過形成(BPH)は、前立腺の非がん性肥大を表す用語である。肥大化した前立腺は尿道を圧迫する可能性があり、その結果排尿が困難になる。植物ステロールの混合物(βシトステロールとして市販されている)を含む植物抽出物はしばしば、BPHに関連する泌尿器症状のための薬草療法に含まれる。しかし、BPHの症状のある男性に対する植物ステロールサプリメントの効能を調べた対照試験は比較的少ない。BPHの症状のある200人の男性による6ヶ月間の研究で、60mg/日のβシトステロール剤によってプラセボに比べて症状のスコアが改善し、最大尿流が増え、排尿後残尿量が減った(74)。追跡研究で、βシトステロールによる治療を続けた38人の参加者でこれらの改善が18ヶ月まで維持されたと報告された(75)。同様にBPHの症状のある177人の男性による6ヶ月の研究で、130mg/日の別のβシトステロール剤によってプラセボより症状のスコアが改善し、最大尿流が増え、排尿後残尿量が減った(76)。これらとその他の2つの対照臨床試験の結果をまとめたシステマティックレビュー(系統的総括)で、βシトステロール抽出物は最大尿流を平均で3.9ml/秒増やし、排尿後残尿量を平均で29ml減らしたことがわかった(77)。いくつかの臨床試験の結果から、比較的低用量の植物ステロールがBPHに関連する下部尿路の症状を改善する可能性があるということが示唆されるが、これらの結果を確認するさらなる研究が必要である(78)。
摂取源
食品
今日のほとんどの先進国での典型的な食事と異なり、我々の祖先の食事は植物ステロールが豊富で、おそらく1,000mg/日も含まれていたであろう(1)。今日の食物性植物ステロール摂取は、集団によって150~450mg/日とばらつくであろうと推定される(3)。菜食主義者、特に完全菜食主義者は一般的に食物性植物ステロール摂取が最も多い(79)。植物ステロールはすべての植物性食品に含まれるが、最も多いのは植物油、ナッツ油、およびオリーブ油などの未精製植物油である(3)。ナッツ、種子、全粒穀物、および豆類も植物ステロールの良好な食品源である(5)。いくつかの食品の植物ステロール含有量を表1に示す。特定の食品についての栄養素含有量については、米国農務省の食品成分データベースを参照のこと。
| 食品 | 分量 | 植物ステロール(mg) |
|---|---|---|
| 小麦胚芽 | 約120ml(57g) | 197 |
| こめ油(米糠油) | 大さじ1(14g) | 162 |
| ごま油 | 大さじ1(14g) | 102 |
| コーン油 | 大さじ1(14g) | 117 |
| キャノーラ油 | 大さじ1(14g) | 92 |
| ピーナッツ | 約28g | 62 |
| 小麦ふすま | 約120ml(29g) | 58 |
| アーモンド | 約28g | 39 |
| 芽キャベツ | 約120ml(78g) | 34 |
| ライ麦パン | 2切れ(64g) | 33 |
| マカデミアナッツ | 約28g | 33 |
| オリーブ油 | 大さじ1(14g) | 22 |
| Take Control(登録商標)スプレッド | 大さじ1(14g) | 1,650mgの植物ステロールエステル(1,000mgの遊離ステロール) |
| Benecol(登録商標)スプレッド | 大さじ1(14g) | 850mgの植物ステロールエステル(500mgの遊離ステロール) |
植物性ステロールおよび植物性スタノールを強化した食品
コレステロール低減効果を実証した臨床試験の大部分では、マーガリンやマヨネーズのような脂肪を含む食品に溶かした植物性ステロールもしくはスタノール・エステルが使用された(11)。より最近の研究で、植物性ステロールまたはスタノールを適切に溶かせば低脂肪または無脂肪の食品ですらそれらを効果的に体に届けることができることが示された(10,59)。低脂肪ヨーグルト(43,84-86)、低脂肪乳(87-89)低脂肪チーズ(90)、ビターチョコレート(91)、およびオレンジジュース(92,93)に添加された植物性ステロールまたはスタノールが、対照臨床試験でLDLコレステロールを低下させたことが報告された。マーガリン、マヨネーズ、植物油、サラダドレッシング、ヨーグルト、牛乳、豆乳、オレンジジュース、棒状のスナック菓子、および肉などの植物性ステロールまたはスタノールを添加した様々な食品が、米国、ヨーロッパ、アジア、オーストラリア、およびニュージーランドで市販されている(10)。最近のメタ解析で、スプレッド、マヨネーズ、サラダドレッシング、牛乳、またはヨーグルトに添加された植物性ステロール/スタノールは、チョコレート、オレンジジュース、チーズ、肉、および棒状のシリアル菓子などのその他の製品に加えられる場合よりも、LDLコレステロール濃度を低下させるのにより効果的であったことがわかった(38)。LDLコレステロールを低下させるのに効果的な用量は最大で2g/日(11)、最少で0.8~1.0g/日(10)であることが、今までの研究から示される。コレステロール低減効果を実証した臨床試験の大半では、1日分の用量の植物性ステロールまたはスタノールを2~3回の食事に分けていたが、これはLDLコレステロール低減により効果的かもしれない(38)。しかし、1日分の植物性ステロールまたはスタノールを1回の食事で摂取しても、いくつかの臨床試験ではLDLコレステロールが下がったことがわかった(43,85,86,94,95)。
サプリメント
βシトステロールとして市販されている植物ステロールのサプリメントは、米国では処方箋なしで入手可能である。60~130mg/日のβシトステロールが良性前立腺過形成(BPH)の症状を軽減することが、いくつかの臨床試験でわかっている(「良性前立腺過形成」の項参照)。0.5gの植物ステロールを含む噛むソフトカプセル(ゲル)が、2g/日の推奨量でコレステロール低下に効くとして市販されている。植物ステロールのサプリメントは、脂肪を含む食事と一緒に摂取すべきである。
安全性
米国では、様々な食製品に添加された植物性ステロールやスタノールは、FDAによって一般的に安全であると認められている(GRAS認証)(96)。またEUの食品科学委員会は、様々な食製品に添加された植物性ステロールやスタノールはヒトが摂取しても安全であると結論づけた(97)。しかしながら委員会は、食製品からの植物性ステロールやスタノールの摂取は3g/日を超えるべきではないと推奨している。なぜならこれより多く摂取しても健康への有益性のエビデンスがないことと、高摂取による望ましくない効果があるかもしれないからである。
悪影響
植物性ステロールまたはスタノールを1年間まで定期的に摂取しても、それに関連する悪影響はほとんどない。1.6g/日の植物性ステロールを強化したスプレッドを摂取した者は、対照となるスプレッドを1年間まで摂取した者と比べても何の悪影響も報告しなかった(26)。また1.8~2.6g/日の植物スタノールを強化したスプレッドを1年間まで摂取した者も、何の悪影響も報告しなかった(47)。マーガリンに含まれる最大8.6g/日までの植物ステロールを3~4週間摂取しても健康な男女には良好な耐用性があり、腸内細菌や女性ホルモン濃度に悪い影響を及ぼすことはなかった(98)。植物ステロールは通常良好な耐用性が見られるが、吐き気、消化不良、下痢、および便秘が時として報告されることもあった(74,76)。
シトステロール血症(フィトステロール血症)
シトステロール血症はフィトステロール血症としても知られ、ABCG5またはABCG8遺伝子のどちらのコピーにも起こる突然変異を受け継ぐことによって起こる非常に稀な遺伝性疾患である(99)。どちらかの輸送タンパク質の突然変異がホモ接合である個人は、腸での植物ステロール吸収が増え胆汁中への排出が減ることで、血清植物ステロール濃度が劇的に高くなる。血清コレステロール濃度が正常またはやや高くても、シトステロール血症の個人は早発性アテローム性動脈硬化のリスクが高い。シトステロール血症の個人は、植物性ステロールが添加された食品またはサプリメントを避けるべきである(10)。より一般的であるシトステロール血症のヘテロ接合保因者における植物性ステロール摂取の効果が、2つの研究で調べられた。2人のヘテロ接合保因者が3g/日の植物性ステロール摂取を4週間(100)しても、12人のヘテロ接合保因者が2.2g/日の植物性ステロールを6~12週間摂取しても、血清植物ステロール濃度が異常に高くなることはなかった(101)。
妊娠と授乳
食品やサプリメントに添加された植物性ステロールまたはスタノールは、妊婦や授乳婦への安全性が研究されていないので、妊婦や授乳婦に勧められない(10)。現在、菜食主義者の女性のように天然の植物ステロールを食事で高摂取しても、妊娠や授乳に悪影響があるというエビデンスはない。
薬物相互作用
植物性ステロールまたはスタノールのコレステロール低減効果は、HMG-CoA還元酵素阻害薬(スタチン)の効果を補足するかもしれない(102,103)。対照臨床試験の結果では、スタチンを治療に使用している個人が2~3g/日の植物性ステロールまたはスタノールを摂取すると、LDLコレステロールがさらに7~11%減少するかもしれないことが示唆されていて、これはスタチンの用量を2倍にすることに匹敵する(50,104-106)。抗凝固作用のためにワルファリン(クマジンまたはコウマディン)を使用している患者が4.5g/日のスタノールエステルを8週間摂取しても、プロトロンビン時間(INR)に影響はなかった(107)。
栄養素との相互作用
脂溶性ビタミン(ビタミンA,D,E,K)
植物性ステロールやスタノールがコレステロールの吸収を減らし血清LDLコレステロール濃度を下げることから、脂溶性ビタミンの状態に対するその効果も臨床試験で研究された。血漿ビタミンA(レチノール)濃度は、植物性ステロールもしくはスタノール・エステルを1年まで摂取しても影響がなかった(11,26)。血漿ビタミンD(25ヒドロキシビタミンD3)濃度には大部分の研究で何の変化もなかったが、1つのプラセボ対照試験で1.6g/日のステロールエステルを1年間摂取した個人に血漿25ヒドロキシビタミンD3濃度に小さい(7%)が統計的に有意義な減少が見られた(26)。ビタミンKの状態に植物性ステロールまたはスタノール摂取が悪影響するというエビデンスはほとんどない。1.6g/日のステロールエステルを6ヶ月間摂取したら血漿ビタミンK濃度が取るに足らない14%の減少になったという関連があったが、ビタミンKの状態の機能的指標であるカルボキシル化されたオステオカルシンには影響がなかった(26)。より短期間のその他の研究では、植物ステロールやスタノール・エステルの摂取は、ビタミンK1(108,109)、またはビタミンK依存性凝固因子(110)の血漿濃度に大きく影響しなかった。植物性ステロールまたはスタノールを強化した食品の摂取は、多くの研究で血漿ビタミンE(α-トコフェロール)濃度を減少させるとわかっている。しかし、α-トコフェロールの濃度をLDLコレステロール濃度に標準化した場合には、これらの減少は一般的にそれほどでもない。このことは、観察された血漿α-トコフェロール濃度の減少が一部にはその担体リポタンパク質であるLDLコレステロールの減少によるものであるということを示唆している。一般に、1.5g/日以上の植物性ステロールやスタノールを強化した食品の摂取は、栄養状態のよい集団では脂溶性ビタミンの栄養状態に悪影響を及ぼさないことがわかっている。
カロテノイド
食事性のカロテノイドはリポタンパク質で循環する脂溶性植物化学物質である。多くの研究で、植物性ステロールまたはスタノールを強化した食品の短期または長期の摂取後に、10~20%の血漿カロテノイド濃度の減少が観察された(11)。血清総コレステロール濃度またはLDLコレステロール濃度に標準化された場合でも、αカロテン、βカロテン、およびリコピンの減少は持続するかもしれない。このことは、植物ステロールがこれらのカロテノイドの吸収を妨げる可能性があることを示唆している(111)。血漿カロテノイド濃度の減少が健康リスクをもたらすのかどうか不明であるが、いくつかの研究でカロテノイドの豊富な果物や野菜の摂取を増やすと、植物ステロールによる血漿カロテノイドの減少を防げる可能性があることがわかった(112)。あるケースでは、カロテノイドの豊富な野菜1食分を含む5食分の果物や野菜を毎日摂取するようにすると、2.5g/日の植物ステロールもしくはスタノール・エステルを摂取する者の血漿カロテノイド濃度を維持するのに十分であった(113)。
Authors and Reviewers
Originally written in 2005 by:
Jane Higdon, Ph.D.
Linus Pauling Institute
Oregon State University
Updated in September 2008 by:
Victoria J. Drake, Ph.D.
Linus Pauling Institute
Oregon State University
Reviewed in September 2008 by:
Peter J.H. Jones, Ph.D.
Professor of Nutrition
Director, Mary Emily Clinical Nutrition Research Center
School of Dietetics and Human Nutrition
McGill University
Copyright 2005-2026 Linus Pauling Institute
Figure Alternative Text
Figure 1. Chemical structures of cholesterol, sitosterol, and campesterol
The figure shows the chemical structures of cholesterol, sitosterol, and campesterol.
Figure 2. Chemical structures of sitostanol and campestanol
The figure shows the chemical structures of two plant-derived stanols: sitostanol and campestanol.
References
- Jenkins DJ, Kendall CW, Marchie A, et al. The Garden of Eden--plant based diets, the genetic drive to conserve cholesterol and its implications for heart disease in the 21st century. Comp Biochem Physiol A Mol Integr Physiol. 2003;136(1):141-151. (PubMed)
- Kendall CW, Jenkins DJ. A dietary portfolio: maximal reduction of low-density lipoprotein cholesterol with diet. Curr Atheroscler Rep. 2004;6(6):492-498. (PubMed)
- Ostlund RE, Jr. Phytosterols in human nutrition. Annu Rev Nutr. 2002;22:533-549. (PubMed)
- Sudhop T, Lutjohann D, von Bergmann K. Sterol transporters: targets of natural sterols and new lipid lowering drugs. Pharmacol Ther. 2005;105(3):333-341. (PubMed)
- de Jong A, Plat J, Mensink RP. Metabolic effects of plant sterols and stanols (Review). J Nutr Biochem. 2003;14(7):362-369. (PubMed)
- Plat J, Mensink RP. Plant stanol and sterol esters in the control of blood cholesterol levels: mechanism and safety aspects. Am J Cardiol. 2005;96(1 Suppl):15-22. (PubMed)
- von Bergmann K, Sudhop T, Lutjohann D. Cholesterol and Plant Sterol Absorption: Recent Insights. Am J Cardiol. 2005;96(1S):10-14. (PubMed)
- Ostlund RE, Jr., McGill JB, Zeng CM, et al. Gastrointestinal absorption and plasma kinetics of soy Delta(5)-phytosterols and phytostanols in humans. Am J Physiol Endocrinol Metab. 2002;282(4):E911-916. (PubMed)
- Sudhop T, Sahin Y, Lindenthal B, et al. Comparison of the hepatic clearances of campesterol, sitosterol, and cholesterol in healthy subjects suggests that efflux transporters controlling intestinal sterol absorption also regulate biliary secretion. Gut. 2002;51(6):860-863. (PubMed)
- Berger A, Jones PJ, Abumweis SS. Plant sterols: factors affecting their efficacy and safety as functional food ingredients. Lipids Health Dis. 2004;3(1):5. (PubMed)
- Katan MB, Grundy SM, Jones P, Law M, Miettinen T, Paoletti R. Efficacy and safety of plant stanols and sterols in the management of blood cholesterol levels. Mayo Clin Proc. 2003;78(8):965-978. (PubMed)
- Nissinen M, Gylling H, Vuoristo M, Miettinen TA. Micellar distribution of cholesterol and phytosterols after duodenal plant stanol ester infusion. Am J Physiol Gastrointest Liver Physiol. 2002;282(6):G1009-1015. (PubMed)
- Jones PJ, Raeini-Sarjaz M, Ntanios FY, Vanstone CA, Feng JY, Parsons WE. Modulation of plasma lipid levels and cholesterol kinetics by phytosterol versus phytostanol esters. J Lipid Res. 2000;41(5):697-705. (PubMed)
- Normen L, Dutta P, Lia A, Andersson H. Soy sterol esters and beta-sitostanol ester as inhibitors of cholesterol absorption in human small bowel. Am J Clin Nutr. 2000;71(4):908-913. (PubMed)
- Richelle M, Enslen M, Hager C, et al. Both free and esterified plant sterols reduce cholesterol absorption and the bioavailability of beta-carotene and alpha-tocopherol in normocholesterolemic humans. Am J Clin Nutr. 2004;80(1):171-177. (PubMed)
- Plat J, Mensink RP. Effects of plant stanol esters on LDL receptor protein expression and on LDL receptor and HMG-CoA reductase mRNA expression in mononuclear blood cells of healthy men and women. FASEB J. 2002;16(2):258-260. (PubMed)
- Mouritsen OG, Zuckermann MJ. What's so special about cholesterol? Lipids. 2004;39(11):1101-1113. (PubMed)
- Halling KK, Slotte JP. Membrane properties of plant sterols in phospholipid bilayers as determined by differential scanning calorimetry, resonance energy transfer and detergent-induced solubilization. Biochim Biophys Acta. 2004;1664(2):161-171. (PubMed)
- Awad AB, Chen YC, Fink CS, Hennessey T. beta-Sitosterol inhibits HT-29 human colon cancer cell growth and alters membrane lipids. Anticancer Res. 1996;16(5A):2797-2804. (PubMed)
- Leikin AI, Brenner RR. Fatty acid desaturase activities are modulated by phytosterol incorporation in microsomes. Biochim Biophys Acta. 1989;1005(2):187-191. (PubMed)
- Ratnayake WM, L'Abbe MR, Mueller R, et al. Vegetable oils high in phytosterols make erythrocytes less deformable and shorten the life span of stroke-prone spontaneously hypertensive rats. J Nutr. 2000;130(5):1166-1178. (PubMed)
- Ratnayake WM, Plouffe L, L'Abbe MR, Trick K, Mueller R, Hayward S. Comparative health effects of margarines fortified with plant sterols and stanols on a rat model for hemorrhagic stroke. Lipids. 2003;38(12):1237-1247. (PubMed)
- Jones PJ, Raeini-Sarjaz M, Jenkins DJ, et al. Effects of a diet high in plant sterols, vegetable proteins, and viscous fibers (dietary portfolio) on circulating sterol levels and red cell fragility in hypercholesterolemic subjects. Lipids. 2005;40(2):169-174. (PubMed)
- Awad AB, Hartati MS, Fink CS. Phytosterol feeding induces alteration in testosterone metabolism in rat tissues. J Nutr Biochem. 1998;9(12):712-717.
- Cabeza M, Bratoeff E, Heuze I, Ramirez E, Sanchez M, Flores E. Effect of beta-sitosterol as inhibitor of 5 alpha-reductase in hamster prostate. Proc West Pharmacol Soc. 2003;46:153-155. (PubMed)
- Hendriks HF, Brink EJ, Meijer GW, Princen HM, Ntanios FY. Safety of long-term consumption of plant sterol esters-enriched spread. Eur J Clin Nutr. 2003;57(5):681-692. (PubMed)
- von Holtz RL, Fink CS, Awad AB. beta-Sitosterol activates the sphingomyelin cycle and induces apoptosis in LNCaP human prostate cancer cells. Nutr Cancer. 1998;32(1):8-12. (PubMed)
- Awad AB, Roy R, Fink CS. Beta-sitosterol, a plant sterol, induces apoptosis and activates key caspases in MDA-MB-231 human breast cancer cells. Oncol Rep. 2003;10(2):497-500. (PubMed)
- Choi YH, Kong KR, Kim YA, et al. Induction of Bax and activation of caspases during beta-sitosterol-mediated apoptosis in human colon cancer cells. Int J Oncol. 2003;23(6):1657-1662. (PubMed)
- Awad AB, Toczek J, Fink CS. Phytosterols decrease prostaglandin release in cultured P388D1/MAB macrophages. Prostaglandins Leukot Essent Fatty Acids. 2004;70(6):511-520. (PubMed)
- Navarro A, De las Heras B, Villar A. Anti-inflammatory and immunomodulating properties of a sterol fraction from Sideritis foetens Clem. Biol Pharm Bull. 2001;24(5):470-473. (PubMed)
- St-Onge MP, Jones PJ. Phytosterols and human lipid metabolism: efficacy, safety, and novel foods. Lipids. 2003;38(4):367-375. (PubMed)
- Moruisi KG, Oosthuizen W, Opperman AM. Phytosterols/stanols lower cholesterol concentrations in familial hypercholesterolemic subjects: a systematic review with meta-analysis. J Am Coll Nutr. 2006;25(1):41-48. (PubMed)
- Ellegard LH, Andersson SW, Normen AL, Andersson HA. Dietary plant sterols and cholesterol metabolism. Nutr Rev. 2007;65(1):39-45. (PubMed)
- Van Horn L, McCoin M, Kris-Etherton PM, et al. The evidence for dietary prevention and treatment of cardiovascular disease. J Am Diet Assoc. 2008;108(2):287-331. (PubMed)
- Law M. Plant sterol and stanol margarines and health. BMJ. 2000;320(7238):861-864. (PubMed)
- Chen JT, Wesley R, Shamburek RD, Pucino F, Csako G. Meta-analysis of natural therapies for hyperlipidemia: plant sterols and stanols versus policosanol. Pharmacotherapy. 2005;25(2):171-183. (PubMed)
- AbuMweis SS, Barake R, Jones P. Plant sterols/stanols as cholesterol lowering agents: A meta-analysis of randomized controlled trials. Food & Nutrition Research. 2008; DOI: 10.3402/fnr.v52i0.1811. (PubMed)
- Hendriks HF, Weststrate JA, van Vliet T, Meijer GW. Spreads enriched with three different levels of vegetable oil sterols and the degree of cholesterol lowering in normocholesterolaemic and mildly hypercholesterolaemic subjects. Eur J Clin Nutr. 1999;53(4):319-327. (PubMed)
- Miettinen TA, Vanhanen H. Dietary sitostanol related to absorption, synthesis and serum level of cholesterol in different apolipoprotein E phenotypes. Atherosclerosis. 1994;105(2):217-226. (PubMed)
- Pelletier X, Belbraouet S, Mirabel D, et al. A diet moderately enriched in phytosterols lowers plasma cholesterol concentrations in normocholesterolemic humans. Ann Nutr Metab. 1995;39(5):291-295. (PubMed)
- Sierksma A, Weststrate JA, Meijer GW. Spreads enriched with plant sterols, either esterified 4,4-dimethylsterols or free 4-desmethylsterols, and plasma total- and LDL-cholesterol concentrations. Br J Nutr. 1999;82(4):273-282. (PubMed)
- Volpe R, Niittynen L, Korpela R, et al. Effects of yoghurt enriched with plant sterols on serum lipids in patients with moderate hypercholesterolaemia. Br J Nutr. 2001;86(2):233-239. (PubMed)
- Hallikainen MA, Sarkkinen ES, Gylling H, Erkkila AT, Uusitupa MI. Comparison of the effects of plant sterol ester and plant stanol ester-enriched margarines in lowering serum cholesterol concentrations in hypercholesterolaemic subjects on a low-fat diet. Eur J Clin Nutr. 2000;54(9):715-725. (PubMed)
- Vanstone CA, Raeini-Sarjaz M, Parsons WE, Jones PJ. Unesterified plant sterols and stanols lower LDL-cholesterol concentrations equivalently in hypercholesterolemic persons. Am J Clin Nutr. 2002;76(6):1272-1278. (PubMed)
- Weststrate JA, Meijer GW. Plant sterol-enriched margarines and reduction of plasma total- and LDL-cholesterol concentrations in normocholesterolaemic and mildly hypercholesterolaemic subjects. Eur J Clin Nutr. 1998;52(5):334-343. (PubMed)
- Miettinen TA, Puska P, Gylling H, Vanhanen H, Vartiainen E. Reduction of serum cholesterol with sitostanol-ester margarine in a mildly hypercholesterolemic population. N Engl J Med. 1995;333(20):1308-1312. (PubMed)
- Wolfs M, de Jong N, Ocke MC, Verhagen H, Monique Verschuren WM. Effectiveness of customary use of phytosterol/-stanol enriched margarines on blood cholesterol lowering. Food Chem Toxicol. 2006;44(10):1682-1688. (PubMed)
- Miettinen TA, Gylling H. Plant stanol and sterol esters in prevention of cardiovascular diseases. Ann Med. 2004;36(2):126-134. (PubMed)
- O'Neill FH, Brynes A, Mandeno R, et al. Comparison of the effects of dietary plant sterol and stanol esters on lipid metabolism. Nutr Metab Cardiovasc Dis. 2004;14(3):133-142. (PubMed)
- O'Neill FH, Sanders TA, Thompson GR. Comparison of efficacy of plant stanol ester and sterol ester: short-term and longer-term studies. Am J Cardiol. 2005;96(1A):29D-36D. (PubMed)
- National Cholesterol Education Program. Third Report of the National Cholesterol Education Program Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III). National Heart Lung and Blood Institute, National Institutes of Health. 2002. http://www.nhlbi.nih.gov/guidelines/cholesterol/atp3_rpt.htm.
- Grundy SM. Stanol Esters as a Component of Maximal Dietary Therapy in the National Cholesterol Education Program Adult Treatment Panel III Report. Am J Cardiol. 2005;96(1 Suppl):47-50. (PubMed)
- Jones PJ, Ntanios FY, Raeini-Sarjaz M, Vanstone CA. Cholesterol-lowering efficacy of a sitostanol-containing phytosterol mixture with a prudent diet in hyperlipidemic men. Am J Clin Nutr. 1999;69(6):1144-1150. (PubMed)
- Jenkins DJ, Kendall CW, Marchie A, et al. Direct comparison of a dietary portfolio of cholesterol-lowering foods with a statin in hypercholesterolemic participants. Am J Clin Nutr. 2005;81(2):380-387. (PubMed)
- Jenkins DJ, Kendall CW, Faulkner DA, et al. Assessment of the longer-term effects of a dietary portfolio of cholesterol-lowering foods in hypercholesterolemia. Am J Clin Nutr. 2006;83(3):582-591. (PubMed)
- Jenkins DJ, Kendall CW, Nguyen TH, et al. Effect of plant sterols in combination with other cholesterol-lowering foods. Metabolism. 2008;57(1):130-139. (PubMed)
- Food and Drug Administration. Health claims: plant sterol/stanol esters and risk of coronary heart disease (CHD). US Government Printing Office. 2002. Available at: http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/cfrsearch.cfm?fr=101.83. Accessed 3/3/15.
- Ostlund RE, Jr. Phytosterols and cholesterol metabolism. Curr Opin Lipidol. 2004;15(1):37-41. (PubMed)
- Ostlund RE, Jr., Racette SB, Stenson WF. Effects of trace components of dietary fat on cholesterol metabolism: phytosterols, oxysterols, and squalene. Nutr Rev. 2002;60(11):349-359. (PubMed)
- Andersson SW, Skinner J, Ellegard L, et al. Intake of dietary plant sterols is inversely related to serum cholesterol concentration in men and women in the EPIC Norfolk population: a cross-sectional study. Eur J Clin Nutr. 2004;58(10):1378-1385. (PubMed)
- Klingberg S, Ellegard L, Johansson I, et al. Inverse relation between dietary intake of naturally occurring plant sterols and serum cholesterol in northern Sweden. Am J Clin Nutr. 2008;87(4):993-1001. (PubMed)
- Ostlund RE, Jr., Racette SB, Okeke A, Stenson WF. Phytosterols that are naturally present in commercial corn oil significantly reduce cholesterol absorption in humans. Am J Clin Nutr. 2002;75(6):1000-1004. (PubMed)
- Ostlund RE, Jr., Racette SB, Stenson WF. Inhibition of cholesterol absorption by phytosterol-replete wheat germ compared with phytosterol-depleted wheat germ. Am J Clin Nutr. 2003;77(6):1385-1389. (PubMed)
- Ju YH, Clausen LM, Allred KF, Almada AL, Helferich WG. beta-Sitosterol, beta-Sitosterol Glucoside, and a Mixture of beta-Sitosterol and beta-Sitosterol Glucoside Modulate the Growth of Estrogen-Responsive Breast Cancer Cells In Vitro and in Ovariectomized Athymic Mice. J Nutr. 2004;134(5):1145-1151. (PubMed)
- Awad AB, Fink CS, Williams H, Kim U. In vitro and in vivo (SCID mice) effects of phytosterols on the growth and dissemination of human prostate cancer PC-3 cells. Eur J Cancer Prev. 2001;10(6):507-513. (PubMed)
- Awad AB, Downie A, Fink CS, Kim U. Dietary phytosterol inhibits the growth and metastasis of MDA-MB-231 human breast cancer cells grown in SCID mice. Anticancer Res. 2000;20(2A):821-824. (PubMed)
- De Stefani E, Boffetta P, Ronco AL, et al. Plant sterols and risk of stomach cancer: a case-control study in Uruguay. Nutr Cancer. 2000;37(2):140-144. (PubMed)
- Mendilaharsu M, De Stefani E, Deneo-Pellegrini H, Carzoglio J, Ronco A. Phytosterols and risk of lung cancer: a case-control study in Uruguay. Lung Cancer. 1998;21(1):37-45. (PubMed)
- Ronco A, De Stefani E, Boffetta P, Deneo-Pellegrini H, Mendilaharsu M, Leborgne F. Vegetables, fruits, and related nutrients and risk of breast cancer: a case-control study in Uruguay. Nutr Cancer. 1999;35(2):111-119. (PubMed)
- McCann SE, Freudenheim JL, Marshall JR, Brasure JR, Swanson MK, Graham S. Diet in the epidemiology of endometrial cancer in western New York (United States). Cancer Causes Control. 2000;11(10):965-974. (PubMed)
- McCann SE, Freudenheim JL, Marshall JR, Graham S. Risk of human ovarian cancer is related to dietary intake of selected nutrients, phytochemicals and food groups. J Nutr. 2003;133(6):1937-1942. (PubMed)
- Strom SS, Yamamura Y, Duphorne CM, et al. Phytoestrogen intake and prostate cancer: a case-control study using a new database. Nutr Cancer. 1999;33(1):20-25. (PubMed)
- Berges RR, Windeler J, Trampisch HJ, Senge T. Randomised, placebo-controlled, double-blind clinical trial of beta-sitosterol in patients with benign prostatic hyperplasia. Beta-sitosterol Study Group. Lancet. 1995;345(8964):1529-1532. (PubMed)
- Berges RR, Kassen A, Senge T. Treatment of symptomatic benign prostatic hyperplasia with beta-sitosterol: an 18-month follow-up. BJU Int. 2000;85(7):842-846. (PubMed)
- Klippel KF, Hiltl DM, Schipp B. A multicentric, placebo-controlled, double-blind clinical trial of beta-sitosterol (phytosterol) for the treatment of benign prostatic hyperplasia. German BPH-Phyto Study group. Br J Urol. 1997;80(3):427-432. (PubMed)
- Wilt TJ, MacDonald R, Ishani A. beta-sitosterol for the treatment of benign prostatic hyperplasia: a systematic review. BJU Int. 1999;83(9):976-983. (PubMed)
- Dreikorn K. The role of phytotherapy in treating lower urinary tract symptoms and benign prostatic hyperplasia. World J Urol. 2002;19(6):426-435. (PubMed)
- Nair PP, Turjman N, Kessie G, et al. Diet, nutrition intake, and metabolism in populations at high and low risk for colon cancer. Dietary cholesterol, beta-sitosterol, and stigmasterol. Am J Clin Nutr. 1984;40(4 Suppl):927-930. (PubMed)
- US Department of Agriculture, Agricultural Research Service. USDA Nutrient Database for Standard Reference, Release 20. 2007. Available at: http://www.nal.usda.gov/fnic/foodcomp/search/. Accessed 7/24/08.
- Normen L, Bryngelsson S, Johnsson M, et al. The phytosterol content of some cereal foods commonly consumed in Sweden and in the Netherlands. J Food Compos Anal. 2002;15(6):693-704.
- Normen L, Johnsson M, Andersson H, van Gameren Y, Dutta P. Plant sterols in vegetables and fruits commonly consumed in Sweden. Eur J Nutr. 1999;38(2):84-89. (PubMed)
- Phillips KM, Ruggio DM, Toivo JI, Swank MA, Simpkins AH. Free and esterified sterol composition of edible oils and fats. J Food Compos Anal. 2002;15(2):123-142.
- Mensink RP, Ebbing S, Lindhout M, Plat J, van Heugten MM. Effects of plant stanol esters supplied in low-fat yoghurt on serum lipids and lipoproteins, non-cholesterol sterols and fat soluble antioxidant concentrations. Atherosclerosis. 2002;160(1):205-213. (PubMed)
- Plana N, Nicolle C, Ferre R, et al. Plant sterol-enriched fermented milk enhances the attainment of LDL-cholesterol goal in hypercholesterolemic subjects. Eur J Nutr. 2008;47(1):32-39. (PubMed)
- Doornbos AM, Meynen EM, Duchateau GS, van der Knaap HC, Trautwein EA. Intake occasion affects the serum cholesterol lowering of a plant sterol-enriched single-dose yoghurt drink in mildly hypercholesterolaemic subjects. Eur J Clin Nutr. 2006;60(3):325-333. (PubMed)
- Noakes M, Clifton PM, Doornbos AME, Trautwein EA. Plant sterol ester-enriched milk and yoghurt effectively reduce serum cholesterol in modestly hypercholesterolemic subjects. Eur J Clin Nutr. 2005;44(4):214-222. (PubMed)
- Thomsen AB, Hansen HB, Christiansen C, Green H, Berger A. Effect of free plant sterols in low-fat milk on serum lipid profile in hypercholesterolemic subjects. Eur J Clin Nutr. 2004;58(6):860-870. (PubMed)
- Seppo L, Jauhiainen T, Nevala R, Poussa T, Korpela R. Plant stanol esters in low-fat milk products lower serum total and LDL cholesterol. Eur J Nutr. 2007;46(2):111-117. (PubMed)
- Jauhiainen T, Salo P, Niittynen L, Poussa T, Korpela R. Effects of low-fat hard cheese enriched with plant stanol esters on serum lipids and apolipoprotein B in mildly hypercholesterolaemic subjects. Eur J Clin Nutr. 2006;60(11):1253-1257. (PubMed)
- Allen RR, Carson L, Kwik-Uribe C, Evans EM, Erdman JW, Jr. Daily consumption of a dark chocolate containing flavanols and added sterol esters affects cardiovascular risk factors in a normotensive population with elevated cholesterol. J Nutr. 2008;138(4):725-731. (PubMed)
- Devaraj S, Jialal I, Vega-Lopez S. Plant sterol-fortified orange juice effectively lowers cholesterol levels in mildly hypercholesterolemic healthy individuals. Arterioscler Thromb Vasc Biol. 2004;24(3):e25-28. (PubMed)
- Devaraj S, Autret BC, Jialal I. Reduced-calorie orange juice beverage with plant sterols lowers C-reactive protein concentrations and improves the lipid profile in human volunteers. Am J Clin Nutr. 2006;84(4):756-761. (PubMed)
- Matvienko OA, Lewis DS, Swanson M, et al. A single daily dose of soybean phytosterols in ground beef decreases serum total cholesterol and LDL cholesterol in young, mildly hypercholesterolemic men. Am J Clin Nutr. 2002;76(1):57-64. (PubMed)
- Plat J, van Onselen EN, van Heugten MM, Mensink RP. Effects on serum lipids, lipoproteins and fat soluble antioxidant concentrations of consumption frequency of margarines and shortenings enriched with plant stanol esters. Eur J Clin Nutr. 2000;54(9):671-677. (PubMed)
- Food and Drug Administration. GRAS Notice No. GRN 000112. 2003. http://www.fda.gov/Food/IngredientsPackagingLabeling/GRAS/NoticeInventory/ucm153924.htm. Accessed 3/3/15.
- Scientific Committee on Food. Opinion on Applications for Approval of a Variety of Plant Sterol-Enriched Foods. 2003. Available at: http://ec.europa.eu/food/fs/sc/scf/out174_en.pdf.
- Ayesh R, Weststrate JA, Drewitt PN, Hepburn PA. Safety evaluation of phytosterol esters. Part 5. Faecal short-chain fatty acid and microflora content, faecal bacterial enzyme activity and serum female sex hormones in healthy normolipidaemic volunteers consuming a controlled diet either with or without a phytosterol ester-enriched margarine. Food Chem Toxicol. 1999;37(12):1127-1138. (PubMed)
- Berge KE. Sitosterolemia: a gateway to new knowledge about cholesterol metabolism. Ann Med. 2003;35(7):502-511. (PubMed)
- Stalenhoef AF, Hectors M, Demacker PN. Effect of plant sterol-enriched margarine on plasma lipids and sterols in subjects heterozygous for phytosterolaemia. J Intern Med. 2001;249(2):163-166. (PubMed)
- Kwiterovich PO, Jr., Chen SC, Virgil DG, Schweitzer A, Arnold DR, Kratz LE. Response of obligate heterozygotes for phytosterolemia to a low-fat diet and to a plant sterol ester dietary challenge. J Lipid Res. 2003;44(6):1143-1155. (PubMed)
- Normen L, Holmes D, Frohlich J. Plant sterols and their role in combined use with statins for lipid lowering. Curr Opin Investig Drugs. 2005;6(3):307-316. (PubMed)
- Thompson GR. Additive effects of plant sterol and stanol esters to statin therapy. Am J Cardiol. 2005;96(1 Suppl):37-39. (PubMed)
- Blair SN, Capuzzi DM, Gottlieb SO, Nguyen T, Morgan JM, Cater NB. Incremental reduction of serum total cholesterol and low-density lipoprotein cholesterol with the addition of plant stanol ester-containing spread to statin therapy. Am J Cardiol. 2000;86(1):46-52. (PubMed)
- Neil HA, Meijer GW, Roe LS. Randomised controlled trial of use by hypercholesterolaemic patients of a vegetable oil sterol-enriched fat spread. Atherosclerosis. 2001;156(2):329-337. (PubMed)
- Simons LA. Additive effect of plant sterol-ester margarine and cerivastatin in lowering low-density lipoprotein cholesterol in primary hypercholesterolemia. Am J Cardiol. 2002;90(7):737-740. (PubMed)
- Nguyen TT, Dale LC. Plant stanol esters and vitamin K. Mayo Clin Proc. 1999;74(6):642-643. (PubMed)
- Raeini-Sarjaz M, Ntanios FY, Vanstone CA, Jones PJ. No changes in serum fat-soluble vitamin and carotenoid concentrations with the intake of plant sterol/stanol esters in the context of a controlled diet. Metabolism. 2002;51(5):652-656. (PubMed)
- Korpela R, Tuomilehto J, Hogstrom P, et al. Safety aspects and cholesterol-lowering efficacy of low fat dairy products containing plant sterols. Eur J Clin Nutr. 2006;60(5):633-642. (PubMed)
- Plat J, Mensink RP. Vegetable oil based versus wood based stanol ester mixtures: effects on serum lipids and hemostatic factors in non-hypercholesterolemic subjects. Atherosclerosis. 2000;148(1):101-112. (PubMed)
- Plat J, Mensink RP. Effects of diets enriched with two different plant stanol ester mixtures on plasma ubiquinol-10 and fat-soluble antioxidant concentrations. Metabolism. 2001;50(5):520-529. (PubMed)
- Ntanios FY, Duchateau GS. A healthy diet rich in carotenoids is effective in maintaining normal blood carotenoid levels during the daily use of plant sterol-enriched spreads. Int J Vitam Nutr Res. 2002;72(1):32-39. (PubMed)
- Noakes M, Clifton P, Ntanios F, Shrapnel W, Record I, McInerney J. An increase in dietary carotenoids when consuming plant sterols or stanols is effective in maintaining plasma carotenoid concentrations. Am J Clin Nutr. 2002;75(1):79-86. (PubMed)
免責事項
ライナスポーリング研究所微量栄養素情報センターは、一般向けの食事要因、健康面、栄養補助食品、食品および飲料に関する科学的情報を提供する。著者および出版社は、本サイト上の医学的、心理学的、栄養学的カウンセリングサービスを利用しないことを合意した上で、本情報を利用することができる。本情報は、有資格の医療従事者または栄養士への相談の代わりとして利用することはできない。
本ウェブサイトに掲載されている食事要因、栄養補助食品、食品および飲料に含まれる情報は、実施可能なすべての使用法、行為、使用上の注意、副作用、および相互作用を網羅するものではない。本ウェブサイトは、個々の問題についての栄養学的、医学的助言をすることは意図していない。本サイトの電子的に利用可能な情報に基づく個人的な行為、または不作為に対する責任は、明示的に否認される。
本ウェブサイトにおける著作権を有する資料のいずれも、複製、修正、配布、表示、発信、実行、公開または販売をおこなってはならない。本ウェブサイトにハイパーリンクを貼ることは可能であるが、その際には以下の文言を付記することとする。
「本リンクは、オレゴン州立大学ライナスポーリング研究所の提供するウェブサイトへ移動します。<<名前>>は、オレゴン州立大学ライナスポーリング研究所のアフィリエイトではなく、認証されたリンクでもありません」