要約
- レスベラトロールは、ぶどう、赤ワイン、紫色のぶどうジュース、ピーナッツ、およびある種のベリー類に含まれるポリフェノール化合物である。(詳細はこちら)
- 経口摂取すると、レスベラトロールはヒトでの吸収が良いように見える。しかし急速に代謝され体外に排出されるため、その生物学的利用性は比較的低い。(詳細はこちら)
- 赤ワインに含まれることが報告され、「フレンチ・パラドックス」を説明しやすいのではないかという憶測から、レスベラトロールの潜在的な健康有益性に関心が持たれた。(詳細はこちら)
- 適度なアルコール摂取は冠動脈心疾患のリスクを20~30%下げるという一貫した相関があるが、赤ワイン中のレスベラトロールなどのポリフェノールがさらにリスク低減をもたらすか否かは未だに不明である。(詳細はこちら)
- レスベラトロールはある動物モデルのがん細胞や培養したがん細胞の成長を抑制することができるが、レスベラトロールの大量摂取がヒトのがんを予防できるか否かはわかっていない。(詳細はこちら)
- 酵母、蠕虫、ショウジョウバエ、魚、および高カロリー食のマウスの寿命がレスベラトロールの投与で延びたものの、ヒトで同様の効果があるかは不明である。(詳細はこちら)
- 現在では、人体におけるレスベラトロールの効果はよくわかっていない。
序説
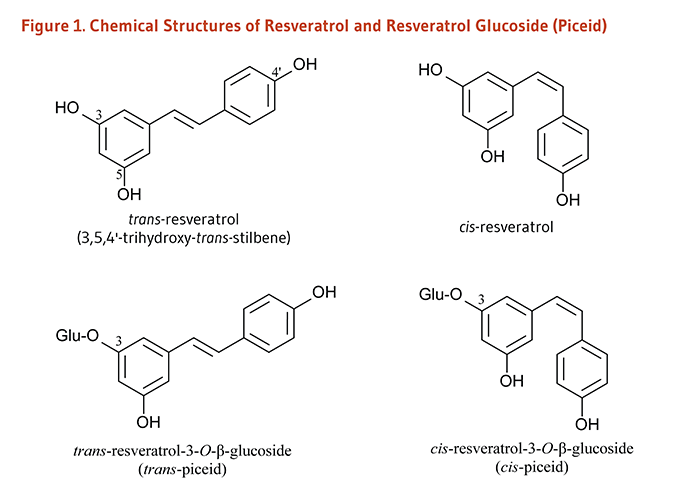
レスベラトロール(3,4',5-トリヒドロキシスチルベン)は、スチルベンと呼ばれるポリフェノール化合物の一種である(1)。ある種の植物は、ストレス、傷、真菌感染、または紫外線などに反応して、レスベラトロールやその他のスチルベンを生成する(2)。レスベラトロールは脂溶性化合物で、トランス型とシス型がある(図1参照)。シス型およびトランス型のどちらも、グルコシド(ブドウ糖分子に結合したもの)としても存在する。レスベラトロール-3-O-(β)グルコシドはピセイドと呼ばれる(3)。1992年に赤ワインに含まれることが最初に報告され(4)、「フレンチ・パラドックス」(下の「心血管疾患」の項目参照)を説明しやすくするのではないかという憶測から、レスベラトロールの潜在的な健康有益性に関心が持たれた。最近では、レスベラトロールががんの発生を抑制(5)し、培養した細胞や動物モデルの寿命を延ばす(6)可能性についての報告に関心が集まっている。
代謝と生物学的利用性
トランス型レスベラトロールは、経口摂取するとヒトでの吸収が良いように見える。しかし急速に代謝され体外に排出されるため、その生物学的利用性は比較的低い(7,8)。レスベラトロールの代謝物は、トランス型レスベラトロールを経口摂取した場合に主に検出される。トランス型レスベラトロール25mgを6人の健康な男女が経口摂取したところ、代謝されていないレスベラトロールの痕跡のみが血漿に検出された。レスベラトロールとその代謝物の血漿濃度は、60分ほどして約2マイクロモル/リットル(491マイクログラム/リットル)の最高値になった(7)。12人の健康な男性がトランス型レスベラトロールを体重70kgあたり25mg経口投与された研究では、レスベラトロールとその代謝物の血清濃度は投与後30分で最高値になった。レスベラトロール全体(レスベラトロールとその代謝物)の濃度は416~471マイクログラム/リットルの範囲で、レスベラトロールがワイン、野菜ジュース、またはぶどうジュースのいずれの形態で投与されたかによって違った(9)。レスベラトロールのグルコシド(ピセイド)を主に含むぶどうジュースからのレスベラトロールの生物学的利用性は、トランス型レスベラトロールよりもさらに低い可能性が別の研究結果から示されている(10)。最近の研究では、食事(低脂肪または高脂肪)と一緒にワインを摂取しても空腹で摂取しても、赤ワインのトランス型レスベラトロールの生物学的利用性に違いはないと報告されている(11)。
ヒトでのレスベラトロールの生物学的利用性に関する情報は重要である。なぜなら、レスベラトロールに関する基礎的な研究の多くは、経口摂取後のヒトの血漿での最高濃度よりもしばしば10~100倍も高いような代謝されていないレスベラトロールにさらされた培養細胞においてなされてきたからである(12)。消化管の内壁の細胞は代謝されていないレスベラトロールにさらされるが、ヒトでの研究はその他の組織が主にレスベラトロールの代謝物にさらされることを示唆している。レスベラトロール代謝物の生物活性についてはほとんどわかっていないし、レスベラトロール代謝物をレスベラトロールにまた転換できる組織があるのか不明である(7)。
生物活性
直接的酸化防止活性
試験管内では、レスベラトロールはフリーラジカル(遊離基)やその他のオキシダント(酸化物質)を効果的に除去(中和)(13)し、低比重リポタンパク質(LDL)の酸化を抑制する(14,15)。しかし、レスベラトロールが生体内で重要な抗酸化物質であるというエビデンス(根拠)はほとんどない(16)。レスベラトロールの経口摂取では、ヒトにおけるレスベラトロールの体内循環中の濃度および細胞内濃度は、ビタミンC、尿酸、ビタミンE、およびグルタチオンといったその他の重要な抗酸化物質よりもずっと低いようである。加えて、体内循環しているレスベラトロールの大部分を占めるレスベラトロール代謝物の抗酸化活性は、レスベラトロールより低いかもしれない。
エストロゲン性および抗エストロゲン性活性
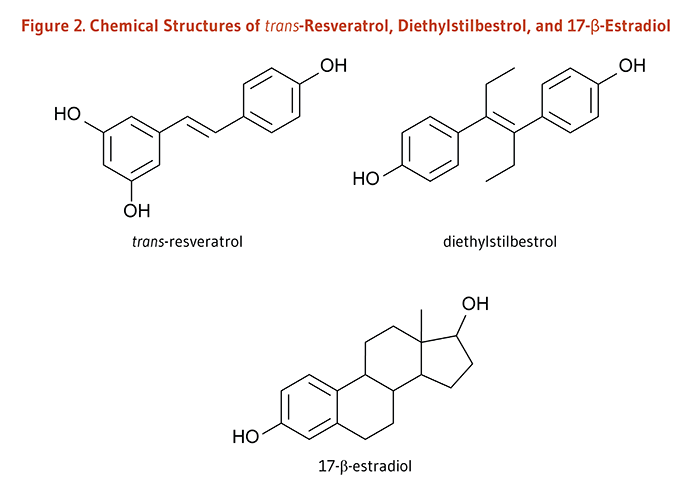
内在性エストロゲンはヒトおよびその他の哺乳類が合成するステロイドホルモンで、細胞内のエストロゲン受容体と結合する。エストロゲンとその受容体の複合体はDNAの非反復配列(エストロゲン応答配列;ERE)と相互作用し、エストロゲン応答性遺伝子の発現を調整する(17)。エストロゲン受容体と結びつき内在性エストロゲンと同様の反応を誘発する化合物は、エストロゲン作動薬とみなされる。一方でエストロゲン受容体と結合はするが内在性エストロゲンによって誘発される反応を防止したり抑制したりする化合物は、エストロゲン拮抗薬とみなされる。レスベラトロールの化学構造は合成エストロゲン作動薬であるジエチルスチルベストロールと非常に似通っており(図2参照)、レスベラトロールがエストロゲン作動薬として機能する可能性を示唆している。しかしながら、培養細胞での実験では、レスベラトロールはある条件下でエストロゲン作動薬として働き、その他の条件下ではエストロゲン拮抗薬として機能する(18,19)。エストロゲン受容体陽性の乳がん細胞では、レスベラトロールは内在性エストロゲンである17β-エストラジオールがない場合にエストロゲン作動薬として機能し、17β-エストラジオールがある場合にはエストロゲン拮抗薬として機能した(20,21)。現時点では、細胞のタイプ、エストロゲン受容体のイソ型(ERαまたはERβ)、および内在性エストロゲンの存在などの要素によって、エストロゲン作動薬または拮抗薬として作用する可能性があるようである(17)。
がん予防に関連する生物活性
生体内変換酵素への効果
ある種の化合物は、体内でチトクロームP450酵素によって代謝されるまで発がん性を持たない(2)。あるチトクロームP450酵素の発現および活動を抑制することで(22,23)、レスベラトロールはこれらの活性化された発がん性物質への接触を減らしてがんを予防することに役立っているのかもしれない。対照的に、第II相生体内変換酵素(第II相代謝酵素)の活動を増進することは、有毒または発がんの可能性のある化学物質の排泄を一般的に促す。レスベラトロールは、培養細胞において第II相代謝酵素であるNAD(P)H、つまりキノンレダクターゼ(キノン還元酵素)の発現と活性を増進することがわかっている(5,24)。
通常の細胞周期制御の保全
DNA損傷の後、DNA修復またはその損傷が修復不能であるならば細胞死(アポトーシス)に至る経路の活性化へと、細胞周期が過渡的に抑止される(25)。細胞周期制御に欠陥があると、がんの発現に寄与する突然変異の伝播に陥りかねない。レスベラトロールは、培養されたがん細胞に添加されると、細胞周期抑止を誘発することがわかっている(26)。
増殖の抑制とアポトーシスの誘発
正常な細胞と異なり、がん細胞は急速に増殖し、アポトーシスを起こす細胞死信号に反応しない。レスベラトロールは多くのがん細胞株で増殖を抑制し、細胞死を誘発することがわかっている(2,27で再調査)。
腫瘍浸潤の抑制と血管新生
がん細胞は、マトリックスメタロプロテアーゼ(マトリックスメタロプロテイナーゼ)という酵素の助成によって、正常な組織を浸潤する。レスベラトロールは、少なくとも1種類のマトリックスメタロプロテアーゼの活動を抑制することがわかっている(28)。急激な増殖を促進するため、浸潤がんは血管新生というプロセスによって新しい血管も作らねばならない。レスベラトロールは、ガラス容器内では血管新生を抑制することがわかっている(29-31)。
抗炎症効果
炎症は細胞増殖や血管新生を促し、アポトーシスを抑制する(32)。レスベラトロールは、ガラス容器内でシクロオキシゲナーゼやリポキシゲナーゼを含むいくつかの炎症酵素の活動を抑制することがわかっている(33,34)。レスベラトロールはNFkBまたはAP-1といった炎症誘発性転写因子も抑制する可能性がある(35,36)。
心血管疾患予防に関連する生物活性
血管細胞癒着分子の発現の抑制
アテローム性動脈硬化は現在では炎症性疾患と認識されており、炎症に関するいくつかの測定値は心筋梗塞のリスク上昇と関連している(37)。アテローム性動脈硬化の発生初期の事象の一つが、炎症を起こす白血球が血液から動脈壁に血管細胞癒着分子によって動員されることである(38)。レスベラトロールは、培養された内皮細胞において癒着分子が発現するのを抑制することがわかっている(39,40)。
血管平滑筋細胞増殖の抑制
血管平滑筋細胞の増殖は、動脈硬化の進行に重要な役割を果たす(41)。レスベラトロールは培養された血管平滑筋細胞の増殖を抑制することがわかっている(42,43)。
内皮性一酸化窒素合成酵素(eNOS)の活動の刺激
eNOSは血管内皮細胞による一酸化窒素(NO)生成の触媒作用を起こす酵素である。一酸化窒素は動脈弛緩(血管拡張)の維持に必要であり、一酸化窒素依存性血管拡張がうまくいかないと、心血管疾患のリスクが高くなる(44)。レスベラトロールは、培養された内皮細胞でeNOSの活動を刺激することがわかっている(45,46)。
血小板凝縮の抑制
血小板凝縮は、冠状動脈や大脳動脈をつまらせる可能性のある血栓形成の第一段階の一つであり、それぞれ心筋梗塞および脳卒中に至る。レスベラトロールは、ガラス容器内で血小板凝縮を抑制することがわかっている(47,48)。
注意:上記の生命活動の多くは、レスベラトロールを経口摂取したヒトの体内よりも高いであろう濃度でレスベラトロールを投与して培養した細胞で見られたものであるということを覚えておくことが大切である(上記の「代謝と生物学的利用性」の項目を参照)。
疾病の予防
心血管疾患
赤ワインのポリフェノール
心血管疾患リスクの大幅な減少は、適度なアルコール飲料の摂取と関連している(49,50)。比較的高レベルの食事性飽和脂肪摂取および喫煙にもかかわらず冠動脈心疾患による死亡率がフランスで比較的低いという「フレンチ・パラドックス」から、定期的に赤ワインを摂取することが心血管疾患への付加的な予防になっているのではないかという考えが導かれた(51,52)。赤ワインはレスベラトロールや、それ以上の濃度のフラボノイドを含む。これらのポリフェノール化合物は、試験管内やアテローム性動脈硬化の動物モデルで、抗酸化効果、抗炎症効果、およびその他の潜在的アテローム産生抑制効果を示す(53)。しかしながら、赤ワインのポリフェノール摂取を増加させると、そのアルコール含有量に関連した以上に付加的な心血管疾患予防効果があるのかどうかは不明である(「アルコール飲料」の記事を参照のこと)。この問題を扱った疫学的研究の結果はまちまちである。いくつかの大規模前向き研究では、ワインを飲む者はビールや蒸留酒を飲む者よりも心血管疾患のリスクが低い(54-56)となっているが、何の差も見られなかった研究もある(57-59)。ワインを好む者とビールや蒸留酒を好む者との社会経済的な差異およびライフスタイルの違いで、いくつかの研究で見られた付加的な効果の一部が説明できるのかもしれない。ワインを好む者は、その他のアルコール飲料を好む者より高収入、高学歴、低喫煙、および果物や野菜の高摂取と飽和脂肪の低摂取の傾向があることがいくつかの研究でわかっている(59-64)。適度なアルコール摂取では一貫して冠動脈心疾患リスクが20~30%低下するが、赤ワインのポリフェノールが付加的なリスク低下をもたらすのかどうかは不明である。興味深いことに、げっ歯類にアルコールを含まない赤ワインを与える研究では、心血管疾患に関連する様々なパラメータの値に向上が見られた(65,66)。さらに、ヒトでのプラセボ対照研究では、赤ぶどうのポリフェノール抽出物を与えられた心臓病患者に内皮機能の急激な改善が見られた(67)。しかしながら、赤ワインを飲むことがそのアルコール含有量に由来する以上に心血管に有益であるのかどうかを決定するには、さらなる研究が必要である。
レスベラトロール
レスベラトロールは、血小板凝縮の抑制(47,48,68)、一酸化窒素の生成を促すことでの血管拡張の促進(46,69)、および炎症を起こす酵素の抑制(34,70,71)など、心臓を保護する可能性のあるいくつかの効果をガラス容器内では発揮することがわかっている。しかしながら、これらの効果を引き起こすのに必要なレスベラトロールの濃度は、レスベラトロールを経口摂取した後のヒトの血漿での濃度よりも高いことが多い(7)。いくつかの動物研究の結果は、レスベラトロールの高用量経口摂取が血栓症(凝血塊の形成)リスクおよびアテローム性動脈硬化症リスクを低減させる可能性を示唆している(72,73)。しかし少なくとも1つの研究では、レスベラトロールを与えられた動物にアテローム性動脈硬化が増えた(74)。赤ワインにレスベラトロールが含まれることは、レスベラトロールが心血管疾患を防ぐ可能性について多大な興味をいだかせるものではある。しかし、レスベラトロールにヒトの心臓保護効果があるという説得力のあるエビデンスはなく、グラスに1~2杯の赤ワインに含まれる量くらいではなおさらである(「摂取源」の項目参照)。
がん
レスベラトロールは、乳がん、前立腺がん、胃がん、大腸がん、すい臓がん、および甲状腺がんなどのヒトの様々ながん細胞株の増殖を抑制することがわかっている(2)。動物モデルでは、発がん性化学物質によって引き起こされた食道がん(75)、腸がん(72)、および乳がん(20,77)の発生が、レスベラトロールの経口投与で抑制された。しかしながら、タバコの煙に含まれる発がん性物質による肺がん発生の抑制には、レスベラトロールの経口投与は効果がなかった(78,79)。遺伝的に大腸がんにかかりやすくしたマウスにレスベラトロールを経口投与した効果はまちまちである(80,81)。また、発がん性物質である1,2ジメチルヒドラジンを投与したラット(ネズミ)の大腸がん発生が、レスベラトロールの経口投与で予防されたとする研究もある(82-84)。レスベラトロールの高摂取がヒトのがん予防に役立つかは不明である。この問題を扱い、レスベラトロールががんの治療にも有益か否かも決定する臨床試験が現在進行中である(85)。ヒトでのレスベラトロールの代謝に関する研究では、レスベラトロールを多量に食事で摂取しても、培養細胞の研究で見られた予防効果を実現する組織濃度まで上がらないのではないかということが示唆されている(7,12)。
長寿
カロリー制限は、哺乳類を含む多くの種で寿命を延ばすことが知られている(86)。酵母では、カロリー制限がSir2という酵素の活動を刺激する(87)。カロリー制限なしで酵母にレスベラトロールを供与するとSir2の活動が増え、酵母の複製的寿命が70%延びた(6)。レスベラトロールの供与は、同様のメカニズムで蠕虫(線虫)やショウジョウバエ(キイロショウジョウバエ)の寿命を延ばした(88)。加えて、レスベラトロールは脊椎動物である魚(ノソブランキウス・フルゼリ)の寿命を、投与量に従って延ばした(89)。しかしながら、より高度な動物でレスベラトロールが同様の効果を持っているかは不明である。最近の研究で、標準的な食事を与えられたマウスと同様なくらいに、レスベラトロールが高カロリー食のマウスの寿命を延ばしたと報告されている(90)。レスベラトロールは、ヒトの相同な酵素(Sirt1)の活動を試験管内で増やす(6)が、レスベラトロールがヒトの寿命を延ばすかは不明である。しかも、ヒトでSirt1の活動を増やすためのレスベラトロール濃度は、経口摂取のあとでヒトの血漿で測定される濃度よりもかなり高い。興味深いことに、最近のマウスでの加齢研究で、低用量の食事性レスベラトロールが、カロリー制限によって引き起こされるのと同様に心臓、脳、および骨格筋で遺伝子発現を変化させることがわかった(91)。カロリー制限と同様に、この研究ではレスベラトロールが加齢に関連する心臓機能低下を鈍らせた。これらの発見がヒトにも当てはまるかどうかを決定するには、臨床試験が必要であろう。
摂取源
食物の摂取源
レスベラトロールは、ぶどう、ワイン、ぶどうジュース、ピーナッツ、およびブルーベリー、ビルベリー、クランベリーといったスノキ属のベリー類に含まれる(92-94)。ぶどうでは、レスベラトロールは皮にのみ含まれる(95)。ぶどうの皮のレスベラトロール量は、ぶどうの栽培品種、原産地、および真菌感染の有無などで異なる(96)。ぶどうの皮と接する発酵時間の長さが、ワインのレスベラトロール含有量を決めるのに重要である。したがって、白ワインやロゼワインは、一般的に赤ワインよりもレスベラトロール含有量が少ない(4)。赤色または紫色のぶどうジュースは、レスベラトロールの優良な摂取源となりうる(3)。ぶどうやぶどうジュースでの主要なレスベラトロールの形態は、トランス型レスベラトロールグルコシド(トランスピセイド)である。しかし、ワインは発酵による糖の切断の結果と思われるレスベラトロールアグリコンも多量に含んでいる(92)。多くのワインは、発酵で生成されるかビニフェリン(レスベラトロールの重合体)から発生するであろうシス型のレスベラトロール(図1参照)も多く含む(97)。赤ワインはレスベラトロールを比較的豊富に含む摂取源であるが、レスベラトロール以外のポリフェノールもかなり高濃度に含む(「フラボノイド」の記事を参照)(98)。いくつかの飲料や食物に含まれるレスベラトロールの全含有量を下の表に示す。食物や飲料に含まれるレスベラトロールの含有量はかなり幅があるので、これらの値は近似値と見なされるべきである。
| 飲料 | 全レスベラトロール量(mg/リットル) | 約140mlのグラス1杯分の全レスベラトロール量(mg) |
|---|---|---|
| 白ワイン(スペイン産) | 0.05-1.80 | 11.9 |
| ロゼワイン(スペイン産) | 0.43-3.52 | 0.06-0.53 |
| 赤ワイン(スペイン産) | 1.92-12.59 | 0.29-1.89 |
| 赤ワイン(全体) | 1.98-7.13 | 0.30-1.07 |
| 赤ぶどうジュース(スペイン産) | 1.14-8.69 | 0.17-1.30 |
| 食品 | 分量 | 全レスベラトロール量(mg) |
|---|---|---|
| ピーナッツ(生) | 146 g | 0.01-0.26 |
| ピーナッツ(ゆでたもの) | 180 g | 0.32-1.28 |
| ピーナッツバター | 258 g | 0.04-0.13 |
| 赤ぶどう | 160 g | 0.24-1.25 |
サプリメント
米国で入手可能なたいていのレスベラトロールのサプリメントは、別名が虎杖根というイタドリの根の抽出物を含む(102)。米国では、レスベラトロールやその他のポリフェノールを含む赤ワインや赤ぶどうの抽出物が、栄養補助食品として入手可能である。レスベラトロールのサプリメントは10~50mgのレスベラトロールを含むであろうが、ヒトの慢性的疾患の予防に有効な用量は不明である。
安全性
悪影響
レスベラトロールのヒトへの有害性や悪影響は知られていないが、今日まで対照臨床試験が少ない。レスベラトロールの経口摂取の安全性を10人の治験者で評価した最近の試験では、1回5グラムまでの服用でも重大な悪影響がなかった(103)。ラットでは、体重1kg換算で300mgまでの用量のトランス型レスベラトロールを毎日4週間経口投与しても、明瞭な悪影響はなかった(104,105)。
妊娠期および授乳期
レスベラトロールを含むサプリメントの妊娠期および授乳期での安全性は確立していない(102)。どの妊娠段階でもアルコール摂取の安全な量が確立していないため(106)、妊娠中の女性はレスベラトロールの摂取源としてワインを飲むことは避けるべきである。
エストロゲン感受性のがん
ヒトにおけるレスベラトロールのエストロゲン様作用についてもっと多くのことがわかるまで、乳がん、卵巣がん、および子宮がんといったエストロゲン感受性のがんの病歴のある女性は、レスベラトロールのサプリメントの摂取を避けるべきである(上記の「エストロゲン性および抗エストロゲン性活性」の項目を参照)。
薬物相互作用
抗凝固薬および血小板凝集抑制薬
レスベラトロールは、ガラス容器内でヒトの血小板凝集を抑制することが知られている(48,107)。理論的には、(サプリメントなどからの)レスベラトロールの高摂取は、ワルファリン(クマジン)などの抗凝固薬、クロピドグレル(プラビックス)やジピリダモール(ペルサンチン)などの血小板凝集抑制薬、およびアスピリン、イブプロフェン、およびその他の抗炎症薬(NSAID)と一緒の服用で出血のリスクを高める。
チトクロームP450 3A4によって代謝される薬物
レスベラトロールは、ガラス容器内でチトクローム(シトクローム)P450 3A4(CYP3A4)の活動を抑制することが報告されている(108,109)。この相互作用はヒトでは報告されていないが、(サプリメントなどからの)レスベラトロールの高摂取は、理論的にはCYP3A4による広範な初回通過代謝を受ける薬物の生物学的利用性や有毒性を高める可能性がある。CYP3A4により代謝される薬物は、HMG-CoA還元酵素抑制薬(アトルバスタチン、ロバスタチン、およびシンバスタチン)、カルシウムチャンネル拮抗薬(フェロジピン、ニカルジピン、ニフェジピン、ニソルジピン、ニトレンジピン、ニモジピン、およびベラパミル)、抗不整脈薬(アミオダロン)、HIVプロテアーゼ阻害薬(サキナビル)、免疫抑制剤(シクロスポリンおよびタクロリムス)、抗ヒスタミン薬(テルフェナジン)、ベンゾジアゼピン(ミダゾラムおよびトリアゾラム)、および勃起不全の治療薬(シルデナフィル)などを含むが、これらに限らない。
Authors and Reviewers
Originally written in 2005 by:
Jane Higdon, Ph.D.
Linus Pauling Institute
Oregon State University
Updated in May 2008 by:
Victoria J. Drake, Ph.D.
Linus Pauling Institute
Oregon State University
Reviewed in May 2008 by:
William P. Steward, M.D., Ph.D.
Professor of Oncology
Co-Director of Cancer Biomarkers and Prevention Group
Department of Oncology
University of Leicester
Copyright 2005-2026 Linus Pauling Institute
Figure Alternative Text
Figure 1. Chemical structures of resveratrol and resveratrol glucoside (piceid)
The figure shows the chemical structures of trans-resveratrol (3,5,4’-trihydroxy-trans-stilbene), cis-resveratrol, trans-resveratrol-3-O-β-glucoside (trans-piceid), and cis-resveratrol-3-O-β-glucoside (cis-piceid).
Figure 2. Chemical structures of trans-resveratrol, diethylstilbestrol, and 17-β-estradiol
The figure shows the chemical structures of trans-resveratrol, diethylstilbestrol, and 17-β-estradiol.
References
- Soleas GJ, Diamandis EP, Goldberg DM. Resveratrol: a molecule whose time has come? And gone? Clin Biochem. 1997;30(2):91-113. (PubMed)
- Aggarwal BB, Bhardwaj A, Aggarwal RS, Seeram NP, Shishodia S, Takada Y. Role of resveratrol in prevention and therapy of cancer: preclinical and clinical studies. Anticancer Res. 2004;24(5A):2783-2840. (PubMed)
- Romero-Perez AI, Ibern-Gomez M, Lamuela-Raventos RM, de La Torre-Boronat MC. Piceid, the major resveratrol derivative in grape juices. J Agric Food Chem. 1999;47(4):1533-1536. (PubMed)
- Siemann EH, Creasey LL. Concentration of the phytoalexin resveratrol in wine. Am J Enol Vitic. 1992;43(1):49-52.
- Jang M, Cai L, Udeani GO, et al. Cancer chemopreventive activity of resveratrol, a natural product derived from grapes. Science. 1997;275(5297):218-220. (PubMed)
- Howitz KT, Bitterman KJ, Cohen HY, et al. Small molecule activators of sirtuins extend Saccharomyces cerevisiae lifespan. Nature. 2003;425(6954):191-196. (PubMed)
- Walle T, Hsieh F, Delegge MH, Oatis JE, Jr., Walle UK. High absorption but very low bioavailability of oral resveratrol in humans. Drug Metab Dispos. 2004;32(12):1377-1382. (PubMed)
- Wenzel E, Somoza V. Metabolism and bioavailability of trans-resveratrol. Mol Nutr Food Res. 2005;49(5):472-481. (PubMed)
- Goldberg DM, Yan J, Soleas GJ. Absorption of three wine-related polyphenols in three different matrices by healthy subjects. Clin Biochem. 2003;36(1):79-87. (PubMed)
- Meng X, Maliakal P, Lu H, Lee MJ, Yang CS. Urinary and plasma levels of resveratrol and quercetin in humans, mice, and rats after ingestion of pure compounds and grape juice. J Agric Food Chem. 2004;52(4):935-942. (PubMed)
- Vitaglione P, Sforza S, Galaverna G, et al. Bioavailability of trans-resveratrol from red wine in humans. Mol Nutr Food Res. 2005;49(5):495-504. (PubMed)
- Gescher AJ, Steward WP. Relationship between mechanisms, bioavailibility, and preclinical chemopreventive efficacy of resveratrol: a conundrum. Cancer Epidemiol Biomarkers Prev. 2003;12(10):953-957. (PubMed)
- Stojanovic S, Sprinz H, Brede O. Efficiency and mechanism of the antioxidant action of trans-resveratrol and its analogues in the radical liposome oxidation. Arch Biochem Biophys. 2001;391(1):79-89. (PubMed)
- Brito P, Almeida LM, Dinis TC. The interaction of resveratrol with ferrylmyoglobin and peroxynitrite; protection against LDL oxidation. Free Radic Res. 2002;36(6):621-631. (PubMed)
- Frankel EN, Waterhouse AL, Kinsella JE. Inhibition of human LDL oxidation by resveratrol. Lancet. 1993;341(8852):1103-1104. (PubMed)
- Bradamante S, Barenghi L, Villa A. Cardiovascular protective effects of resveratrol. Cardiovasc Drug Rev. 2004;22(3):169-188. (PubMed)
- Tangkeangsirisin W, Serrero G. Resveratrol in the chemoprevention and chemotherapy of breast cancer. In: Bagchi D, Preuss HG, eds. Phytopharmaceuticals in Cancer Chemoprevention. Boca Raton: CRC Press; 2005:449-463.
- Bowers JL, Tyulmenkov VV, Jernigan SC, Klinge CM. Resveratrol acts as a mixed agonist/antagonist for estrogen receptors alpha and beta. Endocrinology. 2000;141(10):3657-3667. (PubMed)
- Gehm BD, McAndrews JM, Chien PY, Jameson JL. Resveratrol, a polyphenolic compound found in grapes and wine, is an agonist for the estrogen receptor. Proc Natl Acad Sci U S A. 1997;94(25):14138-14143. (PubMed)
- Bhat KP, Lantvit D, Christov K, Mehta RG, Moon RC, Pezzuto JM. Estrogenic and antiestrogenic properties of resveratrol in mammary tumor models. Cancer Res. 2001;61(20):7456-7463. (PubMed)
- Lu R, Serrero G. Resveratrol, a natural product derived from grape, exhibits antiestrogenic activity and inhibits the growth of human breast cancer cells. J Cell Physiol. 1999;179(3):297-304. (PubMed)
- Chen ZH, Hurh YJ, Na HK, et al. Resveratrol inhibits TCDD-induced expression of CYP1A1 and CYP1B1 and catechol estrogen-mediated oxidative DNA damage in cultured human mammary epithelial cells. Carcinogenesis. 2004;25(10):2005-2013. (PubMed)
- Ciolino HP, Yeh GC. Inhibition of aryl hydrocarbon-induced cytochrome P-450 1A1 enzyme activity and CYP1A1 expression by resveratrol. Mol Pharmacol. 1999;56(4):760-767. (PubMed)
- Yang SH, Kim JS, Oh TJ, et al. Genome-scale analysis of resveratrol-induced gene expression profile in human ovarian cancer cells using a cDNA microarray. Int J Oncol. 2003;22(4):741-750. (PubMed)
- Stewart ZA, Westfall MD, Pietenpol JA. Cell-cycle dysregulation and anticancer therapy. Trends Pharmacol Sci. 2003;24(3):139-145. (PubMed)
- Joe AK, Liu H, Suzui M, Vural ME, Xiao D, Weinstein IB. Resveratrol induces growth inhibition, S-phase arrest, apoptosis, and changes in biomarker expression in several human cancer cell lines. Clin Cancer Res. 2002;8(3):893-903. (PubMed)
- Fulda S, Debatin KM. Resveratrol modulation of signal transduction in apoptosis and cell survival: a mini-review. Cancer Detect Prev. 2006;30(3):217-223. (PubMed)
- Woo JH, Lim JH, Kim YH, et al. Resveratrol inhibits phorbol myristate acetate-induced matrix metalloproteinase-9 expression by inhibiting JNK and PKC delta signal transduction. Oncogene. 2004;23(10):1845-1853. (PubMed)
- Igura K, Ohta T, Kuroda Y, Kaji K. Resveratrol and quercetin inhibit angiogenesis in vitro. Cancer Lett. 2001;171(1):11-16. (PubMed)
- Lin MT, Yen ML, Lin CY, Kuo ML. Inhibition of vascular endothelial growth factor-induced angiogenesis by resveratrol through interruption of Src-dependent vascular endothelial cadherin tyrosine phosphorylation. Mol Pharmacol. 2003;64(5):1029-1036. (PubMed)
- Chen Y, Tseng SH. Review. Pro- and anti-angiogenesis effects of resveratrol. In Vivo. 2007;21(2):365-370. (PubMed)
- Steele VE, Hawk ET, Viner JL, Lubet RA. Mechanisms and applications of non-steroidal anti-inflammatory drugs in the chemoprevention of cancer. Mutat Res. 2003;523-524:137-144. (PubMed)
- Donnelly LE, Newton R, Kennedy GE, et al. Anti-inflammatory effects of resveratrol in lung epithelial cells: molecular mechanisms. Am J Physiol Lung Cell Mol Physiol. 2004;287(4):L774-783. (PubMed)
- Pinto MC, Garcia-Barrado JA, Macias P. Resveratrol is a potent inhibitor of the dioxygenase activity of lipoxygenase. J Agric Food Chem. 1999;47(12):4842-4846. (PubMed)
- Shankar S, Singh G, Srivastava RK. Chemoprevention by resveratrol: molecular mechanisms and therapeutic potential. Front Biosci. 2007;12:4839-4854. (PubMed)
- de la Lastra CA, Villegas I. Resveratrol as an anti-inflammatory and anti-aging agent: mechanisms and clinical implications. Mol Nutr Food Res. 2005;49(5):405-430. (PubMed)
- Blake GJ, Ridker PM. C-reactive protein and other inflammatory risk markers in acute coronary syndromes. J Am Coll Cardiol. 2003;41(4 Suppl S):37S-42S. (PubMed)
- Stocker R, Keaney JF, Jr. Role of oxidative modifications in atherosclerosis. Physiol Rev. 2004;84(4):1381-1478. (PubMed)
- Carluccio MA, Siculella L, Ancora MA, et al. Olive oil and red wine antioxidant polyphenols inhibit endothelial activation: antiatherogenic properties of Mediterranean diet phytochemicals. Arterioscler Thromb Vasc Biol. 2003;23(4):622-629. (PubMed)
- Ferrero ME, Bertelli AE, Fulgenzi A, et al. Activity in vitro of resveratrol on granulocyte and monocyte adhesion to endothelium. Am J Clin Nutr. 1998;68(6):1208-1214. (PubMed)
- Faxon DP, Fuster V, Libby P, et al. Atherosclerotic Vascular Disease Conference: Writing Group III: pathophysiology. Circulation. 2004;109(21):2617-2625. (PubMed)
- Mnjoyan ZH, Fujise K. Profound negative regulatory effects by resveratrol on vascular smooth muscle cells: a role of p53-p21(WAF1/CIP1) pathway. Biochem Biophys Res Commun. 2003;311(2):546-552. (PubMed)
- Haider UG, Sorescu D, Griendling KK, Vollmar AM, Dirsch VM. Resveratrol increases serine15-phosphorylated but transcriptionally impaired p53 and induces a reversible DNA replication block in serum-activated vascular smooth muscle cells. Mol Pharmacol. 2003;63(4):925-932. (PubMed)
- Duffy SJ, Vita JA. Effects of phenolics on vascular endothelial function. Curr Opin Lipidol. 2003;14(1):21-27. (PubMed)
- Klinge CM, Blankenship KA, Risinger KE, et al. Resveratrol and estradiol rapidly activate MAPK signaling through estrogen receptors alpha and beta in endothelial cells. J Biol Chem. 2005; 280(9):7460-7468. (PubMed)
- Wallerath T, Deckert G, Ternes T, et al. Resveratrol, a polyphenolic phytoalexin present in red wine, enhances expression and activity of endothelial nitric oxide synthase. Circulation. 2002;106(13):1652-1658. (PubMed)
- Kirk RI, Deitch JA, Wu JM, Lerea KM. Resveratrol decreases early signaling events in washed platelets but has little effect on platalet in whole blood. Blood Cells Mol Dis. 2000;26(2):144-150. (PubMed)
- Pace-Asciak CR, Hahn S, Diamandis EP, Soleas G, Goldberg DM. The red wine phenolics trans-resveratrol and quercetin block human platelet aggregation and eicosanoid synthesis: implications for protection against coronary heart disease. Clin Chim Acta. 1995;235(2):207-219. (PubMed)
- Klatsky AL. Drink to your health? Sci Am. 2003;288(2):74-81. (PubMed)
- Corrao G, Rubbiati L, Bagnardi V, Zambon A, Poikolainen K. Alcohol and coronary heart disease: a meta-analysis. Addiction. 2000;95(10):1505-1523. (PubMed)
- Criqui MH, Ringel BL. Does diet or alcohol explain the French paradox? Lancet. 1994;344(8939-8940):1719-1723. (PubMed)
- St Leger AS, Cochrane AL, Moore F. Factors associated with cardiac mortality in developed countries with particular reference to the consumption of wine. Lancet. 1979;1(8124):1017-1020. (PubMed)
- German JB, Walzem RL. The health benefits of wine. Annu Rev Nutr. 2000;20:561-593. (PubMed)
- Gronbaek M, Becker U, Johansen D, et al. Type of alcohol consumed and mortality from all causes, coronary heart disease, and cancer. Ann Intern Med. 2000;133(6):411-419. (PubMed)
- Klatsky AL, Friedman GD, Armstrong MA, Kipp H. Wine, liquor, beer, and mortality. Am J Epidemiol. 2003;158(6):585-595. (PubMed)
- Renaud SC, Gueguen R, Siest G, Salamon R. Wine, beer, and mortality in middle-aged men from eastern France. Arch Intern Med. 1999;159(16):1865-1870. (PubMed)
- Mukamal KJ, Conigrave KM, Mittleman MA, et al. Roles of drinking pattern and type of alcohol consumed in coronary heart disease in men. N Engl J Med. 2003;348(2):109-118. (PubMed)
- Rimm EB, Klatsky A, Grobbee D, Stampfer MJ. Review of moderate alcohol consumption and reduced risk of coronary heart disease: is the effect due to beer, wine, or spirits. BMJ. 1996;312(7033):731-736. (PubMed)
- Wannamethee SG, Shaper AG. Type of alcoholic drink and risk of major coronary heart disease events and all-cause mortality. Am J Public Health. 1999;89(5):685-690. (PubMed)
- Barefoot JC, Gronbaek M, Feaganes JR, McPherson RS, Williams RB, Siegler IC. Alcoholic beverage preference, diet, and health habits in the UNC Alumni Heart Study. Am J Clin Nutr. 2002;76(2):466-472. (PubMed)
- McCann SE, Sempos C, Freudenheim JL, et al. Alcoholic beverage preference and characteristics of drinkers and nondrinkers in western New York (United States). Nutr Metab Cardiovasc Dis. 2003;13(1):2-11. (PubMed)
- Mortensen EL, Jensen HH, Sanders SA, Reinisch JM. Better psychological functioning and higher social status may largely explain the apparent health benefits of wine: a study of wine and beer drinking in young Danish adults. Arch Intern Med. 2001;161(15):1844-1848. (PubMed)
- Johansen D, Friis K, Skovenborg E, Gronbaek M. Food buying habits of people who buy wine or beer: cross sectional study. BMJ. 2006;332(7540):519-522. (PubMed)
- Ruidavets JB, Bataille V, Dallongeville J, et al. Alcohol intake and diet in France, the prominent role of lifestyle. Eur Heart J. 2004;25(13):1153-1162. (PubMed)
- Stocker R, O'Halloran RA. Dealcoholized red wine decreases atherosclerosis in apolipoprotein E gene-deficient mice independently of inhibition of lipid peroxidation in the artery wall. Am J Clin Nutr. 2004;79(1):123-130. (PubMed)
- De Curtis A, Murzilli S, Di Castelnuovo A, et al. Alcohol-free red wine prevents arterial thrombosis in dietary-induced hypercholesterolemic rats: experimental support for the 'French paradox'. J Thromb Haemost. 2005;3(2):346-350. (PubMed)
- Lekakis J, Rallidis LS, Andreadou I, et al. Polyphenolic compounds from red grapes acutely improve endothelial function in patients with coronary heart disease. Eur J Cardiovasc Prev Rehabil. 2005;12(6):596-600. (PubMed)
- Wang Z, Huang Y, Zou J, Cao K, Xu Y, Wu JM. Effects of red wine and wine polyphenol resveratrol on platelet aggregation in vivo and in vitro. Int J Mol Med. 2002;9(1):77-79. (PubMed)
- Chen CK, Pace-Asciak CR. Vasorelaxing activity of resveratrol and quercetin in isolated rat aorta. Gen Pharmacol. 1996;27(2):363-366. (PubMed)
- Szewczuk LM, Forti L, Stivala LA, Penning TM. Resveratrol is a peroxidase-mediated inactivator of COX-1 but not COX-2: a mechanistic approach to the design of COX-1 selective agents. J Biol Chem. 2004;279(21):22727-22737. (PubMed)
- Tsai SH, Lin-Shiau SY, Lin JK. Suppression of nitric oxide synthase and the down-regulation of the activation of NFkappaB in macrophages by resveratrol. Br J Pharmacol. 1999;126(3):673-680. (PubMed)
- Fukao H, Ijiri Y, Miura M, et al. Effect of trans-resveratrol on the thrombogenicity and atherogenicity in apolipoprotein E-deficient and low-density lipoprotein receptor-deficient mice. Blood Coagul Fibrinolysis. 2004;15(6):441-446. (PubMed)
- Wang Z, Zou J, Huang Y, Cao K, Xu Y, Wu JM. Effect of resveratrol on platelet aggregation in vivo and in vitro. Chin Med J (Engl). 2002;115(3):378-380. (PubMed)
- Wilson T, Knight TJ, Beitz DC, Lewis DS, Engen RL. Resveratrol promotes atherosclerosis in hypercholesterolemic rabbits. Life Sci. 1996;59(1):PL15-21. (PubMed)
- Li ZG, Hong T, Shimada Y, et al. Suppression of N-nitrosomethylbenzylamine (NMBA)-induced esophageal tumorigenesis in F344 rats by resveratrol. Carcinogenesis. 2002;23(9):1531-1536. (PubMed)
- Tessitore L, Davit A, Sarotto I, Caderni G. Resveratrol depresses the growth of colorectal aberrant crypt foci by affecting bax and p21(CIP) expression. Carcinogenesis. 2000;21(8):1619-1622. (PubMed)
- Banerjee S, Bueso-Ramos C, Aggarwal BB. Suppression of 7,12-dimethylbenz(a)anthracene-induced mammary carcinogenesis in rats by resveratrol: role of nuclear factor-kappaB, cyclooxygenase 2, and matrix metalloprotease 9. Cancer Res. 2002;62(17):4945-4954. (PubMed)
- Hecht SS, Kenney PM, Wang M, et al. Evaluation of butylated hydroxyanisole, myo-inositol, curcumin, esculetin, resveratrol and lycopene as inhibitors of benzo(a)pyrene plus 4-(methylnitrosamino)-1-(3-pyridyl)-1-butanone-induced lung tumorigenesis in A/J mice. Cancer Lett. 1999;137(2):123-130. (PubMed)
- Berge G, Ovrebo S, Eilertsen E, Haugen A, Mollerup S. Analysis of resveratrol as a lung cancer chemopreventive agent in A/J mice exposed to benzo(a)pyrene. Br J Cancer. 2004;91(7):1380-1383. (PubMed)
- Ziegler CC, Rainwater L, Whelan J, McEntee MF. Dietary resveratrol does not affect intestinal tumorigenesis in Apc(Min/+) mice. J Nutr. 2004;134(1):5-10. (PubMed)
- Schneider Y, Duranton B, Gosse F, Schleiffer R, Seiler N, Raul F. Resveratrol inhibits intestinal tumorigenesis and modulates host-defense-related gene expression in an animal model of human familial adenomatous polyposis. Nutr Cancer. 2001;39(1):102-107. (PubMed)
- Sengottuvelan M, Nalini N. Dietary supplementation of resveratrol suppresses colonic tumour incidence in 1,2-dimethylhydrazine-treated rats by modulating biotransforming enzymes and aberrant crypt foci development. Br J Nutr. 2006;96(1):145-153. (PubMed)
- Sengottuvelan M, Senthilkumar R, Nalini N. Modulatory influence of dietary resveratrol during different phases of 1,2-dimethylhydrazine induced mucosal lipid-peroxidation, antioxidant status and aberrant crypt foci development in rat colon carcinogenesis. Biochim Biophys Acta. 2006;1760(8):1175-1183. (PubMed)
- Sengottuvelan M, Viswanathan P, Nalini N. Chemopreventive effect of trans-resveratrol--a phytoalexin against colonic aberrant crypt foci and cell proliferation in 1,2-dimethylhydrazine induced colon carcinogenesis. Carcinogenesis. 2006;27(5):1038-1046. (PubMed)
- Baur JA, Sinclair DA. Therapeutic potential of resveratrol: the in vivo evidence. Nat Rev Drug Discov. 2006;5(6):493-506. (PubMed)
- Heilbronn LK, Ravussin E. Calorie restriction and aging: review of the literature and implications for studies in humans. Am J Clin Nutr. 2003;78(3):361-369. (PubMed)
- Lin SJ, Defossez PA, Guarente L. Requirement of NAD and SIR2 for life-span extension by calorie restriction in Saccharomyces cerevisiae. Science. 2000;289(5487):2126-2128. (PubMed)
- Wood JG, Rogina B, Lavu S, et al. Sirtuin activators mimic caloric restriction and delay ageing in metazoans. Nature. 2004;430(7000):686-689. (PubMed)
- Valenzano DR, Terzibasi E, Genade T, Cattaneo A, Domenici L, Cellerino A. Resveratrol prolongs lifespan and retards the onset of age-related markers in a short-lived vertebrate. Curr Biol. 2006;16(3):296-300. (PubMed)
- Baur JA, Pearson KJ, Price NL, et al. Resveratrol improves health and survival of mice on a high-calorie diet. Nature. 2006;444(7117):337-342. (PubMed)
- Barger JL, Kayo T, Vann JM, et al. A low dose of dietary resveratrol partially mimics caloric restriction and retards aging parameters in mice. PLoS One. 2008;3(6):e2264. (PubMed)
- Burns J, Yokota T, Ashihara H, Lean ME, Crozier A. Plant foods and herbal sources of resveratrol. J Agric Food Chem. 2002;50(11):3337-3340. (PubMed)
- Rimando AM, Kalt W, Magee JB, Dewey J, Ballington JR. Resveratrol, pterostilbene, and piceatannol in vaccinium berries. J Agric Food Chem. 2004;52(15):4713-4719. (PubMed)
- Sanders TH, McMichael RW, Jr., Hendrix KW. Occurrence of resveratrol in edible peanuts. J Agric Food Chem. 2000;48(4):1243-1246. (PubMed)
- Creasey LL, Coffee M. Phytoalexin production potential of grape berries. J Am Soc Hortic Sci. 1988;113(2):230-234.
- Fremont L. Biological effects of resveratrol. Life Sci. 2000;66(8):663-673. (PubMed)
- Goldberg DM, Karumanchiri A, Ng E, Yan J, Eleftherios P, Soleas G. Direct gas chromatographic-mass spectrometric method to assay cis-resveratrol in wines: preliminary survey of its concentration in commercial wines. J Agric Food Chem. 1995;43(5):1245-1250.
- Burns J, Gardner PT, Matthews D, Duthie GG, Lean ME, Crozier A. Extraction of phenolics and changes in antioxidant activity of red wines during vinification. J Agric Food Chem. 2001;49(12):5797-5808. (PubMed)
- Moreno-Labanda JF, Mallavia R, Perez-Fons L, Lizama V, Saura D, Micol V. Determination of piceid and resveratrol in Spanish wines deriving from Monastrell (Vitis vinifera L.) grape variety. J Agric Food Chem. 2004;52(17):5396-5403. (PubMed)
- Romero-Perez AI, Lamuela-Raventos RM, Waterhouse AL, de la Torre-Boronat MC. Levels of cis- and trans-resveratrol and their glucosides in white and rosé Vitis vinifera wines from Spain. J Agric Food Chem. 1996;44(8):2124-2128.
- Sobolev VS, Cole RJ. trans-resveratrol content in commercial peanuts and peanut products. J Agric Food Chem. 1999;47(4):1435-1439. (PubMed)
- Hendler SS, Rorvik DR, eds. PDR for Nutritional Supplements. Montvale: Medical Economics Company, Inc; 2001.
- Boocock DJ, Faust GE, Patel KR, et al. Phase I dose escalation pharmacokinetic study in healthy volunteers of resveratrol, a potential cancer chemopreventive agent. Cancer Epidemiol Biomarkers Prev. 2007;16(6):1246-1252. (PubMed)
- Crowell JA, Korytko PJ, Morrissey RL, Booth TD, Levine BS. Resveratrol-associated renal toxicity. Toxicol Sci. 2004;82(2):614-619. (PubMed)
- Juan ME, Vinardell MP, Planas JM. The daily oral administration of high doses of trans-resveratrol to rats for 28 days is not harmful. J Nutr. 2002;132(2):257-260. (PubMed)
- American Academy of Pediatrics. Committee on Substance Abuse and Committee on Children With Disabilities. Fetal alcohol syndrome and alcohol-related neurodevelopmental disorders. Pediatrics. 2000;106(2 Pt 1):358-361. (PubMed)
- Bertelli AA, Giovannini L, Giannessi D, et al. Antiplatelet activity of synthetic and natural resveratrol in red wine. Int J Tissue React. 1995;17(1):1-3. (PubMed)
- Piver B, Berthou F, Dreano Y, Lucas D. Inhibition of CYP3A, CYP1A and CYP2E1 activities by resveratrol and other non volatile red wine components. Toxicol Lett. 2001;125(1-3):83-91. (PubMed)
- Regev-Shoshani G, Shoseyov O, Kerem Z. Influence of lipophilicity on the interactions of hydroxy stilbenes with cytochrome P450 3A4. Biochem Biophys Res Commun. 2004;323(2):668-673. (PubMed)
免責事項
ライナスポーリング研究所微量栄養素情報センターは、一般向けの食事要因、健康面、栄養補助食品、食品および飲料に関する科学的情報を提供する。著者および出版社は、本サイト上の医学的、心理学的、栄養学的カウンセリングサービスを利用しないことを合意した上で、本情報を利用することができる。本情報は、有資格の医療従事者または栄養士への相談の代わりとして利用することはできない。
本ウェブサイトに掲載されている食事要因、栄養補助食品、食品および飲料に含まれる情報は、実施可能なすべての使用法、行為、使用上の注意、副作用、および相互作用を網羅するものではない。本ウェブサイトは、個々の問題についての栄養学的、医学的助言をすることは意図していない。本サイトの電子的に利用可能な情報に基づく個人的な行為、または不作為に対する責任は、明示的に否認される。
本ウェブサイトにおける著作権を有する資料のいずれも、複製、修正、配布、表示、発信、実行、公開または販売をおこなってはならない。本ウェブサイトにハイパーリンクを貼ることは可能であるが、その際には以下の文言を付記することとする。
「本リンクは、オレゴン州立大学ライナスポーリング研究所の提供するウェブサイトへ移動します。<<名前>>は、オレゴン州立大学ライナスポーリング研究所のアフィリエイトではなく、認証されたリンクでもありません」