ニンニクと有機硫黄化合物
要約
- ニンニク(Allium sativum L.)は有機硫黄化合物を豊富に含有しており、現在これら化合物の病気予防および治療の可能性について研究が行われている。(詳細な情報)
- ニンニクをつぶすもしくはみじん切りにすると、Allicinの形成を触媒するAlliinaseと呼ばれている酵素が放出される。Allicinは速やかに分解して様々な有機硫黄合成物を形成する。(詳細な情報)
- 加熱調理することでアリイナーゼを不活性することができるため、一部の科学者は加熱調理をする前に、ニンニクを細かく刻んだり、粉砕してから10分間放置することを勧めている。(詳細な情報)
- ニンニク製剤には、いくつかの種類が市販されており、各種製剤はニンニクがどのように処理されたかに応じて、異なる有機硫黄化合物の分析結果を提供している。(詳細な情報)
- 無作為比較試験の結果は、ニンニクの摂取が血小板凝集を阻害することを示唆しているが、ニンニク製剤が循環器疾患を防ぐことができるかどうかは不明である。(詳細な情報)
- いくつかの疫学的研究の結果、ニンニクや他のネギ属野菜(例えば、玉ねぎやネギ)の多量摂取は胃癌·大腸癌の予防に役立つことを示唆しているが、ニンニク由来の有機硫黄化合物が、ヒトの癌予防または治療に有効であるかどうかは不明である。(詳細な情報)
はじめに
ニンニク(Allium sativum L.)は、何世紀にもわたり多様な文化のなかで料理や薬用に用いられてきた (1)。ニンニクは有機硫黄化合物を特に豊富に含んでおり、これらはその味と香りだけでなく、健康上の潜在的利益にも関与していると考えられている(2)。ニンニクの健康上の利点に対する消費者の関心は、アメリカ国内でのハーブ系製剤の売上1位を獲得できるほど十分に高い(3)。科学者は、癌や循環器疾患などの慢性疾患を予防・治療するニンニク由来の有機硫黄化合物の可能性に興味を持っている(4)。
ニンニクの有機硫黄化合物
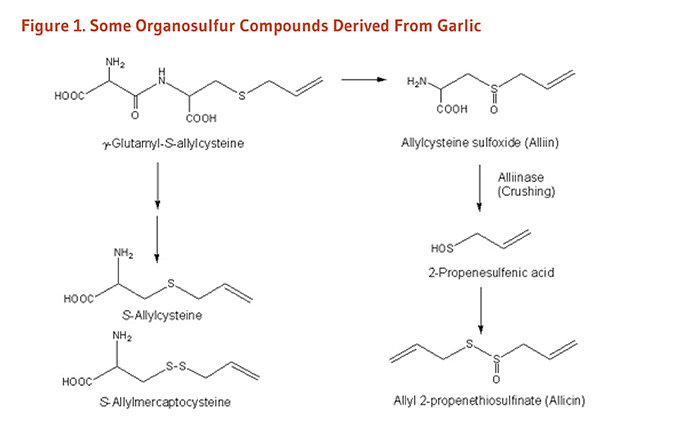
2種類の有機硫黄化合物がニンニクから発見されている。ひとつはGamma-glutamylcysteines、もうひとつはCysteine sulfoxidesである。Allylcysteine sulfoxide (alliin) は、ニンニクに含まれるCysteine sulfoxidesの約80%を占めている (1)。生のニンニク片がつぶされたりみじん切りにされる、または噛まれたとき、Alliinaseとして知られている酵素が放出される。Alliinaseは、Cysteine sulfoxidesからのスルフェン酸の形成を触媒する(Figure 1)。スルフェン酸は互いに自発的に反応してthiosulfinatesと呼ばれる不安定な化合物を形成する。Alliinの場合、Alliinaseによって生じたスルフェン酸が互いに反応しあってAllicinとして知られるthiosulfinateを形成する(つぶしたニンニクの場合、23℃における半減期は2.5日。)。Thiosulfinatesの形成は非常に迅速であり、粉砕したニンニクの場合、10〜60秒以内に完了することが見出されている。Allicinはin vitroでの分解で、diallyl trisulfide(DATS)、diallyl disulfide(DADS)、およびdiallyl sulfide(DAS)を含む多様な脂溶性有機硫黄化合物を形成するか (Figure 2)、油または有機溶媒存在下ではajoene やvinyldithiinsを形成する(2)。ニンニクを粉砕してもそのGamma-glutamylcysteine含量は変化しない。例えばS-allylcysteine等の水溶性有機硫黄化合物は、熟成ニンニク抽出液の製造など、水溶液中でつぶしたニンニクの長期保存中にgamma-glutamylcysteinesから形成される (下記出典を参照)。

生物学的利用能と代謝
Allicin由来の化合物
AllicinおよびAllicin由来の化合物の吸収と代謝は、部分的にしか明らかにされていない (5)。多くの生物活性は多様なAllicin由来の化合物に起因しているが、それらの化合物や代謝産物のどれが実際に標的組織に到達するかはまだ明確になっていない(1)。放射性標識化合物を用いた動物実験では、Allicinまたはその分解生成物が腸管吸収されることを示している (6,7)。しかしながら、AllicinとAllicin由来の化合物(diallylsufides、ajoene、vinyldithiins)は、新鮮なニンニク25 gまたはAllicin 60 mgの摂取後でもヒトの血液、尿、糞中に検出されない。これらの知見は、Allicin及びAllicin由来化合物は急速に代謝されることを示唆している。呼気中のアリルメチルスルフィド濃度は、Allicin及びAllicin由来化合物の生物学的利用能の指標として提案されている(5)。つぶしたニンニクとそれに相当する量のallicin、DATS、DADS、ajoene、アリルメチルスルフィドをヒトが消費したとき、呼気中のアリルメチルスルフィド濃度が同様に増加したことから、Allicin及びAllicin由来化合物は、呼気中の計測できる揮発性化合物であるアリルメチルスルフィドに代謝されることを示唆している。
Gamma-GlutamylcysteinesとS-Allylcysteine
Gamma-glutamylcysteinesはそのまま吸収されS-allylcysteineおよびS-1-propenylcysteineに加水分解されると考えられている。その理由として、これら化合物の代謝物がニンニク摂取後のヒト尿中で測定されているためである (8,9)。熟成ニンニク抽出物やS-allylcysteineを含有する市販のニンニク製剤を摂取したヒトでは、血漿中のS-allylcysteine濃度が増加することが見出された(10,11)。
生物活性
心血管疾患の予防に関連して
コレステロール合成の阻害
ニンニクおよびニンニク由来の有機硫黄化合物は、肝細胞によるコレステロール合成を減少させることが見出されている(12)。 S-allylcysteineとajoeneを含む、 いくつかのニンニク由来の有機硫黄化合物は、コレステロール生合成経路において重要な酵素である3-hydroxy-3-methyl-glutaryl-coenzyme A reductase (HMG-CoA reductase) を阻害することが見出されている(13,14)。またニンニク由来の化合物は4-alpha-methyl oxidaseを含むコレステロール生合成経路内の他の酵素を阻害する可能性がある(15)。
血小板凝集抑制
ニンニク由来の多様な有機硫黄化合物は血小板凝集を阻害することが試験管内で見出されている (16,17)。
抗炎症活性
炎症は、心臓血管疾患の病状に重要な役割を果たすと思われる(18)。ニンニク由来の有機硫黄化合物はin vitroでcyclooxygenaseおよびlipoxygenaseといった炎症性酵素の活性を阻害し[総説19]、炎症性白血球細胞(マクロファージ)中の誘導型一酸化窒素合成酵素(iNOS)の発現を減少させることが見出されている(20,21)。特に最近では、有機硫黄化合物は培養したマクロファージ内およびヒト全血中における炎症性シグナル分子の産生を減少させることが見出されている(22,23)。
動脈平滑筋増殖の阻害
正常に休止した動脈平滑筋細胞の増殖と遊走は、アテローム性動脈硬化症および冠動脈再狭窄を含む血管疾患の主要な特徴である。ヒトの心血管疾患におけるこれらの知見の重要性はまだ明らかではないが、限られた細胞培養の研究では、ニンニク由来の有機硫黄化合物は血管平滑筋細胞の増殖と遊走を阻害し得ることを示唆している(13,25,26)。
抗酸化活性
多数の有機硫黄化合物は、試験管内で抗酸化活性を有することが見出され、有機硫黄化合物は、重要な細胞内抗酸化物質であるグルタチオンの合成を促進することができるいくつかの証拠が存在している(27)。高血圧成人におけるニンニク油の摂取試験では、小規模非対照試験にてin vivo で脂質 (脂肪) 酸化のバイオマーカーを減少させることが報告されているが(28)、ニンニク由来の有機硫黄化合物が、in vivoで臨床的に重要な抗酸化効果を有するかどうかはまだ明らかではない。
硫化水素を介した血管拡張活性
正常な動脈機能の維持は心血管疾患の予防において重要な役割を果たしている。体内の細胞により産生されるガス状のシグナル伝達分子である硫化水素は、血管拡張剤 (血管を弛緩する) として作用し、従って心臓保護作用を有する可能性がある(29,30)。最近の研究においてニンニク由来の化合物は、in vitroで赤血球によって硫化水素に変換されることがわかった(31)。しかし、ヒトにおける生ニンニクの大量摂取は呼気中の硫化水素濃度を増加させないため、in vivoにおいてニンニク化合物らの硫化水素生成への代謝はあまり起こらないことを示唆している(32)。
癌に関連する生物活性
発癌性物質の代謝に及ぼす影響
フェーズI生体内変換酵素の阻害
いくつかの化学発癌性物質は、チトクロームP450(CYP)ファミリーに属するようなフェーズI生体内変換酵素によって代謝されるまで、活性を有する発癌性物質にならない。発癌性物質の活性化に関与する特異的CYP酵素の阻害は、いくつかの動物モデルにおける癌の進展を阻害する(33)。特に、DASとその代謝物は、in vitro (34)、および動物に高用量で経口投与した場合において、CYP2E1活性を阻害することが見出されている(35,36)。ヒトにおいてもガーリックオイルとDASの経口投与はCYP2E1活性を減少させる証拠を示す結果となった(37,38)。
フェーズII生体内変換酵素の誘導
フェーズII生体内酵素によって触媒される反応は、一般的に体内の薬物、毒素そして発癌性物質の除去を促進する。そのためglutathione S-transferaseおよびquinone reductaseなどのフェーズII酵素の活性増大は、発癌性物質となり得る物質の除去を促進し、癌を防ぐ手助けをする可能性がある(39)。動物実験においてニンニク製剤および有機硫黄化合物の経口投与は、様々な組織中のフェーズII酵素の活性を増加させる(40-42)。多数のフェーズII酵素の遺伝子は、抗酸化応答因子(ARE)と呼ばれるDNAの特異的配列を含んでいる。最近の研究では、allyl sulfides、特にDATSはNrf2として知られる転写因子の核への移行を促進し、核でNrf2がAREと結合してAREを含む遺伝子の転写を増大させることを示唆している(43,44)。非常に高用量の有機硫黄化合物が多くの動物実験で投与されたが、少なくとも一つの研究では、ヒトが摂取し得る量でDADSを投与したマウスの消化管でキノンレダクターゼ活性が増加していることがわかった(45)。
細胞内グルタチオン合成の促進
グルタチオンは重要な細胞内の抗酸化物質であり、いくつかのフェーズII生体内変換反応にも必要とされる。細胞培養および動物研究から、ニンニク由来の有機硫黄化合物が細胞内グルタチオン濃度を増加させるという証拠がある(43,46)。多くのフェーズII酵素の遺伝子と同様に、グルタチオン合成に重要な酵素の遺伝子にもまたAREが含まれている。このように、有機硫黄化合物は、核への移行とAREsを含む遺伝子へのNrf2転写因子の結合を促進することにより、細胞のグルタチオン合成を増加させることができる(上記のフェーズII酵素の誘導を参照)。
細胞周期停止の誘導
無秩序な細胞分裂はヒトの癌の顕著な特徴である(47)。正常細胞では、細胞周期は細胞分裂前における染色体の分離とDNA複製を忠実、且つ確実にするために厳密に調節されている。DNAが損傷すると、細胞周期はDNAの修復もしくは細胞死(アポトーシス)に至る経路の活性化のため一時的に停止することになる。細胞培養実験でDATS、DADS、ajoene、およびS-allylmercaptocysteine(SAMC)などの有機硫黄化合物を癌細胞に加えると、細胞周期の停止を誘導することが見出されている(48-50)。
アポトーシスの誘発
アポトーシスは、遺伝的に損傷もしくは不要になった細胞の自己破壊のための正常な生理的プロセスである。前癌性および癌性細胞はアポトーシス誘導シグナルに対して抵抗性を持つ(51)。Allicin、ajoene、DAS、DADS、DATSおよびSAMCなどのニンニク由来の有機硫黄化合物は、様々な培養癌細胞株に添加するとアポトーシスを誘導することが見出されている[総説 (48,51)]。ニンニクの水抽出物、S-allylcysteineの経口投与は、口腔癌の動物モデルでアポトーシスを促進することが報告されている(52,53)。
抗菌活性
ニンニク抽出物は、抗菌剤及び抗真菌特性を有することが見出された(54,55)。Thiosulfinate類、特にAllicinは、ニンニクの抗菌活性において重要な役割を果たすと考えられている(55-57)。DATSやajoeneなどのAllicin由来の化合物もある程度の抗菌活性をin vitroで示すが、その抗菌性はAllicinよりもかなり弱い(1)。これまで、無作為化比較試験では、経口ニンニク調製物がヒトで有意な抗菌活性を示すという確定的な証拠は得られていない(58-60)が、Allicinの豊富なニンニク製剤(生または加熱調理したニンニク)を使用した臨床試験は行われていない。小規模無作為比較試験では、1日2回の1%ajoeneクリームの皮膚への塗布が、足白癬(水虫)治療において、1%テルビナフィン(ラミシール)クリームと同等のの効果があることがわかった(61)。
病気の予防
心臓血管疾患
ニンニクとそれによる心血管疾患予防の可能性への関心は、地中海付近に住む人々の心血管疾患による死亡率が低いという観察から始まった(62)。ニンニクは地中海料理において一般的な食材であるが、 数多くの"地中海食"の特徴が、その心臓保護効果を説明するために提案されている。ニンニクの消費と心血管疾患リスクの関連を検討してきた疫学的研究の数は少ないが、心血管疾患の危険因子に対するニンニク補給効果に関する多数の介入試験で検討がされてきている。
血清脂質プロファイル
40以上の無作為化比較試験において、血清コレステロールレベルが正常もしくは高値のヒトの血清脂質プロファイルに対する多様なニンニク製剤の摂取による効果が検討された(63)。これらの試験の多くには方法論的な限界があったものの、いくつかのメタ分析の結果では、ニンニクの摂取により血清総コレステロール、LDLコレステロール、トリグリセリドにおいて若干(6から11パーセント)の減少がプラセボに対して認められた(63-65)。今日における最も網羅的なメタ分析では、摂取開始から3ヶ月後における血清コレステロールレベルのわずかな減少は、6ヶ月後にはもはや統計的に有意な差でないことが明らかになった(63)。最近のいくつかの臨床試験では、プラセボと比較した場合ニンニク製剤の使用は、血清脂質プロファイルにおいて臨床的または統計的に有意に改善される結果になることが明らかにされていない(66-74)。最新の大規模試験では、生ニンニクと高いアリシンの生物学的利用能を有するニンニクサプリメントがそれぞれ高用量で用いられた。しかしどちらの製剤も中程度の高コレステロール血症者において6ヶ月後の血清脂質に有意な効果はなかった(74)。従って、LDLコレステロールが非常に高値のヒトを除いて、ニンニクの摂取は血清脂質に対してほとんど影響を及ぼさないものと強く思われる。
血小板凝集
血小板凝集は、冠動脈または大脳動脈を閉塞する血栓(凝血塊)形成の第一段階の一つであり、それぞれ、心筋梗塞(心臓発作)または虚血性脳梗塞を引き起こす。ほとんどの無作為比較試験によって、ニンニクの投与により、ex vivo (生体外)での血小板凝集が有意に減少することが分かってきた。5件の試験のうち4件において、脱水ニンニクまたはニンニク油浸漬物を投与すると、プラセボ投与に比べて血小板の自然凝集が減少することが分かった(文献(63)にレビューされている)。さらに最近、2件の独立した試験において、熟成ニンニク抽出物の投与は、生理学的な活性化因子に起因する血小板凝集をex vivoで阻害した(11,75)。
血圧
多数の比較臨床試験からは、ニンニクの投与が正常あるいは高血圧の人々における収縮期あるいは拡張期の血圧を有意に低下させるという結果は得られていない(63,76)。システマティック・レビュー(63)に記載された23件の無作為化比較試験のうち3件のみにおいて、拡張期血圧の統計的に有意な低下が報告されており(77-79)、1件のみにおいて収縮期血圧の統計的に有意な低下が報告されている(77)。現時点では、ニンニクの投与を高血圧症の予防もしくは治療に用いることを支持する証拠は少ない。
ニンニクとアテローム性動脈硬化
ヒトのアテローム性動脈硬化の進行に及ぼすニンニクの投与効果を評価しようとした二つの研究が報告されている。一つはドイツで行われた研究で、900 mg/dayの脱水ニンニクの投与が頸動脈および大腿動脈におけるアテローム斑(動脈硬化性プラーク)の進行に及ぼす効果を超音波画像診断で評価したものである(80)。4年間の試験において、プラセボを投与した女性のプラークの増加はニンニク投与した女性のプラークよりも有意に大きかった。しかし、ニンニクまたは偽薬を投与した男性の場合有意差はなかった(81)。もう一つの小規模のパイロット研究では、研究者たちは電子ビーム断層撮影法を用いて冠動脈カルシウムを測定することで、HMG-CoAレダクターゼインヒビター(statins)を既に摂取している19名の大人のアテローム性動脈硬化の進行に及ぼす熟成ニンニク抽出物の投与効果を評価した(82)。1年間の試験において、プラセボを投与した場合に比べて熟成ニンニク抽出物を投与 (4 ml/day) した場合に冠動脈カルシウム値の増加が有意に低かった。冠動脈カルシウム値は冠動脈アテローム性動脈硬化の重症度と相関しているけれども、この技術による予測は依然として研究段階である(83)。いずれの研究もニンニクサプリメントを市販している企業により資金援助を受けて実施された。
要約:心臓血管疾患
要約すると、無作為化比較試験の結果は、3か月のニンニクの投与により血小板凝集が阻害され、血清の脂質プロファイルが穏やかながら改善されることを示唆している。ニンニクの投与によってアテローム性動脈硬化を弱めたり、心筋梗塞や脳卒中といった心臓血管の症状を防止したりできるかどうかは依然不明である。
癌
胃癌
胃癌による死亡率の低い中国のある地域では、男性の82%および女性の74%が1週間に3度以上ニンニクを摂取していることが報告されている。一方、中国でも胃癌による死亡率の高い地域では、1週間に3度以上ニンニクを摂取している男性および女性はわずか1%に過ぎなかった(84)。ヨーロッパとアジアで行われた4つの症例対照研究の内3つにおいて、胃癌と診断された人々の過去におけるニンニクの消費が、癌でない対照群に比べて有意に低かったことが示された(85-87)。症例対照研究の結果を統合評価したメタ解析の結果、ニンニクの摂取量が最高の人々の胃癌になるリスクは、ニンニク摂取量の低い人々よりも約50%低いことが示された(88)。一方、オランダで行われた前向きコホート研究の結果からは、ニンニクサプリメントの利用と胃癌になるリスクとの間に相関性は見られなかった(89)。しかし、ある研究によれば、ヨーロッパで市販されている様々なニンニクサプリメントの硫黄化合物の含量は12倍以上異なっており、このことは注目すべきである(90)。さらに最近になって中国で行われたランダム化二重盲検プラセボ対照介入試験によると、熟成ニンニク抽出物と蒸気蒸留ニンニク油を7.3年間投与しても、胃の前癌病変の罹患率や胃癌の発生率を減少させなかった(60)。おそらくサプリメントとして消費される場合のニンニク化合物の量は、食品として消費される場合の量よりも低い。そのため、ニンニクの抗癌作用を見出すには、日常的にニンニク食品を消費することが必要かもしれない。
Helicobacter pylori感染と胃癌
細菌H. pyloriのいくつかの株の感染が、胃癌になるリスクを顕著に増加させる。実験室内の研究によって、ニンニク製剤および有機硫黄化合物がH. pyloriの増殖を阻害することが示されている。しかし、ニンニクあるいはニンニクサプリメントの多量摂取によりヒトにおけるH. pylori感染を防止あるいは除去する可能性についてはあまり証拠がない(91,92)。中国あるいはトルコにおける研究で、ニンニクの多量摂取量とH. pylori感染率の有意な低下には相関が認められなかった(93,94)。さらに、ニンニクの鱗片(95)、熟成ニンニク抽出物(59)、水蒸気蒸留ニンニク油(59,96)、ニンニク油漬け(97)、またはニンニク粉(98)を用いた臨床試験の結果からも、ニンニクの投与がヒトにおけるH. pyloriの感染を除去する効果は認められていない。
結腸直腸癌
4つの症例対照研究の内3つにおいて、結腸直腸癌と診断された人々のニンニクの摂取量が、癌でない対照群に比べて有意に低かったことが示された(99-101)。一方、3つの前向きコホート研究の結果からは、ニンニクの消費と結腸直腸癌になるリスクとの間に相関性は認められなかった(102-104)。しかし、これらのコホートにおけるニンニクの消費は概して低く、1つの研究においてはニンニクサプリメントを用いて評価したものであった(102)。これらの症例対照研究ならびに前向きコホート研究の結果を用いたメタ解析の結果、ニンニクの摂取量が最も高い人々の結腸直腸癌になるリスクは、ニンニク摂取量の最も低い人々よりも約30%低いことが示された(88)。同様に、イタリアおよびスイスで行われた症例対照研究のデータを解析したところ、ニンニクの摂取量が最も高い人々のリスクは、摂取量が最も低い人々よりも約26%低いことが示された(105)。結腸直腸腺腫(ポリープ)は前癌病変である。大人に対してS状結腸鏡検査を行った1つの症例対照研究によると、結腸直腸腺腫の人々は、結腸直腸腺腫がない人々に比べて有意にニンニクの摂取量が少ないことがわかった(106)。37名の結腸直腸腺腫の患者における小規模の予備的介入試験において、熟成ニンニク抽出物の12か月間の投与が腺腫のサイズや再発に影響するか否かが調べられた。高用量の投与患者(2.4 ml/day)は少量を投与した患者(0.16 ml/day)に比べて、腺腫の数およびサイズ共に有意に減少した(107,108)。ニンニクまたはニンニク抽出物が実質的に腺腫の再発を減少させるかどうかを決定するには、より大規模なランダム化比較試験が必要である。
要約:癌
ヒトを母集団とした疫学研究の結果は、ニンニクおよび他のAllium属の野菜の高摂取によって胃癌および結腸直腸癌を防止する助けとなりうることを示唆しているが、ニンニクの高摂取がヒトの各種の癌のリスクを低減できる証拠は限定的で一貫性が得られていない(88,109)。ニンニクおよび有機硫黄化合物は、動物モデルにおいて化学的に誘導された口腔癌、食道癌、胃癌、大腸癌、子宮癌、乳癌、前立腺癌(110)、皮膚癌(51)の進行を阻止することが示されてきたが、ニンニク由来の有機硫黄化合物がヒトの癌の進行を防いだり遅らせたりするかどうかは分からない。
供給源
食品による供給
ニンニク、タマネギを含むAllium属の野菜は、ヒトの食事における有機硫黄化合物の最も豊富な供給源である(109)。今日まで、有機硫黄化合物の健康に及ぼす効果に関する主な科学的研究は、ニンニク由来の化合物に焦点が当てられてきた。生のニンニクの鱗片には2-6 mg/gのγ-glutamyl-S-allylcysteine (新鮮重量の0.2-0.6%)および6-14 mg/gのアリイン (新鮮重量の0.6-14%)が含まれる。ニンニクの鱗片を破砕すると新鮮重量 1 g当たり2,500-4,500 mcg (= μg)のアリシンが得られる。新鮮なニンニクの鱗片1片の重さは2-4 gである(1)。
調理の効果
酵素アリイナーゼは加熱により失活させることができる。ある研究では、皮を剥かず破砕していないニンニクを電子レンジで加熱調理することで完全にアリイナーゼの活性が消失した(111)。あるin vitroの研究によると、オーブンで長時間(6 分間あるいはそれ以上)加熱あるいは煮ることで、破砕していないあるいは破砕したニンニクの血小板凝集に対する阻害効果が抑制されが、破砕したニンニクは破砕していないニンニクに比べて高い抗凝集活性を維持していた(112)。生ニンニクをラットに投与したところ、化学発癌物質によって誘導されたDNA損傷の量が有意に低減したが、破砕していないニンニクの鱗片を投与に先立ち電子レンジで60秒間、もしくは対流式オーブンで45 分間加熱したところ、ニンニクによるその保護作用が失われた(113)。ニンニクのDNA損傷に対する防御作用は、電子レンジでの60秒間の加熱の前に破砕し10 分間静置した場合、あるいは対流式オーブンの加熱の前に、ニンニクの鱗片の上部を切除し10 分間静置した場合には部分的に残存した。アリイナーゼが触媒する反応に由来する有機硫黄化合物がニンニクの生物学的効果に何らかの役割を果たしていると考えられるので、何人かの科学者達は、破砕あるいは刻んだニンニクを加熱調理する前に最低10 分間「静置」することを推奨している(111)。
サプリメント
いくつかの異なるタイプのニンニク製品が市販されており、製造工程によってそれぞれタイプが異なる組成の有機硫黄化合物が含まれる (下表を参照)。全てのニンニク製品が規格化されているわけではなく、規格化されているブランドにおいても、それらが含んでいる有機硫黄化合物の量と生物学的利用能に関しては変動する可能性がある(1)。
粉末(脱水)ニンニク
粉末あるいは脱水ニンニクは、通常、スライスされ低温で乾燥させることでアリイナーゼの失活を防止したニンニクの鱗片から作られている(114)。この乾燥ニンニクは微粉砕され、しばしば錠剤にもされている。合衆国薬局方(USP)の規格に適合するために、粉末ニンニクサプリメントは、0.1%以上のγ-glutamyl-S-allylcysteineおよび0.3%以上のアリイン(いずれも乾燥重量)を含まなければならない(115)。粉末ニンニクサプリメントは実際にはアリシンを含んでいないが、製造業者はそのサプリメントの「アリシンポテンシャル」あるいは「アリシン産生量」をラベルに表示してもよい。これらの値はサプリメントから得られるアリシンの最大値を示している(116)。これは粉末ニンニクを水に溶解させ室温で30 分後のアリシン含量を測定することで決定される(115)。アリイナーゼは胃の酸性pHにより不活性化されるので、ほとんどの粉末ニンニクの錠剤は腸溶性錠剤となっており、腸の中性pHに到達する前に溶解するのを防いでいる。薬剤の遊離を評価するUSP法を用いて、胃および腸を模した条件下で腸溶性錠剤からの“アリシンの遊離”を測定するのがより適切であると議論されている(115)。この方法によるアリシンの遊離は真の生物学的利用能と類似することが示されている(116)。ほとんどの錠剤ブランドにおいて、これらの条件ではわずかのアリシンしか産生されないことが分かっている。これは主に低いアリイナーゼ活性と長期の粉末化時間によるものである(116,117)。多くの製造業者は彼らの粉末ニンニクサプリメントの「アリシンポテンシャル」についての情報を提供しているが、「アリシンの遊離」についての情報を提供している製造業者は少ない。いくつもの対照臨床試験によって、粉末あるいは脱水ニンニクサプリメントが心血管リスク因子に及ぼす効果が調べられている(上述の心血管疾患を参照)。最も一般的に使用される投与量は600-900 mg/dayの間であり、これに含まれるアリシンの潜在量は3,600-5,400 mcg/day (= μg/day)である(63)。
ニンニク抽出液(熟成ニンニク抽出物TM)
ニンニクの鱗片をエタノールの水溶液中で最大20か月間インキュベートすると、アリシンは主に硫化アリル化合物に変換され、これらは蒸発して消失するか他の化合物に変換される(114)。こうして得られた抽出物には主にSAC、SAMCなどの水溶性有機硫黄化合物が含まれる(118)。熟成ニンニク抽出物を含むニンニク抽出液はそのS-allylcysteine含量で規格化されている。対照臨床試験において、熟成ニンニク抽出物を2.4-7.2 g/day投与することで、ex vivo (生体外)での血小板凝集が短期的に減少することが示され(11)、血清コレステロールのレベルを最長12週間、減少することも示された(119)。
水蒸気蒸留ニンニク油
粉砕ニンニク鱗片を水蒸気蒸留すると、DATS、DADSそしてDASを含む硫化アリル化合物を主成分とする製品が得られる(114)。これらの脂溶性の水蒸気蒸留製品は通常植物油に溶解されている。
ニンニク油漬け
粉砕ニンニク鱗片を油に漬け込み室温でインキュベートすると、DADSおよびDATS(1)などの硫化アリル化合物に加えて、アリシンからビニルジチイン類(vinyldithiins)およびアホエン(ajoene)が生成される。エーテル抽出を行うとニンニク油漬けと同様の組成の成分が得られるが、より高濃度である(76)。
安全性
悪影響
ニンニクおよびニンニクサプリメントを摂取した場合の最も一般的な悪影響は、息と体の悪臭である(63,120)。また、胸やけ、腹痛、吐き気、嘔吐、腹部膨満、下痢などの胃腸の症状も報告されている(121)。ニンニクの経口投与による最も深刻な悪影響は、出血が止まらなくなることである。ニンニクの投与に伴う、手術後あるいは突然の出血の例がいくつか医学書に報告されている(122-125)。仕事でニンニクの粉や粉末に曝される人々のなかで、喘息患者を含む一部の人々においてアレルギー反応を引き起こす例がある(126)。肌へのニンニクの暴露により接触性皮膚炎を引き起こす例がいくつか報告されている(120,127)。6時間以上のニンニクの局所暴露により、水膨れや炎症を含むさらに深刻な皮膚の病変もおこることが報告されている。
妊娠と授乳
食事によりニンニクを摂取した際の妊娠に及ぼす悪影響の結果については報告されていない。妊娠第3期のイランの女性が脱水ニンニク錠剤(800 mg/day)を2か月間服用したが妊娠に悪影響は見られなかった(128)。けれども、妊娠におけるニンニクサプリメントの安全性は確立してはいない。ニンニクの摂取により、母乳の臭いおよびおそらくフレーバーに変化が起こる証拠がいくつかある。1例の対照交差試験では、1.5 gのニンニク抽出物を経口摂取した授乳女性の母乳の臭いが強く感じられることが示された(129)。母親がニンニク抽出物を摂取した後では、プラセボを摂取した場合に比べて乳児の授乳に要する時間が長くなったが、母乳の消費量と授乳の回数に有意差はなかった。また、妊娠または授乳期間におけるニンニクの局所的使用が安全かどうかは分かっていない。
薬物相互作用
抗凝血薬
ニンニクはワルファリンwarfarin (クマディンCoumadin)の抗凝血作用を増加させる可能性がある。ワルファリン投与量や他の習慣を変えないで、ニンニク錠剤またはニンニク油の摂取を開始した患者においてプロトロンビン時間(INR)が延長されたという報告が2例ある(130)。しかし、最近の研究によると、ワルファリン治療を受けている厳密に監視された患者では、出血の危険性はニンニク抽出液(熟成ニンニク抽出物)では増加しなかった(131)。ニンニクサプリメントは血小板の凝集を阻害することが分かっているため(63)、多量の魚油やビタミンEなど血小板凝集を阻害する他の薬剤やサプリメントと一緒にニンニクサプリメントを摂取すると、何らかの付加的影響が生じる可能性が考えられる。ニンニクサプリメントが抗凝血治療を行っている人々に安全かどうかを決定するためにさらなる研究が必要である。
HIVプロテアーゼ阻害剤
健常ボランティアにニンニクのカプセル型錠剤(カプレット)を1日2回(アリシン産生量:7,200 mcg/day(= μg/day))3週間投与した結果、プロテアーゼ阻害剤サキナビルsaquinavir (Fortovase)の生物学的利用能が50%減少した(133)。サキナビルはCYP3A4 (肝チトクロームP450 3A4)により代謝されるが、2週間のニンニク抽出物の摂取により健常ボランティアのCYP3A4活性は有意に変化しなかった(134)。ニンニク抽出物の投与(10 mg/day)を4日間続けても、プロテアーゼ阻害剤、リトナビルritonavir (Norvir)の一回投与における薬物動態を有意に変化させなかった。しかし、よく知られたニンニクサプリメントとリトナビルの間の定常状態での相互作用を明らかにするためにさらなる研究が必要である(135)。
Authors and Reviewers
Originally written in 2005 by:
Jane Higdon, Ph.D.
Linus Pauling Institute
Oregon State University
Updated in July 2008 by:
Victoria J. Drake, Ph.D.
Linus Pauling Institute
Oregon State University
Reviewed in July 2008 by:
Larry D. Lawson, Ph.D.
Research Director, Silliker, Inc.
Orem, Utah
Copyright 2005-2026 Linus Pauling Institute
Figure Alternative Text
Figure 1. Some organosulfur compounds derived from garlic
The figure illustrates several organosulfur compounds derived from garlic, along with their chemical structures. On the left, γ-glutamyl-S-allylcysteine is converted to S-allylcysteine and then to S-allylmercaptocysteine. Alternatively, γ-glutamyl-S-allylcysteine is converted to allylcysteine sulfoxide, known as alliin. When garlic is crushed, alliin is converted by alliinase to form 2-propenesulfenic acid, which then forms allyl 2-propenethiosulfinate, known as allicin.
Figure 2. Some organosulfur compounds derived from the decomposition of allicin
The figure shows the decomposition of allicin and the resulting organosulfur compounds, with their chemical structures shown. At the top, allicin branches into two groups of products: The first group includes diallyl trisulfide (DATS), diallyl disulfide (DADS), diallyl sulfide (DAS), and trans-ajoene. The second group includes the cyclic vinyldithiins, 2-vinyl-4H-1,3-dithiin and 3-vinyl-4H-1,2-dithiin.
References
- Lawson LD. Garlic: a review of its medicinal effects and indicated active compounds. In: Lawson LD, Bauer R, eds. Phytomedicines of Europe: Chemistry and Biological Activity. Washington, D. C.: American Chemical Society; 1998:177-209.
- Block E. The chemistry of garlic and onions. Sci Am. 1985;252(3):114-119. (PubMed)
- Blumenthal M. Herb Sales Down 7.4 Percent in Mainstream Market. HerbalGram: American Botanical Council; 2005:63.
- Tapiero H, Townsend DM, Tew KD. Organosulfur compounds from alliaceae in the prevention of human pathologies. Biomed Pharmacother. 2004;58(3):183-193. (PubMed)
- Lawson LD, Wang ZJ. Allicin and allicin-derived garlic compounds increase breath acetone through allyl methyl sulfide: use in measuring allicin bioavailability. J Agric Food Chem. 2005;53(6):1974-1983. (PubMed)
- Germain E, Auger J, Ginies C, Siess MH, Teyssier C. In vivo metabolism of diallyl disulphide in the rat: identification of two new metabolites. Xenobiotica. 2002;32(12):1127-1138. (PubMed)
- Lachmann G, Lorenz D, Radeck W, Steiper M. [The pharmacokinetics of the S35 labeled labeled garlic constituents alliin, allicin and vinyldithiine]. Arzneimittelforschung. 1994;44(6):734-743. (PubMed)
- de Rooij BM, Boogaard PJ, Rijksen DA, Commandeur JN, Vermeulen NP. Urinary excretion of N-acetyl-S-allyl-L-cysteine upon garlic consumption by human volunteers. Arch Toxicol. 1996;70(10):635-639. (PubMed)
- Jandke J, Spiteller G. Unusual conjugates in biological profiles originating from consumption of onions and garlic. J Chromatogr. 1987;421(1):1-8. (PubMed)
- Kodera Y, Suzuki A, Imada O, et al. Physical, chemical, and biological properties of s-allylcysteine, an amino acid derived from garlic. J Agric Food Chem. 2002;50(3):622-632. (PubMed)
- Steiner M, Li W. Aged garlic extract, a modulator of cardiovascular risk factors: a dose-finding study on the effects of AGE on platelet functions. J Nutr. 2001;131(3s):980S-984S. (PubMed)
- Gebhardt R, Beck H. Differential inhibitory effects of garlic-derived organosulfur compounds on cholesterol biosynthesis in primary rat hepatocyte cultures. Lipids. 1996;31(12):1269-1276. (PubMed)
- Ferri N, Yokoyama K, Sadilek M, et al. Ajoene, a garlic compound, inhibits protein prenylation and arterial smooth muscle cell proliferation. Br J Pharmacol. 2003;138(5):811-818. (PubMed)
- Liu L, Yeh YY. S-alk(en)yl cysteines of garlic inhibit cholesterol synthesis by deactivating HMG-CoA reductase in cultured rat hepatocytes. J Nutr. 2002;132(6):1129-1134. (PubMed)
- Singh DK, Porter TD. Inhibition of sterol 4alpha-methyl oxidase is the principal mechanism by which garlic decreases cholesterol synthesis. J Nutr. 2006;136(3 Suppl):759S-764S. (PubMed)
- Chan KC, Hsu CC, Yin MC. Protective effect of three diallyl sulphides against glucose-induced erythrocyte and platelet oxidation, and ADP-induced platelet aggregation. Thromb Res. 2002;108(5-6):317-322. (PubMed)
- Lawson LD, Ransom DK, Hughes BG. Inhibition of whole blood platelet-aggregation by compounds in garlic clove extracts and commercial garlic products. Thromb Res. 1992;65(2):141-156. (PubMed)
- Blake GJ, Ridker PM. C-reactive protein and other inflammatory risk markers in acute coronary syndromes. J Am Coll Cardiol. 2003;41(4 Suppl S):37S-42S. (PubMed)
- Ali M, Thomson M, Afzal M. Garlic and onions: their effect on eicosanoid metabolism and its clinical relevance. Prostaglandins Leukot Essent Fatty Acids. 2000;62(2):55-73. (PubMed)
- Dirsch VM, Kiemer AK, Wagner H, Vollmar AM. Effect of allicin and ajoene, two compounds of garlic, on inducible nitric oxide synthase. Atherosclerosis. 1998;139(2):333-339. (PubMed)
- Kim KM, Chun SB, Koo MS, et al. Differential regulation of NO availability from macrophages and endothelial cells by the garlic component S-allyl cysteine. Free Radic Biol Med. 2001;30(7):747-756. (PubMed)
- Chang HP, Huang SY, Chen YH. Modulation of cytokine secretion by garlic oil derivatives is associated with suppressed nitric oxide production in stimulated macrophages. J Agric Food Chem. 2005;53(7):2530-2534. (PubMed)
- Keiss HP, Dirsch VM, Hartung T, et al. Garlic (Allium sativum L.) modulates cytokine expression in lipopolysaccharide-activated human blood thereby inhibiting NF-kappaB activity. J Nutr. 2003;133(7):2171-2175. (PubMed)
- Hedin U, Roy J, Tran PK. Control of smooth muscle cell proliferation in vascular disease. Curr Opin Lipidol. 2004;15(5):559-565. (PubMed)
- Campbell JH, Efendy JL, Smith NJ, Campbell GR. Molecular basis by which garlic suppresses atherosclerosis. J Nutr. 2001;131(3s):1006S-1009S. (PubMed)
- Golovchenko I, Yang CH, Goalstone ML, Draznin B. Garlic extract methylallyl thiosulfinate blocks insulin potentiation of platelet-derived growth factor-stimulated migration of vascular smooth muscle cells. Metabolism. 2003;52(2):254-259. (PubMed)
- Banerjee SK, Mukherjee PK, Maulik SK. Garlic as an antioxidant: the good, the bad and the ugly. Phytother Res. 2003;17(2):97-106. (PubMed)
- Dhawan V, Jain S. Effect of garlic supplementation on oxidized low density lipoproteins and lipid peroxidation in patients of essential hypertension. Mol Cell Biochem. 2004;266(1-2):109-115. (PubMed)
- Pryor WA, Houk KN, Foote CS, et al. Free radical biology and medicine: it's a gas, man! Am J Physiol Regul Integr Comp Physiol. 2006;291(3):R491-511. (PubMed)
- Lefer DJ. A new gaseous signaling molecule emerges: cardioprotective role of hydrogen sulfide. Proc Natl Acad Sci U S A. 2007;104(46):17907-17908. (PubMed)
- Benavides GA, Squadrito GL, Mills RW, et al. Hydrogen sulfide mediates the vasoactivity of garlic. Proc Natl Acad Sci U S A. 2007;104(46):17977-17982. (PubMed)
- Suarez F, Springfield J, Furne J, Levitt M. Differentiation of mouth versus gut as site of origin of odoriferous breath gases after garlic ingestion. Am J Physiol. 1999;276(2 Pt 1):G425-430. (PubMed)
- Yang CS, Chhabra SK, Hong JY, Smith TJ. Mechanisms of inhibition of chemical toxicity and carcinogenesis by diallyl sulfide (DAS) and related compounds from garlic. J Nutr. 2001;131(3s):1041S-1045S. (PubMed)
- Brady JF, Ishizaki H, Fukuto JM, et al. Inhibition of cytochrome P-450 2E1 by diallyl sulfide and its metabolites. Chem Res Toxicol. 1991;4(6):642-647. (PubMed)
- Jeong HG, Lee YW. Protective effects of diallyl sulfide on N-nitrosodimethylamine-induced immunosuppression in mice. Cancer Lett. 1998;134(1):73-79. (PubMed)
- Park KA, Kweon S, Choi H. Anticarcinogenic effect and modification of cytochrome P450 2E1 by dietary garlic powder in diethylnitrosamine-initiated rat hepatocarcinogenesis. J Biochem Mol Biol. 2002;35(6):615-622. (PubMed)
- Gurley BJ, Gardner SF, Hubbard MA, et al. Cytochrome P450 phenotypic ratios for predicting herb-drug interactions in humans. Clin Pharmacol Ther. 2002;72(3):276-287. (PubMed)
- Loizou GD, Cocker J. The effects of alcohol and diallyl sulphide on CYP2E1 activity in humans: a phenotyping study using chlorzoxazone. Hum Exp Toxicol. 2001;20(7):321-327. (PubMed)
- Munday R, Munday CM. Induction of phase II enzymes by aliphatic sulfides derived from garlic and onions: an overview. Methods Enzymol. 2004;382:449-456. (PubMed)
- Andorfer JH, Tchaikovskaya T, Listowsky I. Selective expression of glutathione S-transferase genes in the murine gastrointestinal tract in response to dietary organosulfur compounds. Carcinogenesis. 2004;25(3):359-367. (PubMed)
- Hatono S, Jimenez A, Wargovich MJ. Chemopreventive effect of S-allylcysteine and its relationship to the detoxification enzyme glutathione S-transferase. Carcinogenesis. 1996;17(5):1041-1044. (PubMed)
- Munday R, Munday CM. Relative activities of organosulfur compounds derived from onions and garlic in increasing tissue activities of quinone reductase and glutathione transferase in rat tissues. Nutr Cancer. 2001;40(2):205-210. (PubMed)
- Chen C, Pung D, Leong V, et al. Induction of detoxifying enzymes by garlic organosulfur compounds through transcription factor Nrf2: effect of chemical structure and stress signals. Free Radic Biol Med. 2004;37(10):1578-1590. (PubMed)
- Fisher CD, Augustine LM, Maher JM, et al. Induction of drug-metabolizing enzymes by garlic and allyl sulfide compounds via activation of constitutive androstane receptor and nuclear factor E2-related factor 2. Drug Metab Dispos. 2007;35(6):995-1000. (PubMed)
- Munday R, Munday CM. Low doses of diallyl disulfide, a compound derived from garlic, increase tissue activities of quinone reductase and glutathione transferase in the gastrointestinal tract of the rat. Nutr Cancer. 1999;34(1):42-48. (PubMed)
- Kweon S, Park KA, Choi H. Chemopreventive effect of garlic powder diet in diethylnitrosamine-induced rat hepatocarcinogenesis. Life Sci. 2003;73(19):2515-2526. (PubMed)
- Stewart ZA, Westfall MD, Pietenpol JA. Cell-cycle dysregulation and anticancer therapy. Trends Pharmacol Sci. 2003;24(3):139-145. (PubMed)
- Herman-Antosiewicz A, Singh SV. Signal transduction pathways leading to cell cycle arrest and apoptosis induction in cancer cells by Allium vegetable-derived organosulfur compounds: a review. Mutat Res. 2004;555(1-2):121-131. (PubMed)
- Knowles LM, Milner JA. Possible mechanism by which allyl sulfides suppress neoplastic cell proliferation. J Nutr. 2001;131(3s):1061S-1066S. (PubMed)
- Arunkumar A, Vijayababu MR, Srinivasan N, Aruldhas MM, Arunakaran J. Garlic compound, diallyl disulfide induces cell cycle arrest in prostate cancer cell line PC-3. Mol Cell Biochem. 2006;288(1-2):107-113. (PubMed)
- Wu X, Kassie F, Mersch-Sundermann V. Induction of apoptosis in tumor cells by naturally occurring sulfur-containing compounds. Mutat Res. 2005;589(2):81-102. (PubMed)
- Balasenthil S, Rao KS, Nagini S. Apoptosis induction by S-allylcysteine, a garlic constituent, during 7,12-dimethylbenz[a]anthracene-induced hamster buccal pouch carcinogenesis. Cell Biochem Funct. 2002;20(3):263-268. (PubMed)
- Balasenthil S, Rao KS, Nagini S. Garlic induces apoptosis during 7,12-dimethylbenz[a]anthracene-induced hamster buccal pouch carcinogenesis. Oral Oncol. 2002;38(5):431-436. (PubMed)
- Fenwick GR, Hanley AB. The genus Allium--Part 3. Crit Rev Food Sci Nutr. 1985;23(1):1-73. (PubMed)
- Harris JC, Cottrell SL, Plummer S, Lloyd D. Antimicrobial properties of Allium sativum (garlic). Appl Microbiol Biotechnol. 2001;57(3):282-286. (PubMed)
- Ankri S, Mirelman D. Antimicrobial properties of allicin from garlic. Microbes Infect. 1999;1(2):125-129. (PubMed)
- Cavallito CJ, Bailey JH. Allicin, the antibacterial principle of Allium sativum. I. Isolation, physical properties and antibacterial action. J Am Chem Soc. 1944;66(11):1950-1951.
- Martin KW, Ernst E. Herbal medicines for treatment of bacterial infections: a review of controlled clinical trials. J Antimicrob Chemother. 2003;51(2):241-246. (PubMed)
- Gail MH, Pfeiffer RM, Brown LM, et al. Garlic, vitamin, and antibiotic treatment for Helicobacter pylori: a randomized factorial controlled trial. Helicobacter. 2007;12(5):575-578. (PubMed)
- You WC, Brown LM, Zhang L, et al. Randomized double-blind factorial trial of three treatments to reduce the prevalence of precancerous gastric lesions. J Natl Cancer Inst. 2006;98(14):974-983. (PubMed)
- Ledezma E, Marcano K, Jorquera A, et al. Efficacy of ajoene in the treatment of tinea pedis: a double-blind and comparative study with terbinafine. J Am Acad Dermatol. 2000;43(5 Pt 1):829-832. (PubMed)
- Keys A. Wine, garlic, and CHD in seven countries. Lancet. 1980;1(8160):145-146. (PubMed)
- Ackermann RT, Mulrow CD, Ramirez G, Gardner CD, Morbidoni L, Lawrence VA. Garlic shows promise for improving some cardiovascular risk factors. Arch Intern Med. 2001;161(6):813-824. (PubMed)
- Alder R, Lookinland S, Berry JA, Williams M. A systematic review of the effectiveness of garlic as an anti-hyperlipidemic agent. J Am Acad Nurse Pract. 2003;15(3):120-129. (PubMed)
- Stevinson C, Pittler MH, Ernst E. Garlic for treating hypercholesterolemia. A meta-analysis of randomized clinical trials. Ann Intern Med. 2000;133(6):420-429. (PubMed)
- Berthold HK, Sudhop T, von Bergmann K. Effect of a garlic oil preparation on serum lipoproteins and cholesterol metabolism: a randomized controlled trial. JAMA. 1998;279(23):1900-1902. (PubMed)
- Gardner CD, Chatterjee LM, Carlson JJ. The effect of a garlic preparation on plasma lipid levels in moderately hypercholesterolemic adults. Atherosclerosis. 2001;154(1):213-220. (PubMed)
- Kannar D, Wattanapenpaiboon N, Savige GS, Wahlqvist ML. Hypocholesterolemic effect of an enteric-coated garlic supplement. J Am Coll Nutr. 2001;20(3):225-231. (PubMed)
- McCrindle BW, Helden E, Conner WT. Garlic extract therapy in children with hypercholesterolemia. Arch Pediatr Adolesc Med. 1998;152(11):1089-1094. (PubMed)
- Neil HA, Silagy CA, Lancaster T, et al. Garlic powder in the treatment of moderate hyperlipidaemia: a controlled trial and meta-analysis. J R Coll Physicians Lond. 1996;30(4):329-334. (PubMed)
- Turner B, Molgaard C, Marckmann P. Effect of garlic (Allium sativum) powder tablets on serum lipids, blood pressure and arterial stiffness in normo-lipidaemic volunteers: a randomised, double-blind, placebo-controlled trial. Br J Nutr. 2004;92(4):701-706. (PubMed)
- Zhang L, Gail MH, Wang YQ, et al. A randomized factorial study of the effects of long-term garlic and micronutrient supplementation and of 2-wk antibiotic treatment for Helicobacter pylori infection on serum cholesterol and lipoproteins. Am J Clin Nutr. 2006;84(4):912-919. (PubMed)
- van Doorn MB, Espirito Santo SM, Meijer P, et al. Effect of garlic powder on C-reactive protein and plasma lipids in overweight and smoking subjects. Am J Clin Nutr. 2006;84(6):1324-1329. (PubMed)
- Gardner CD, Lawson LD, Block E, et al. Effect of raw garlic vs commercial garlic supplements on plasma lipid concentrations in adults with moderate hypercholesterolemia: a randomized clinical trial. Arch Intern Med. 2007;167(4):346-353. (PubMed)
- Rahman K, Billington D. Dietary supplementation with aged garlic extract inhibits ADP-induced platelet aggregation in humans. J Nutr. 2000;130(11):2662-2665. (PubMed)
- Brace LD. Cardiovascular benefits of garlic (Allium sativum L). J Cardiovasc Nurs. 2002;16(4):33-49. (PubMed)
- Adler AJ, Holub BJ. Effect of garlic and fish-oil supplementation on serum lipid and lipoprotein concentrations in hypercholesterolemic men. Am J Clin Nutr. 1997;65(2):445-450. (PubMed)
- Auer W, Eiber A, Hertkorn E, et al. Hypertension and hyperlipidaemia: garlic helps in mild cases. Br J Clin Pract Suppl. 1990;69:3-6. (PubMed)
- Vorberg G, Schneider B. Therapy with garlic: results of a placebo-controlled, double-blind study. Br J Clin Pract Suppl. 1990;69:7-11. (PubMed)
- Koscielny J, Klussendorf D, Latza R, et al. The antiatherosclerotic effect of Allium sativum. Atherosclerosis. 1999;144(1):237-249. (PubMed)
- Siegel G, Klussendorf D. The anti-atheroslerotic effect of Allium sativum: statistics re-evaluated. Atherosclerosis. 2000;150(2):437-438. (PubMed)
- Budoff MJ, Takasu J, Flores FR, et al. Inhibiting progression of coronary calcification using Aged Garlic Extract in patients receiving statin therapy: a preliminary study. Prev Med. 2004;39(5):985-991. (PubMed)
- Vliegenthart R. Non-invasive assessment of coronary calcification. Eur J Epidemiol. 2004;19(12):1063-1072. (PubMed)
- Takezaki T, Gao CM, Ding JH, Liu TK, Li MS, Tajima K. Comparative study of lifestyles of residents in high and low risk areas for gastric cancer in Jiangsu Province, China; with special reference to allium vegetables. J Epidemiol. 1999;9(5):297-305. (PubMed)
- Buiatti E, Palli D, Decarli A, et al. A case-control study of gastric cancer and diet in Italy. Int J Cancer. 1989;44(4):611-616. (PubMed)
- Kim HJ, Chang WK, Kim MK, Lee SS, Choi BY. Dietary factors and gastric cancer in Korea: a case-control study. Int J Cancer. 2002;97(4):531-535. (PubMed)
- You WC, Blot WJ, Chang YS, et al. Allium vegetables and reduced risk of stomach cancer. J Natl Cancer Inst. 1989;81(2):162-164. (PubMed)
- Fleischauer AT, Poole C, Arab L. Garlic consumption and cancer prevention: meta-analyses of colorectal and stomach cancers. Am J Clin Nutr. 2000;72(4):1047-1052. (PubMed)
- Dorant E, van den Brandt PA, Goldbohm RA, Sturmans F. Consumption of onions and a reduced risk of stomach carcinoma. Gastroenterology. 1996;110(1):12-20. (PubMed)
- Lawson LD, Wang ZJ, Hughes BG. Identification and HPLC quantitation of the sulfides and dialk(en)yl thiosulfinates in commercial garlic products. Planta Med. 1991;57(4):363-370. (PubMed)
- Canizares P, Gracia I, Gomez LA, et al. Allyl-thiosulfinates, the bacteriostatic compounds of garlic against Helicobacter pylori. Biotechnol Prog. 2004;20(1):397-401. (PubMed)
- O'Gara EA, Hill DJ, Maslin DJ. Activities of garlic oil, garlic powder, and their diallyl constituents against Helicobacter pylori. Appl Environ Microbiol. 2000;66(5):2269-2273. (PubMed)
- Salih BA, Abasiyanik FM. Does regular garlic intake affect the prevalence of Helicobacter pylori in asymptomatic subjects? Saudi Med J. 2003;24(8):842-845. (PubMed)
- You WC, Zhang L, Gail MH, et al. Helicobacter pylori infection, garlic intake and precancerous lesions in a Chinese population at low risk of gastric cancer. Int J Epidemiol. 1998;27(6):941-944. (PubMed)
- Graham DY, Anderson SY, Lang T. Garlic or jalapeno peppers for treatment of Helicobacter pylori infection. Am J Gastroenterol. 1999;94(5):1200-1202. (PubMed)
- McNulty CA, Wilson MP, Havinga W, Johnston B, O'Gara EA, Maslin DJ. A pilot study to determine the effectiveness of garlic oil capsules in the treatment of dyspeptic patients with Helicobacter pylori. Helicobacter. 2001;6(3):249-253. (PubMed)
- Aydin A, Ersoz G, Tekesin O, Akcicek E, Tuncyurek M. Garlic oil and Helicobacter pylori infection. Am J Gastroenterol. 2000;95(2):563-564. (PubMed)
- Ernst E. Is garlic an effective treatment for Helicobacter pylori infection? Arch Intern Med. 1999;159(20):2484-2485. (PubMed)
- Hu JF, Liu YY, Yu YK, Zhao TZ, Liu SD, Wang QQ. Diet and cancer of the colon and rectum: a case-control study in China. Int J Epidemiol. 1991;20(2):362-367. (PubMed)
- Iscovich JM, L'Abbe KA, Castelleto R, et al. Colon cancer in Argentina. I: Risk from intake of dietary items. Int J Cancer. 1992;51(6):851-857. (PubMed)
- Levi F, Pasche C, La Vecchia C, Lucchini F, Franceschi S. Food groups and colorectal cancer risk. Br J Cancer. 1999;79(7-8):1283-1287. (PubMed)
- Dorant E, van den Brandt PA, Goldbohm RA. A prospective cohort study on the relationship between onion and leek consumption, garlic supplement use and the risk of colorectal carcinoma in The Netherlands. Carcinogenesis. 1996;17(3):477-484. (PubMed)
- Giovannucci E, Rimm EB, Stampfer MJ, Colditz GA, Ascherio A, Willett WC. Intake of fat, meat, and fiber in relation to risk of colon cancer in men. Cancer Res. 1994;54(9):2390-2397. (PubMed)
- Steinmetz KA, Kushi LH, Bostick RM, Folsom AR, Potter JD. Vegetables, fruit, and colon cancer in the Iowa Women's Health Study. Am J Epidemiol. 1994;139(1):1-15. (PubMed)
- Galeone C, Pelucchi C, Levi F, et al. Onion and garlic use and human cancer. Am J Clin Nutr. 2006;84(5):1027-1032. (PubMed)
- Witte JS, Longnecker MP, Bird CL, Lee ER, Frankl HD, Haile RW. Relation of vegetable, fruit, and grain consumption to colorectal adenomatous polyps. Am J Epidemiol. 1996;144(11):1015-1025. (PubMed)
- Tanaka S, Haruma K, Kunihiro M, et al. Effects of aged garlic extract (AGE) on colorectal adenomas: a double-blinded study. Hiroshima J Med Sci. 2004;53(3-4):39-45. (PubMed)
- Tanaka S, Haruma K, Yoshihara M, et al. Aged garlic extract has potential suppressive effect on colorectal adenomas in humans. J Nutr. 2006;136(3 Suppl):821S-826S. (PubMed)
- Bianchini F, Vainio H. Allium vegetables and organosulfur compounds: do they help prevent cancer? Environ Health Perspect. 2001;109(9):893-902. (PubMed)
- Arunkumar A, Vijayababu MR, Venkataraman P, Senthilkumar K, Arunakaran J. Chemoprevention of rat prostate carcinogenesis by diallyl disulfide, an organosulfur compound of garlic. Biol Pharm Bull. 2006;29(2):375-379. (PubMed)
- Song K, Milner JA. The influence of heating on the anticancer properties of garlic. J Nutr. 2001;131(3s):1054S-1057S. (PubMed)
- Cavagnaro PF, Camargo A, Galmarini CR, Simon PW. Effect of cooking on garlic (Allium sativum L.) antiplatelet activity and thiosulfinates content. J Agric Food Chem. 2007;55(4):1280-1288. (PubMed)
- Song K, Milner JA. Heating garlic inhibits its ability to suppress 7, 12-dimethylbenz(a)anthracene-induced DNA adduct formation in rat mammary tissue. J Nutr. 1999;129(3):657-661. (PubMed)
- Staba EJ, Lash L, Staba JE. A commentary on the effects of garlic extraction and formulation on product composition. J Nutr. 2001;131(3s):1118S-1119S. (PubMed)
- Dietary Supplements: Garlic. The United States Pharmacopeia. Vol 28. Rockville, MD: United States Pharmacopeial Convention, Inc.; 2005:2087-2092.
- Lawson LD, Wang ZJ. Low allicin release from garlic supplements: a major problem due to the sensitivities of alliinase activity. J Agric Food Chem. 2001;49(5):2592-2599. (PubMed)
- Lawson LD, Wang ZJ, Papadimitriou D. Allicin release under simulated gastrointestinal conditions from garlic powder tablets employed in clinical trials on serum cholesterol. Planta Med. 2001;67(1):13-18. (PubMed)
- Amagase H, Petesch BL, Matsuura H, Kasuga S, Itakura Y. Intake of garlic and its bioactive components. J Nutr. 2001;131(3s):955S-962S. (PubMed)
- Steiner M, Khan AH, Holbert D, Lin RI. A double-blind crossover study in moderately hypercholesterolemic men that compared the effect of aged garlic extract and placebo administration on blood lipids. Am J Clin Nutr. 1996;64(6):866-870. (PubMed)
- Borrelli F, Capasso R, Izzo AA. Garlic (Allium sativum L.): adverse effects and drug interactions in humans. Mol Nutr Food Res. 2007;51(11):1386-1397. (PubMed)
- Mulrow C, Lawrence V, Ackermann R, et al. Garlic: effects on cardiovascular risks and disease, protective effects against cancer, and clinical adverse effects: summary. Agency for Healthcare Research and Quality [Evidence Report/Technology Assessment No. 20]. October, 2000. Available at: http://www.ncbi.nlm.nih.gov/books/NBK11910/. Accessed 3/4/15.
- Burnham BE. Garlic as a possible risk for postoperative bleeding. Plast Reconstr Surg. 1995;95(1):213. (PubMed)
- Carden SM, Good WV, Carden PA, Good RM. Garlic and the strabismus surgeon. Clin Experiment Ophthalmol. 2002;30(4):303-304. (PubMed)
- German K, Kumar U, Blackford HN. Garlic and the risk of TURP bleeding. Br J Urol. 1995;76(4):518. (PubMed)
- Rose KD, Croissant PD, Parliament CF, Levin MB. Spontaneous spinal epidural hematoma with associated platelet dysfunction from excessive garlic ingestion: a case report. Neurosurgery. 1990;26(5):880-882. (PubMed)
- Anibarro B, Fontela JL, De La Hoz F. Occupational asthma induced by garlic dust. J Allergy Clin Immunol. 1997;100(6 Pt 1):734-738. (PubMed)
- Jappe U, Bonnekoh B, Hausen BM, Gollnick H. Garlic-related dermatoses: case report and review of the literature. Am J Contact Dermat. 1999;10(1):37-39. (PubMed)
- Ziaei S, Hantoshzadeh S, Rezasoltani P, Lamyian M. The effect of garlic tablet on plasma lipids and platelet aggregation in nulliparous pregnants at high risk of preeclampsia. Eur J Obstet Gynecol Reprod Biol. 2001;99(2):201-206. (PubMed)
- Mennella JA, Beauchamp GK. Maternal diet alters the sensory qualities of human milk and the nursling's behavior. Pediatrics. 1991;88(4):737-744. (PubMed)
- Sunter WH. Warfarin and garlic. Pharm J. 1991;246:722.
- Macan H, Uykimpang R, Alconcel M, et al. Aged garlic extract may be safe for patients on warfarin therapy. J Nutr. 2006;136(3 Suppl):793S-795S. (PubMed)
- Izzo AA, Ernst E. Interactions between herbal medicines and prescribed drugs: a systematic review. Drugs. 2001;61(15):2163-2175. (PubMed)
- Piscitelli SC, Burstein AH, Welden N, Gallicano KD, Falloon J. The effect of garlic supplements on the pharmacokinetics of saquinavir. Clin Infect Dis. 2002;34(2):234-238. (PubMed)
- Markowitz JS, Devane CL, Chavin KD, Taylor RM, Ruan Y, Donovan JL. Effects of garlic (Allium sativum L.) supplementation on cytochrome P450 2D6 and 3A4 activity in healthy volunteers. Clin Pharmacol Ther. 2003;74(2):170-177. (PubMed)
- Gallicano K, Foster B, Choudhri S. Effect of short-term administration of garlic supplements on single-dose ritonavir pharmacokinetics in healthy volunteers. Br J Clin Pharmacol. 2003;55(2):199-202. (PubMed)
免責事項
ライナスポーリング研究所微量栄養素情報センターは、一般向けの食事要因、健康面、栄養補助食品、食品および飲料に関する科学的情報を提供する。著者および出版社は、本サイト上の医学的、心理学的、栄養学的カウンセリングサービスを利用しないことを合意した上で、本情報を利用することができる。本情報は、有資格の医療従事者または栄養士への相談の代わりとして利用することはできない。
本ウェブサイトに掲載されている食事要因、栄養補助食品、食品および飲料に含まれる情報は、実施可能なすべての使用法、行為、使用上の注意、副作用、および相互作用を網羅するものではない。本ウェブサイトは、個々の問題についての栄養学的、医学的助言をすることは意図していない。本サイトの電子的に利用可能な情報に基づく個人的な行為、または不作為に対する責任は、明示的に否認される。
本ウェブサイトにおける著作権を有する資料のいずれも、複製、修正、配布、表示、発信、実行、公開または販売をおこなってはならない。本ウェブサイトにハイパーリンクを貼ることは可能であるが、その際には以下の文言を付記することとする。
「本リンクは、オレゴン州立大学ライナスポーリング研究所の提供するウェブサイトへ移動します。<<名前>>は、オレゴン州立大学ライナスポーリング研究所のアフィリエイトではなく、認証されたリンクでもありません」