塩(塩化ナトリウム)は生命に不可欠である。人体におけるナトリウムと塩化物の濃度を厳格に管理することは非常に重要なので、それらを制御するために複数のメカニズムが協働する。最低限の量の塩が生きるために必要であることは科学者も認めるところであるが、過剰な塩の摂取が健康に与える影響は、科学者、臨床医、および保健専門家の間で継続して研究がなされている分野である(1)。
機能
ナトリウムイオン(Na+:以下「ナトリウム」と称する)および塩化物イオン(Cl-:以下「塩化物」と称する)は、血漿を含む細胞外液の主要なイオンである。したがって、それらは多数の生命維持プロセスにおいて重要な役割を果たす(2)。
細胞膜電位の維持
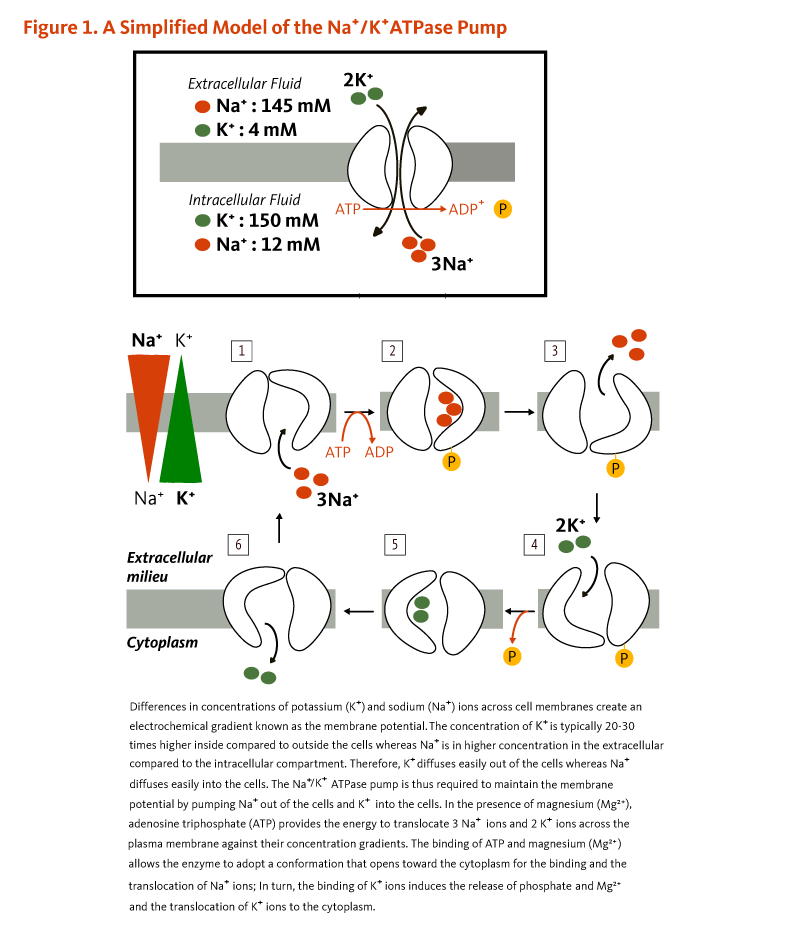
ナトリウムおよび塩化物は細胞膜の内外での濃度維持や電位差に寄与する電解物である。カリウムは細胞内で正の電荷を帯びたイオン(カチオン)の主たるものであり、ナトリウムは細胞外液での主なカチオンである。カリウムの濃度は細胞内では細胞外より約30倍も高い。一方で、ナトリウムは細胞内では細胞外より10倍以上も濃度が低い。細胞膜の内外でのカリウムとナトリウムの濃度差は、細胞膜電位として知られる電気化学的勾配を作り出す。細胞膜電位は、細胞膜のイオンポンプ、特にナトリウム-カリウムポンプによって維持される。これらのポンプは、カリウムと交換にナトリウムを細胞外に汲み出すためにATP(エネルギー)を使用する(下図参照)。その活動は、典型的な成人では安静時のエネルギー消費の20~40%を占めると推定される。ナトリウム/カリウムの濃度勾配の維持に使われるエネルギーの割合が多いということは、この機能が生命維持に重要であることの証である。細胞膜電位の厳密な制御は、神経インパルスの伝達、筋肉の収縮、および心機能にとって重要である。(3,4)
細胞壁を挟んでのカリウムイオンとナトリウムイオンの濃度差が、細胞膜電位として知られる電気化学的勾配を生む。アデノシン三リン酸(ATP)が、3つのナトリウムイオンを2つのカリウムイオンと交換に細胞の外に汲み出すエネルギーを提供し、細胞膜電位を維持する。
栄養素の吸収と輸送
小腸でのナトリウムの吸収は、塩化物、アミノ酸、ブドウ糖、および水分の吸収に重要な役割を果たす。同様のメカニズムは、これらの栄養素が腎臓によって血液から濾し取られた後でのこれらの栄養素の再吸収にも係る。塩酸(HCL)の形での塩化物は胃液の重要な成分でもあり、それは多くの栄養素の消化と吸収を助ける(2,5)。
血液量および血圧の維持
ナトリウムは血液量を含む細胞外液の量を決める主要な決定要因であるので、血液量や血圧を調整する数々の生理的メカニズムは、体内のナトリウム量を調整することによって機能する。循環器系では、圧力の受容体(圧受容器)が血圧の変化を感知し、興奮性または抑制性の信号を神経系および/または内分泌腺に送って、腎臓によるナトリウムの調整に作用する。一般に、ナトリウムの保持は水分の保持となり、ナトリウムの損失は水分の損失となる(4,5)。下にナトリウムの調整を介して血液量と血圧に影響する多くの系統の中から2つを記載する。
レニン-アンジオテンシン-アルドステロン系
血液量または血圧の著しい減少(重篤な失血または脱水など)に反応して、腎臓はレニンを放出して循環させる。レニンは、肝臓で作られる大きなタンパク質(アンジオテンシノーゲン)を小さなペプチド(アンジオテンシンI)に分割する酵素である。アンジオテンシンIは、血管内面、肺、肝臓、および腎臓にあるアンジオテンシン変換酵素(ACE)によってさらに小さいペプチド(アンジオテンシンII)に分割される。アンジオテンシンIIは小動脈の収縮を促し、その結果血圧が上昇する。アンジオテンシンIIは、副腎によるアルドステロンの合成も強く促す。アルドステロンはステロイドホルモンで、腎臓に作用してナトリウムの再吸収とカリウムの排泄を増やす。腎臓がナトリウムを保持することで水分も保持され、結果として血液量や血圧も上昇する(4)。
抗利尿ホルモン(ADH)
血液量や血圧の著しい減少は、脳下垂体後葉によるADHの分泌を促す。ADHは腎臓に作用して、水分の再吸収を増やす(4)。
欠乏症
ナトリウム(および塩化物)の欠乏は、たとえ非常に低塩分の食事をしていても、食事による摂取不足から起こることは一般にはない(5)。
低ナトリウム血症
血清ナトリウム濃度が136ミリモル/リットル未満の低ナトリウム血症は、体液保持の増進(希釈性の低ナトリウム血症)またはナトリウム損失の増加で起こることがある。希釈性の低ナトリウム血症は、抗利尿ホルモン(ADH)の分泌が不適切である可能性があり、中枢神経系に影響する障害や特定の薬(「薬物との相互作用」の項参照)の使用と関連している。時として、過剰な水分摂取も希釈性低ナトリウム血症を起こす可能性がある。ナトリウムや塩化物の損失を増やす条件は、激しかったり長引いたりする嘔吐や下痢、過剰で持続する発汗、抗利尿剤の使用、およびある種の腎臓病などである。低ナトリウム血症の症状は、頭痛、吐き気、嘔吐、筋肉の痙攣、疲労、見当識障害(方向感覚の喪失)、および失神である。重篤で急に発症する低ナトリウム血症の合併症として、脳水腫(脳のはれ)、脳卒中、昏睡、および脳損傷などがある。急性または重篤な低ナトリウム血症は、迅速で適切な医療的処置がなされないと、致命的になることもある(6)。
長時間の持久運動と低ナトリウム血症
マラソン、ウルトラマラソン、鉄人トライアスロンレースなどの非常に長時間の持久競技に参加する個人にとって、低ナトリウム血症は潜在的な問題であると最近では認知されている。1997年に鉄人レースに参加した650人のうち25人(ほぼ4%)が、低ナトリウム血症で治療を受けた。鉄人レースで低ナトリウム血症を起こした参加者は、比較的控えめな水分補給にもかかわらず水分過負荷の症状を示していた。このことから水分排出が不十分だったこと、および/またはこれらの超長距離アスリートは現在推奨されているよりも水分需要が低い可能性がうかがわれる(8)。非ステロイド性抗炎症薬(NSAID)の使用が、水分の排泄を損なうことで運動関連の低ナトリウム血症のリスクを高めているのではないか(9)と疑われているが、確固たる根拠は現在のところない。
ナトリウムの目安量(AI)
2004年に米国医学研究所の食品栄養委員会は、適度に活動的な人々が汗として損失するナトリウムを補充し、その他の必須栄養素を十分に摂れる食事を実現するのに必要な量に基づいて、ナトリウム摂取の目安量(AI)を設定した(5)。この推奨量は、ほとんどの米国民が平均的食事から摂取する量をはるかに下回っている。
疾病の予防(食事に含まれるナトリウムと疾病)
胃がん
主にアジアの国々で行われた疫学調査では、塩漬け、燻製、および塩酢漬けの食品摂取が多いと、胃がんのリスクが高まることが示された(10,11)。これらの食品は塩分が高く、ニトロソアミンのような発がん性物質も含んでいる可能性がある。ニトロソアミンとがんについての詳細は、ライナス・ポーリング研究所の2000年秋/冬リサーチ・ニュースレター(Research Newsletter)の記事を参照されたい。さらに、塩漬け食品の摂取が多い集団は、胃がん予防によい果物や野菜の摂取が少ない傾向がある(12)。胃がんのリスクは、胃の慢性的な炎症やヘリコバクター・ピロリ菌の感染によって高まる。高濃度の塩分は胃の内側の細胞を傷つけ、ピロリ菌の感染やがんを促しやすい遺伝子損傷のリスクを潜在的に高める可能性がある。塩そのものが発がん性物質だという根拠はほとんどないが、特定の塩漬け食品、たとえば塩漬けの魚などをたくさん摂取することは、胃がんになりやすい個人のリスクを高めるかもしれない(11,13,14)。
骨粗しょう症
骨粗しょう症は多因子的な骨障害で、骨の強度が損なわれ、その結果骨折のリスクが高まる。栄養は、骨粗しょう症の発症と進行に関与する多数の要素の中の一つである。塩分摂取が多いと、カルシウムの尿中への排泄が増えることがわかっている。腎臓から排泄されるナトリウム2.3gごと(塩(塩化ナトリウムNaCl)では5.8gごと)に、約24~40ミリグラム(mg)のカルシウムが尿に出て行く(15)。塩分摂取が骨の再吸収の生化学的マーカーと関連しているとする研究もあるが、そうではないものもある。一般に、横断研究ではナトリウム摂取と骨密度(BMD)の関連は見つかっていない(16)。しかしながら、閉経後の女性を2年間調べた研究では、尿中ナトリウム排泄(ナトリウム摂取の指標)の増加と、腰部のBMDの減少という関連が見られた(17)。さらに最近では、40人の閉経後女性の縦断的研究で、6ヶ月間低塩分の食事(2g/日)に固執すると、ナトリウムの排泄、カルシウムの排泄、および骨の再吸収のバイオマーカーであるI型コラーゲンのアミノ末端プロペプチドに著しい減少が見られた。しかしこれらの関連は、基線尿中ナトリウム排泄が3.4g/日(米国成人の平均的ナトリウム摂取量)以上の女性にのみ見られた(18)。塩分摂取を減少させることが、骨粗しょう症のリスクのある個人のBMDや骨折リスクに臨床的に意義のある効果があるかどうかを決定する長期の前向き研究が必要である。骨粗しょう症についての詳細は、「カルシウム」の記事を参照されたい。
腎結石
腎結石の大半は、カルシウムを主要成分とする。その原因はしばしば不明であるが、尿中カルシウムが異常に高くなる(高カルシウム尿症)と、カルシウム結石発症のリスクが高まる(19)。食事からの塩分摂取が増えると、尿中へのカルシウムの排泄が増えることが知られており、カルシウムを含んだ腎結石の病歴のある患者にはこの効果がより顕著である可能性がある(20)。9万人以上の女性を12年間にわたって追跡した大規模な前向き研究では、ナトリウムの摂取が平均4.9g/日(塩では12.6g/日)の女性は、平均1.5g/日のナトリウム(塩では4.0g/日)を摂取する女性よりも、腎結石の兆候の発症リスクが30%高かった(21)。しかし、男性を対象とした同様の研究では、ナトリウムの摂取と腎結石の兆候との間に相関は見られなかった(22)。臨床的研究では、ナトリウムの摂取を制限すると、カルシウム結石のできやすい個人の尿中カルシウムの量が減った(23)。また、再発性シュウ酸カルシウム結石の男性に2種類の異なった食事を与えた5年間の無作為化試験では、塩分と動物性タンパク質を控えた食事は、低カルシウムの食事よりも結石の再発を著しく減らすことがわかった(24)。
高血圧
数十年にわたって行われた複数連の研究で、ナトリウムの摂取と血圧の因果関係が示唆されてきた。動物研究は、この関係についての生理学的情報を多く提供している。特に重要なのは、ヒトの近接種であるチンパンジーの大人26匹に行われた主要な動物実験で、ナトリウムの濃度を実験的に高くしたり低くしたりした結果、血圧が上下したことが示され、ナトリウムの摂取が多いと血圧が上がり、低いと血圧も下がることの強力な根拠となった(25)。
ヒトでは、非常に低塩分な食事の文化を持つ人々と高塩分な食事の文化を持つ人々とを比べた異文化集団間の研究や、大半が横断的研究である観察研究の結果、塩の消費の増大と血圧の上昇の関連が示唆されている。しかし、異文化間研究に使われる集団群は血圧に影響するかもしれないその他のたくさんの点で異なっている可能性があり、観察研究は紛らわしい要素をコントロールする技量がまちまちである(26)。ナトリウムと血圧に関する最も大規模で最も厳密に計画された観察研究はインターソルト(INTERSALT)であり、32カ国で1万人以上の男女を研究した。集団横断的分析および集団内分析のどちらにおいても同じ結論が支持されており、24時間の尿採取で測定されたナトリウムの摂取と血圧には相関があった(27)。より高度な統計技術を用いたその後の分析は、この相関を以前報告されていたよりもさらにもっと強くしている(28)。
血圧に対する減塩の効果についての臨床試験とメタ解析
多くの無作為化臨床試験では、高血圧および非高血圧(非高血圧の血圧は現在では前高血圧と呼ばれる血圧の範囲を含むので、非高血圧は必ずしも正常血圧ではないことに注意)の人々を対象に、食事の減塩が血圧に及ぼす効果を調べてきた。中には、多くの異なった試験で集まったデータを分析するメタ解析と呼ばれる技法を用いて、食事の減塩が血圧にもたらす効果の大きさを推定したものもある(29-34)。様々なメタ解析に含まれる試験の数やタイプは実質的に異なっているが、食事の減塩が血圧にもたらす効果の大きさの推定は、解析結果で大きな差はない。コクラン・メタ解析は高血圧の参加者による20の試験と、高血圧でない参加者の11の試験から中程度の減塩の結果を評価した。中程度の減塩(24時間尿中ナトリウム排泄に基づく1.7~1.8g/日のナトリウムの減少)によって、収縮期血圧(最高血圧)/拡張期血圧(最低血圧)が、高血圧の参加者で平均で5.1/2.7mmHg、高血圧でない参加者で平均2.0/1.0mmHg減った(34)。
特に重要なのはTONE(35)およびTOHP-Phase II(36)と呼ばれる2つの大規模長期(2年以上の期間)試験の結果で、臨床および公衆衛生活動に最も関連があるものである。TONEでは、中程度の約1.0g/日のナトリウム摂取の減少で、始めは血圧の投薬を受けていた中高年の高血圧をより良くコントロールできることが示された。TOHP -Phase II(2つの高血圧予防試験のうちの2つ目の試験)は、同じ程度のナトリウム摂取の減少で、高血圧でない肥満の参加者の最高/最低血圧が1.2/1.6mmHg減っただけでなく、4年後には高血圧の発症が14%減ったことを示した(36)。高血圧の参加者の血圧減少値がささやかであることに疑問を呈する臨床医もいるが、観察研究および無作為化試験の概要では、米国人が平均2mmHg最低血圧を下げれば高血圧の蔓延が17%抑えられ、心臓発作のリスクが5%減り、脳卒中のリスクも15%減る(37)。したがって、血圧が平均してささやかに減少しただけでも、米国人全体の公衆衛生に大きな利益となる可能性がある。
食事に含まれるナトリウムの変化に対する反応の変動:塩への感受性
ナトリウム摂取の短期的変化による血圧反応の変動に関する文献は相当量ある(38,39)。しかし、たいていはたったの1回しか行われない実験用手順に従って塩分変化に対する血圧の反応を基に個人を分類することは、非常に問題である。大部分の生理的反応と同様に、塩分摂取変化に対する血圧反応は、連続的にほぼ正規分布を示す(40)。食事に変化がなかった時でも、日々の血圧は変動する(40)。個人を塩分に敏感であるとか抵抗性があると分類するのは、今のところでは集団のサンプルに基いていないし、経時的によく再現できるとは未だに示されていない。加えて、「塩分への感受性」の研究に使われる手順のほとんどでは、数日から1週間という短期間に極端な塩分摂取の操作(ナトリウム過剰および欠乏)を行う。これらの非常に短期間の研究が、長期間にわたって徐々に穏やかに変化する塩分摂取による血圧変化に関連するという根拠はない。にもかかわらず、集団内の特定の部分集団では、ナトリウム摂取の変化に平均血圧の反応が大きい傾向がある。それらの人々はすでに高血圧であったり、より高齢であったり、アフリカ系の米国人であったりする(41)。塩分への感受性に対する遺伝的根拠の研究から、ゆくゆくは塩分への感受性に関してより良くて信頼性のある個人分類ができるようになる可能性がある。多形性として知られる特定の遺伝子の共通変異が現在調査されており、これにはレニン-アンジオテンシン-アルドステロン系(「機能」の項参照)において顕著に機能する生産物を作る遺伝子の共通変異が含まれる(42)。さらに、食事の質(たとえば下のDASH食)と体重減少も、血圧を減少させる(43-45)。したがって、遺伝的要因に加えて環境的影響が塩分への感受性に影響しているようである。
食事のパターンと血圧(DASH 試験)
DASH(高血圧防止の食事療法)試験という名称の、多機関による無作為化摂食研究は、果物、野菜、精白されていない穀物、家禽、魚、木の実、および低脂肪乳製品を多く摂る食事が、典型的な米国の食事に比べて、高血圧および非高血圧の人々の血圧を実質的に低下させた(高血圧の人の最高/最低血圧で11.4mmHg/5.5mmHg、非高血圧の人では3.5/2.1mmHg)ことを示した(46)。DASH食は、典型的な米国の食事よりもカリウムとカルシウムが顕著に多く、タンパク質はやや多めで、総脂肪、飽和脂肪、およびコレステロールが低めである。しかし、ナトリウム以外の食事成分の効果をよりよく評価するために、研究ではナトリウムの濃度は一定に保たれた。その後DASHナトリウム試験では、DASH 食と典型的な米国の食事(対照食)を、塩分摂取が低(2.9g/日)、中(米国の食事指針で上限として推奨されている5.8g/日)、高(米国で典型的摂取量である8.7g/日)という3レベルに分けて比較した(47)。DASH食は、対照食に比べてどの塩分摂取レベルでも高血圧および非高血圧の人々の最高および最低血圧を著しく低下させた。塩分摂取の減少は、最高および最低血圧をさらに下げることになったのだ。DASH食と減塩は、どちらもそれ単独で行うよりも、組み合わせるとさらに血圧を下げたということである。高塩分の対照食と比べて、低ナトリウムのDASH食を摂った人の平均血圧は8.9/4.5mmHg下がった。これは、対照食での減塩効果はDASH食よりも高く、典型的な米国の食事をしている人々には減塩がより有益である可能性を示唆している。DASH試験の結果は、健康的な食事パターンが高血圧の予防および治療に効果的な方法であるという考えを支持している(48)。さらに、88,517人の中年女性を24年間追跡した前向きコホート研究で、DASH式の食事に固執すると冠動脈性心疾患と脳卒中のリスクが著しく低下することがわかった(49)。DASH食の詳細情報は、米国国立衛生研究所(NIH)の国立心肺血液研究所(NHLBI)から入手可能である。
米国の高血圧教育プログラムおよびNIHの国立心肺血液研究所は、塩の摂取を6g/日以下にするよう勧めており(50)、米国医学研究所の食品栄養委員会は最近、成人は5.8g/日以下の塩分摂取に留めるよう勧めている(5)(「安全性」の項参照)。塩分摂取に関する米国の食事指針の詳細用に、高血圧教育プログラムの記載および国立心肺血液研究所のナトリウムと血圧に関するワークショップの所見の要約がオンラインで閲覧可能である。
標的臓器の損傷
慢性的な高血圧は、心臓、血管、および腎臓を損傷し、それによって心臓疾患や脳卒中、さらには高血圧性腎臓疾患のリスクを高める。いくつかの臨床研究では、塩分摂取は左心室肥大という異常な心筋の肥厚と著しく相関があり、これは心血管疾患による死亡率の上昇と関連がある(51)。最近の研究は、高塩分摂取が血圧への影響とは別の意味で臓器の損傷に関与しているいう可能性を示している(52-54)。たとえば、動物およびヒトでの研究で、塩分摂取の増加が血圧の変化とは無関係の太い弾性動脈の構造と機能の病理変化と関連があることがわかっている(55)。
心血管疾患(CVD)
ナトリウム摂取の減少が心血管疾患および死亡率にもたらす効果を調べた研究は少なく、まちまちの結果となっている(56-61)。一般に、それらの研究では直接の関連が示唆され、特に尿中ナトリウムをナトリウム摂取の測定法として使用した研究ではそうであった(56-58)。TONE研究ではナトリウムを減らすように割り当てられた参加者の心血管疾患の減少傾向が見られた(35)。重要なのは、以前の2つのTOHP試験でナトリウム摂取の介入試験に参加したもともと高血圧でなかった人々は、対照群と比べて10~15年後に心血管疾患の発症が25%減ったことが最近の研究でわかったことである(62)。このTOHPの追跡研究をその後分析したところ、ナトリウム-カリウムの比率が容量-反応関係における心血管疾患のリスク上昇と関係があることがわかり、ナトリウムの摂取と心血管疾患の間の有害な関連を補完する証拠となっている。
摂取源
食事に含まれるナトリウムも塩化物も、大部分は塩に由来する。米国での塩の摂取の75%は、食事時にかけたり料理の際に入れたりする塩ではなく、食品の加工や製造の過程で添加される塩に由来する。最も少ない塩分摂取に関連しているのは、加工されていない食品、特に果物、野菜、豆類などを重視する食事である。最近の調査で、米国の食事からの平均塩分摂取は、成人男性で7.8~11.8g/日で、成人女性で5.8~7.8g/日であるとわかった(5)。これらの数字は、食事時に食べ物にかける塩を含んでいないので、少なめの見積もりである可能性がある。
下の表は、塩分を多く含んでいる食品、および比較的塩分の少ない食品のナトリウム含有量(ミリグラム(mg)表示)を示す。ナトリウムと塩化物の多くが塩に由来するので、食事に含まれる塩の含有量は、ナトリウムの含有量を2.5倍することで推定できる。
例:ナトリウム2,000mg(2g)×2.5 = 塩5,000mg(5g)
食品の栄養素量についての詳細は、USDAの食品成分データベースを検索されたい。
安全性
毒性
塩化ナトリウムの過剰摂取は、正常なナトリウム濃度を維持するために水分が細胞から引き出されて、細胞外液の体積増加につながる。しかし、水分が需要どおりに摂取できる限り、正常に働いている腎臓ならば過剰なナトリウムを排泄して身体を正常な状態に戻す(50)。大量の塩の摂取は、吐き気、嘔吐、下痢、および異常な痙攣を起こす可能性がある(64)。異常に高い血漿ナトリウム濃度(高ナトリウム血症)は、一般的に過剰な水分損失から始まり、渇きのメカニズムが損なわれていたり水が摂取できなかったりする状況を伴うことがよくある。過剰な体液の損失を伴う高ナトリウム血症の症状は、めまいや失神、低血圧、および尿生産の減少などを含むことがある。深刻な高ナトリウム血症は、浮腫(腫れ上がること)、高血圧、動悸、呼吸困難、痙攣、昏睡、および死亡に至る可能性がある。高ナトリウム血症は、ナトリウムの過剰摂取(たとえば海水の多量摂取や高濃度食塩水の静脈注射など)で起きることはまれである。末期腎不全では、塩分と水分の摂取が制限されないと、尿へのナトリウム排泄が損なわれることで体液貯留となり、その結果として浮腫、高血圧、うっ血性心不全となる可能性がある(2,65)。
悪影響
2004年に、米国医学研究所の食品栄養委員会は、心血管疾患および腎臓疾患の主要なリスク要因である高ナトリウム摂取が血圧に及ぼす悪影響に基いて、ナトリウム摂取の許容上限摂取量(UL)を成人で2.3g/日(塩では5.8g/日)と設定した(5)。中高年、アフリカ系アメリカ人、および高血圧、糖尿病、または慢性腎臓病の個人を含むナトリウムの血圧への影響に最も敏感な人々には、ナトリウムの許容上限摂取量がさらに少ない可能性があることを留意すべきである。ナトリウムおよび塩の許容上限摂取量の値を年齢層ごとに下の表に示す。
| 年齢層 | ナトリウムのUL(g/日) | 塩(g/日) |
|---|---|---|
| 乳児(0-12ヶ月) | 未決定* | 未決定* |
| 幼児(1-3歳) | 1.5 | 3.8 |
| 子供(4-8歳) | 1.9 | 4.8 |
| 子供(9-13歳) | 2.2 | 5.5 |
| 青少年(14-18歳) | 2.3 | 5.8 |
| 成人(19歳以上) | 2.3 | 5.8 |
| *食品および人口乳からのみ摂取。 | ||
薬物相互作用
以下の薬物は、低ナトリウム血症(異常に低い血中ナトリウム濃度)のリスクを高める可能性がある(6)。
ライナス・ポーリング研究所の推奨
比較的低塩分(5.8g/日以下)で高カリウム(少なくとも4.7g/日)の食事が、高血圧やそれに関連する心血管疾患や腎臓病のリスク低下と相関があることを示す強力で一貫した根拠がある。加えてDASH試験では、果物、野菜、精白されていない穀物、木の実、および低脂肪乳製品を多く摂る食事が実質的に血圧を減少させることが示された。この効果は塩分摂取を5.8g/日以下にすることで強められ、3.8g/日に抑えることで最も強化される。塩分摂取を3.8g/日までに限ることを目標にすべきである。ライナス・ポーリング研究所は、果物および野菜(少なくとも5品目/日)が豊富で、塩分の多い加工食品を限定する食事を推奨する。
中高年(50歳以上)
低塩分(3.8g/日以下)で高カリウム(少なくとも4.7g/日)の食事が、高血圧およびそれに関連する心血管疾患および腎臓疾患のリスクが高い中高年にとって、特に有益であると思われる。塩が血圧を上げる効果への感受性は年とともに上昇するので、低塩分で高カリウムの食事は中高年に特に有益である可能性がある。
Authors and Reviewers
Originally written in 2001 by:
Jane Higdon, Ph.D.
Linus Pauling Institute
Oregon State University
Updated in February 2004 by:
Jane Higdon, Ph.D.
Linus Pauling Institute
Oregon State University
Updated in November 2008 by:
Victoria J. Drake, Ph.D.
Linus Pauling Institute
Oregon State University
Reviewed in November 2008 by:
Eva Obarzanek, Ph.D, M.P.H., R.D.
Research Nutritionist (Retired)
Prevention and Population Sciences Program
Division of Cardiovascular Sciences
National, Heart, Lung, and Blood Institute (NHLBI)
Copyright 2001-2026 Linus Pauling Institute
Figure Alternative Text
Figure 1. A simplified model of the Na+/K+ATPase pump
The figure illustrates how the Na+/K+ ATPase pump maintains membrane potential by actively transporting ions across the plasma membrane. Sodium (Na+) concentration is 145 mM outside the cell and 12 mM inside the cell, while potassium (K+) is 4 mM outside the cell and 150 mM inside the cell. The Na+/K+ATPase pump uses ATP to transport three sodium ions out of the cell and two potassium ions into the cell. The figure shows the pump cycle, with ATP binding, phosphorylation, conformational changes in the enzyme, and ion exchange between the extracellular milieu and cytoplasm.
References
- Taubes G. The (political) science of salt. Science. 1998;281(5379):898-901, 903-897. (PubMed)
- Harper ME, Willis JS, Patrick J. Sodium and chloride in nutrition. In: O'Dell BL, Sunde RA, eds. Handbook of nutritionally essential minerals. New York: Marcel Dekker; 1997:93-116.
- Brody T. Nutritional Biochemistry. 2nd ed. San Diego: Academic Press; 1999.
- Sheng H-W. Sodium, chloride and potassium. In: Stipanuk M, ed. Biochemical and Physiological Aspects of Human Nutrition. Philadelphia: W.B. Saunders Company; 2000:686-710.
- Food and Nutrition Board, Institute of Medicine. Sodium and Chloride. Dietary Reference Intakes for Water, Potassium, Sodium, Chloride, and Sulfate. Washington, D.C.: National Academies Press; 2005:269-423. (The National Academies Press)
- Adrogue HJ, Madias NE. Hyponatremia. N Engl J Med. 2000;342(21):1581-1589.
- Speedy DB, Rogers IR, Noakes TD, et al. Diagnosis and prevention of hyponatremia at an ultradistance triathlon. Clin J Sport Med. 2000;10(1):52-58. (PubMed)
- Speedy DB, Noakes TD, Kimber NE, et al. Fluid balance during and after an ironman triathlon. Clin J Sport Med. 2001;11(1):44-50. (PubMed)
- Ayus JC, Varon J, Arieff AI. Hyponatremia, cerebral edema, and noncardiogenic pulmonary edema in marathon runners. Ann Intern Med. 2000;132(9):711-714. (PubMed)
- Palli D. Epidemiology of gastric cancer: an evaluation of available evidence. J Gastroenterol. 2000;35 Suppl 12:84-89. (PubMed)
- Tsugane S. Salt, salted food intake, and risk of gastric cancer: epidemiologic evidence. Cancer Sci. 2005;96(1):1-6. (PubMed)
- Liu C, Russell RM. Nutrition and gastric cancer risk: an update. Nutr Rev. 2008;66(5):237-249. (PubMed)
- Cohen AJ, Roe FJ. Evaluation of the aetiological role of dietary salt exposure in gastric and other cancers in humans. Food Chem Toxicol. 1997;35(2):271-293. (PubMed)
- Hirohata T, Kono S. Diet/nutrition and stomach cancer in Japan. Int J Cancer. 1997;Suppl 10:34-36. (PubMed)
- Weaver CM, Heaney RP. Calcium. In: Shils M, Olson JA, Shike M, Ross AC, eds. Modern Nutrition in Health and Disease. 9th ed. Baltimore: Williams & Wilkins;1999:141-155.
- Cohen AJ, Roe FJ. Review of risk factors for osteoporosis with particular reference to a possible aetiological role of dietary salt. Food Chem Toxicol. 2000;38(2-3):237-253. (PubMed)
- Devine A, Criddle RA, Dick IM, Kerr DA, Prince RL. A longitudinal study of the effect of sodium and calcium intakes on regional bone density in postmenopausal women. Am J Clin Nutr. 1995;62(4):740-745. (PubMed)
- Carbone LD, Barrow KD, Bush AJ, et al. Effects of a low sodium diet on bone metabolism. J Bone Miner Metab. 2005;23(6):506-513. (PubMed)
- Heller HJ. The role of calcium in the prevention of kidney stones. J Am Coll Nutr. 1999;18(5 Suppl):373S-378S. (PubMed)
- Audran M, Legrand E. Hypercalciuria. Joint Bone Spine. 2000;67(6):509-515. (PubMed)
- Curhan GC, Willett WC, Speizer FE, Spiegelman D, Stampfer MJ. Comparison of dietary calcium with supplemental calcium and other nutrients as factors affecting the risk for kidney stones in women. Ann Intern Med. 1997;126(7):497-504. (PubMed)
- Curhan GC, Willett WC, Rimm EB, Stampfer MJ. A prospective study of dietary calcium and other nutrients and the risk of symptomatic kidney stones. N Engl J Med. 1993;328(12):833-838. (PubMed)
- Assimos DG, Holmes RP. Role of diet in the therapy of urolithiasis. Urol Clin North Am. 2000;27(2):255-268. (PubMed)
- Borghi L, Schianchi T, Meschi T, et al. Comparison of two diets for the prevention of recurrent stones in idiopathic hypercalciuria. N Engl J Med. 2002;346(2):77-84. (PubMed)
- Denton D, Weisinger R, Mundy NI, et al. The effect of increased salt intake on blood pressure of chimpanzees. Nat Med. 1995;1(10):1009-1016. (PubMed)
- Elliott P. Observational studies of salt and blood pressure. Hypertension. 1991;17(1 Suppl):I3-8. (PubMed)
- Intersalt Cooperative Research Group. Intersalt: an international study of electrolyte excretion and blood pressure. Results for 24 hour urinary sodium and potassium excretion. BMJ. 1988;297(6644):319-328. (PubMed)
- Elliott P, Stamler J, Nichols R, et al. Intersalt revisited: further analyses of 24 hour sodium excretion and blood pressure within and across populations. Intersalt Cooperative Research Group. BMJ. 1996;312(7041):1249-1253. (PubMed)
- He FJ, MacGregor GA. Importance of salt in determining blood pressure in children: meta-analysis of controlled trials. Hypertension. 2006;48(5):861-869. (PubMed)
- Dickinson HO, Mason JM, Nicolson DJ, et al. Lifestyle interventions to reduce raised blood pressure: a systematic review of randomized controlled trials. J Hypertens. 2006;24(2):215-233. (PubMed)
- Graudal NA, Galloe AM, Garred P. Effects of sodium restriction on blood pressure, renin, aldosterone, catecholamines, cholesterols, and triglyceride: a meta-analysis. JAMA. 1998;279(17):1383-1391. (PubMed)
- Cutler JA, Follmann D, Allender PS. Randomized trials of sodium reduction: an overview. Am J Clin Nutr. 1997;65(2 Suppl):643S-651S. (PubMed)
- Midgley JP, Matthew AG, Greenwood CM, Logan AG. Effect of reduced dietary sodium on blood pressure: a meta-analysis of randomized controlled trials. JAMA. 1996;275(20):1590-1597. (PubMed)
- He FJ, MacGregor GA. Effect of longer-term modest salt reduction on blood pressure. Cochrane Database Syst Rev. 2004;(3):CD004937. (PubMed)
- Whelton PK, Appel LJ, Espeland MA, et al. Sodium reduction and weight loss in the treatment of hypertension in older persons: a randomized controlled trial of nonpharmacologic interventions in the elderly (TONE). TONE Collaborative Research Group. JAMA. 1998;279(11):839-846. (PubMed)
- The Trials of Hypertension Prevention Collaborative Research Group. Effects of weight loss and sodium reduction intervention on blood pressure and hypertension incidence in overweight people with high-normal blood pressure. The Trials of Hypertension Prevention, phase II. Arch Intern Med. 1997;157(6):657-667. (PubMed)
- Cook NR, Cohen J, Hebert PR, Taylor JO, Hennekens CH. Implications of small reductions in diastolic blood pressure for primary prevention. Arch Intern Med. 1995;155(7):701-709. (PubMed)
- Luft FC, Weinberger MH. Heterogeneous responses to changes in dietary salt intake: the salt-sensitivity paradigm. Am J Clin Nutr. 1997;65(2 Suppl):612S-617S. (PubMed)
- Weinberger MH. Salt sensitivity of blood pressure in humans. Hypertension. 1996;27(3 Pt 2):481-490. (PubMed)
- Obarzanek E, Proschan MA, Vollmer WM, et al. Individual blood pressure responses to changes in salt intake: results from the DASH-Sodium trial. Hypertension. 2003;42(4):459-467. (PubMed)
- Vollmer WM, Sacks FM, Ard J, et al. Effects of diet and sodium intake on blood pressure: subgroup analysis of the DASH-sodium trial. Ann Intern Med. 2001;135(12):1019-1028. (PubMed)
- Giner V, Poch E, Bragulat E, et al. Renin-angiotensin system genetic polymorphisms and salt sensitivity in essential hypertension. Hypertension. 2000;35(1 Pt 2):512-517. (PubMed)
- Neter JE, Stam BE, Kok FJ, Grobbee DE, Geleijnse JM. Influence of weight reduction on blood pressure: a meta-analysis of randomized controlled trials. Hypertension. 2003;42(5):878-884. (PubMed)
- Franco V, Oparil S. Salt sensitivity, a determinant of blood pressure, cardiovascular disease and survival. J Am Coll Nutr. 2006;25(3 Suppl):247S-255S. (PubMed)
- Akita S, Sacks FM, Svetkey LP, Conlin PR, Kimura G. Effects of the Dietary Approaches to Stop Hypertension (DASH) diet on the pressure-natriuresis relationship. Hypertension. 2003;42(1):8-13. (PubMed)
- Appel LJ, Moore TJ, Obarzanek E, et al. A clinical trial of the effects of dietary patterns on blood pressure. DASH Collaborative Research Group. N Engl J Med. 1997;336(16):1117-1124. (PubMed)
- Sacks FM, Svetkey LP, Vollmer WM, et al. Effects on blood pressure of reduced dietary sodium and the Dietary Approaches to Stop Hypertension (DASH) diet. DASH-Sodium Collaborative Research Group. N Engl J Med. 2001;344(1):3-10. (PubMed)
- Greenland P. Beating high blood pressure with low-sodium DASH. N Engl J Med. 2001;344(1):53-55.
- Fung TT, Chiuve SE, McCullough ML, Rexrode KM, Logroscino G, Hu FB. Adherence to a DASH-style diet and risk of coronary heart disease and stroke in women. Arch Intern Med. 2008;168(7):713-720. (PubMed)
- Chobanian AV, Hill M. National Heart, Lung, and Blood Institute Workshop on Sodium and Blood Pressure : a critical review of current scientific evidence. Hypertension. 2000;35(4):858-863. (PubMed)
- Chrysant GS. High salt intake and cardiovascular disease: is there a connection? Nutrition. 2000;16(7-8):662-664.
- du Cailar G, Ribstein J, Mimran A. Dietary sodium and target organ damage in essential hypertension. Am J Hypertens. 2002;15(3):222-229. (PubMed)
- Perry IJ, Beevers DG. Salt intake and stroke: a possible direct effect. J Hum Hypertens. 1992;6(1):23-25. (PubMed)
- Aviv A. Salt and hypertension: the debate that begs the bigger question. Arch Intern Med. 2001;161(4):507-510. (PubMed)
- Safar ME, Thuilliez C, Richard V, Benetos A. Pressure-independent contribution of sodium to large artery structure and function in hypertension. Cardiovasc Res. 2000;46(2):269-276. (PubMed)
- Nagata C, Takatsuka N, Shimizu N, Shimizu H. Sodium intake and risk of death from stroke in Japanese men and women. Stroke. 2004;35(7):1543-1547. (PubMed)
- Tuomilehto J, Jousilahti P, Rastenyte D, et al. Urinary sodium excretion and cardiovascular mortality in Finland: a prospective study. Lancet. 2001;357(9259):848-851. (PubMed)
- Tunstall-Pedoe H, Woodward M, Tavendale R, A'Brook R, McCluskey MK. Comparison of the prediction by 27 different factors of coronary heart disease and death in men and women of the Scottish Heart Health Study: cohort study. BMJ. 1997;315(7110):722-729. (PubMed)
- He J, Ogden LG, Vupputuri S, Bazzano LA, Loria C, Whelton PK. Dietary sodium intake and subsequent risk of cardiovascular disease in overweight adults. JAMA. 1999;282(21):2027-2034. (PubMed)
- Cohen HW, Hailpern SM, Fang J, Alderman MH. Sodium intake and mortality in the NHANES II follow-up study. Am J Med. 2006;119(3):275 e277-214. (PubMed)
- Alderman MH, Cohen H, Madhavan S. Dietary sodium intake and mortality: the National Health and Nutrition Examination Survey (NHANES I). Lancet. 1998;351(9105):781-785. (PubMed)
- Cook NR, Cutler JA, Obarzanek E, et al. Long term effects of dietary sodium reduction on cardiovascular disease outcomes: observational follow-up of the trials of hypertension prevention (TOHP). BMJ. 2007;334(7599):885. (PubMed)
- Cook NR, Obarzanek E, Cutler JA, et al. Joint effects of sodium and potassium intake on subsequent cardiovascular disease: The Trials of Hypertension Prevention (TOHP) Follow-up Study. Arch Intern Med. 2009;169(1)32-40. (PubMed)
- Minerals. Drug Facts and Comparisons. St. Louis: Facts and Comparisons; 2000:27-51
- Okuda T. Fluid and electrolyte disorders. In: Tierney LM, McPhee SJ, Papadakis MA, eds. Current medical diagnosis and treatment. 37th ed. Stamford: Appleton & Lange; 1998:824-849.
免責事項
ライナスポーリング研究所微量栄養素情報センターは、一般向けの食事要因、健康面、栄養補助食品、食品および飲料に関する科学的情報を提供する。著者および出版社は、本サイト上の医学的、心理学的、栄養学的カウンセリングサービスを利用しないことを合意した上で、本情報を利用することができる。本情報は、有資格の医療従事者または栄養士への相談の代わりとして利用することはできない。
本ウェブサイトに掲載されている食事要因、栄養補助食品、食品および飲料に含まれる情報は、実施可能なすべての使用法、行為、使用上の注意、副作用、および相互作用を網羅するものではない。本ウェブサイトは、個々の問題についての栄養学的、医学的助言をすることは意図していない。本サイトの電子的に利用可能な情報に基づく個人的な行為、または不作為に対する責任は、明示的に否認される。
本ウェブサイトにおける著作権を有する資料のいずれも、複製、修正、配布、表示、発信、実行、公開または販売をおこなってはならない。本ウェブサイトにハイパーリンクを貼ることは可能であるが、その際には以下の文言を付記することとする。
「本リンクは、オレゴン州立大学ライナスポーリング研究所の提供するウェブサイトへ移動します。<<名前>>は、オレゴン州立大学ライナスポーリング研究所のアフィリエイトではなく、認証されたリンクでもありません」