要約
- ターメリックはショウガ科に属するウコンの地下茎から作られる香辛料である。クルクミノイドはターメリックの黄色の元となるポリフェノール化合物で、クルクミンはターメリックに含まれるクルクミノイドの主要成分である。
- 結直腸がん(大腸がん)患者を対象とした第I相臨床試験の結果、生物活性を呈する濃度のクルクミンがクルクミンの経口補給後に消化管に到達することがわかった。そのような試験は、消化管のがんのリスクのある人々に対するさらなる臨床評価の裏付けとなっている。(詳細はこちら)
- 嚢胞性線維症の個人におけるクルクミンの安全性と有効性が臨床試験で評価されるまで、嚢胞性線維症の療法としてのクルクミンの使用を嚢胞性線維症財団は推奨しない。(詳細はこちら)
- クルクミンはヒトで抗炎症作用があることを示唆する予備的な試験がいくつかあるが、炎症性疾患の治療にクルクミンの経口補給が有効であるかを決定するには、大規模無作為化対照試験が必要である。(詳細はこちら)
- アルツハイマー病の動物モデルで有望な発見があったため、初期のアルツハイマー病の患者に対するクルクミン補給の臨床試験が進行中である。(詳細はこちら)
序説
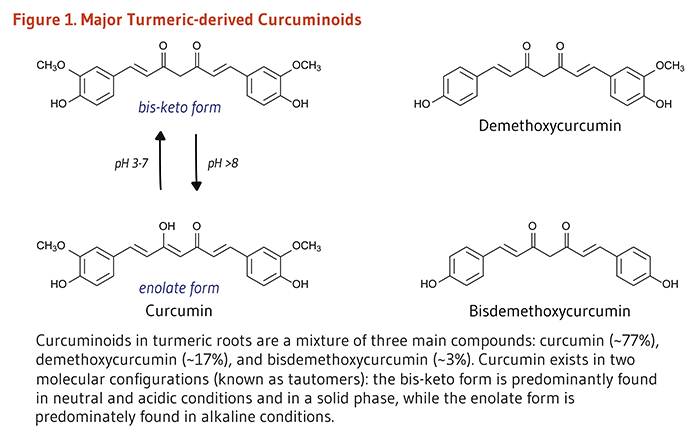
ターメリックは、ショウガ科に属するウコンの地下茎から作られる香辛料である。地下茎は地下に伸びる水平な茎で、そこからシュート(苗条)や根が出る。ターメリックの鮮やかな黄色は、クルクミノイドとして知られる脂溶性のポリフェノール色素に主に由来する(図1)。ターメリックの主要なクルクミノイドであるクルクミンは、その中で最も活性のある成分であると一般的に考えられている(1)。ターメリックに含まれるその他のクルクミノイドには、デメトキシクルクミンやビスデメトキシクルクミンなどがある。香辛料や顔料としての使い方の他に、ターメリックはインドで数世紀にわたって薬用に使われてきた。最近では、クルクミンに抗炎症作用や抗がん作用があるかもしれないというエビデンス(科学的根拠)によって、病気の予防や治療にクルクミンを使用する可能性に改めて科学的関心が寄せられている。
代謝と生物学的利用性
ヒトでの臨床試験では、経口投与されたクルクミンの全身的な生物学的利用性は比較的低く(1-3)、経口摂取の後ではクルクミンそのものではなく、大半はクルクミンの代謝物が血漿や血清に検出される(4,5)。腸や肝臓では、クルクミンはすぐにクルクミンのグルクロン酸抱合体や硫酸抱合体を形成するか、ヘキサヒドロクルクミンに還元される(図2)(6)。クルクミンの代謝物は、元の化合物と同じ生物活性を持っていない可能性がある。ある研究では、クルクミンが変化したり還元されたりした代謝物は、ヒトの培養大腸細胞で炎症を起こす酵素の発現を効果的に抑制することがクルクミンそのものよりもできなかった(7)。台湾で行われた臨床試験では、血清クルクミン濃度は経口投与後1~2時間でピークとなり、投与量が4、6、8gでピークの濃度がそれぞれ0.5、0.6、1.8マイクロモル/リットルであった(8)。クルクミンは、4g/日より低い投与量では血清中で検出できないのかもしれない。最近では、英国で行われた臨床試験で、3.6gのクルクミンの経口投与後1時間で、クルクミン、クルクミンの硫酸抱合体、およびクルクミンのグルクロン酸抱合体の血漿濃度は、10ナノモル/リットル(0.01マイクロモル/リットル)のオーダーであった(9)。クルクミンとその代謝物は、3.6g/日よりも少ない用量では血漿で検出されない可能性がある。クルクミンとそのグルクロン酸抱合体および硫酸抱合体は、3.6g/日の用量で投与された後に尿でも検出されている。経口投与されたクルクミンは、消化管の組織に蓄積するというエビデンスがある。たとえば、結直腸がんの患者が手術の前に3.6g/日のクルクミンを7日間経口摂取したところ、クルクミンはがんの結直腸組織でも正常な結直腸組織でも検出された(10)。対照的に、結直腸がんが肝臓に転移した患者の肝臓組織では、同量のクルクミンの経口摂取後にクルクミンは検出されなかった(11)。このことから、クルクミンの経口投与では消化管以外の組織にクルクミンを効果的に届けることができなかったということが示唆される。

生物活性
抗酸化活性
クルクミンは、試験管内(ガラス容器内)では活性酸素種や活性窒素種の効果的な捕捉剤である(12,13)。しかしながら、クルクミンが生体内で抗酸化物質として直接働くのかどうかは不明である。ヒトでの経口投与による生物学的利用性が限られている(「代謝と生物学的利用性」の項参照)ため、血漿および組織でのクルクミン濃度は、αトコフェロール(ビタミンE)などのその他の脂溶性抗酸化物質に比べてずっと低いであろう。しかし、クルクミンを7日間経口補給(3.6g/日)すると結直腸の悪性組織における酸化DNA付加体が減るという発見は、経口摂取されたクルクミンがDNAの酸化ダメージを抑制するほど十分な濃度で消化管に届くということを示唆している可能性がある(11)。直接的な抗酸化活性だけでなく、クルクミンは炎症を起こす酵素の活性を抑制したり、重要な細胞内抗酸化物質であるグルタチオンの合成を強化したりして、間接的に抗酸化物質として機能しているのかもしれない。
抗炎症活性
細胞膜におけるアラキドン酸の代謝は、エイコサノイドとして知られる強力な化学伝達物質を生成することで、炎症反応に重要な役割を果たしている(14)。膜リン脂質はホスホリパーゼA2(PLA2)によって加水分解され、アラキドン酸を放出する。これはシクロオキシゲナーゼ(COX)によって代謝されてプロスタグランジンとトロンボキサンを生成するか、リポキシゲナーゼ(LOX)によって代謝されてロイコトリエンを生成するのかもしれない。クルクミンは、培養細胞中ではPLA2,COX-2,および5-LOXの活性を抑制することがわかっている(15)。クルクミンは5-LOXの触媒活性を直接抑制していたが、PLA2のリン酸化反応を防いでその活性を抑制し、またCOX-2の転写を主に抑制することでその活性も抑制していた。核内因子κB(NF-κB)はDNAを結合させ、COX-2遺伝子や、誘導型一酸化窒素合成酵素(iNOS)などのその他の炎症誘発性遺伝子の転写を促進する。マクロファージなどの炎症細胞の中では、iNOSは一酸化窒素の合成に触媒作用をし、その一酸化窒素がスーパーオキシド(超酸化物)と反応して、蛋白質やDNAを損傷する可能性のある活性窒素種であるペルオキシナイトライト(過酸化亜硝酸)を生成する可能性がある。クルクミンは、NF-κBに依存する遺伝子の転写(16)や、培養細胞や動物試験におけるCOX-2やiNOSの誘発(17,18)を抑制することがわかっている。
グルタチオンの合成
グルタチオンは、細胞のストレス適応に重大な役割を果たす重要な細胞内抗酸化物質である(19)。ストレスに関連して細胞のグルタチオン濃度が上昇するのは、グルタチオン合成の律速酵素であるグルタミン酸システインリガーゼ(GCL)の発現が増大する結果である。培養細胞の研究では、GCLをコード化する遺伝子の転写を増進することでクルクミンが細胞のグルタチオン濃度を上げる可能性があることが示唆されている(20,21)。
発がん性物質の代謝に関連する生体内変換酵素への影響
生体内変換酵素は、薬物や発がん性物質を含む様々な生物活性化合物の代謝や除去に重要な役割を果している。一般に、シトクロムP450(CYP)ファミリーを含む第I相生体内変換酵素は、疎水性(脂溶性)化合物の反応性を上げるような触媒作用をし、第II相生体内変換酵素が触媒となる反応の準備をする。第II相酵素が触媒作用をする反応は、一般的に水溶性を上げてこれらの化合物の除去を促進する(22)。生体内変換酵素の活性を上げると発がんの可能性のある物質の除去を強化するかもしれないが、発がん物質の前駆体(前発がん物質)の中には、第I相酵素によって活動的な発がん物質に代謝されてしまうものもある(23)。CYP1A1は、いくつかの化学発がん性物質の代謝活性化に関係している。培養細胞や動物実験では、クルクミンは前発がん物質の生体内活性化またはCYP1A1活性の測定値を抑制することがわかっている(24-27)。第II相生体内変換酵素の活性を高めることは、一般的に発がんの可能性のある物質の除去を強化すると考えられている。いくつかの動物実験で、グルタチオンS転移酵素(GST)などの第II相酵素の活性が食事からのクルクミンによって高まったことがわかった(26,28,29)。しかしながら、0.45~3.6g/日のクルクミンを最長4ヶ月摂取しても、ヒトでの白血球のGST活性は上がらなかった(9)。
細胞周期停止とアポトーシスの誘発
細胞分裂後には、細胞周期としてまとめられる一連の段階を経てから細胞が再び分裂する。DNAの損傷の後では細胞周期は過渡的に停止し、DNAの修復をするか、損傷が修復できないものである場合には細胞死(アポトーシス)に至る経路を活性化する(30)。細胞周期の調整が不良であると、がんの発症に寄与する突然変異の伝播に至る可能性がある。クルクミンは様々な培養がん細胞株で、細胞周期の停止やアポトーシスを誘発することがわかっている(1,31-35)。クルクミンがアポトーシスを誘発するメカニズムはいろいろであるが、いくつかの細胞シグナル伝達経路に対する抑制効果を含むのかもしれない。しかし、クルクミンによるがん細胞のアポトーシスの誘発がすべての研究で見られたわけではない。クルクミンは、腫瘍抑制蛋白質p53によって誘発されるアポトーシスをヒトの培養大腸がん細胞で抑制した(36,37)。また、ある一つの研究では、培養乳がん細胞内でいくつかの化学療法薬によって誘発されるアポトーシスを、1~10マイクロモル/リットルの濃度のクルクミンが抑制したことがわかった(38)。
腫瘍浸潤および血管新生の抑制
がん細胞は、マトリックスメタロプロテイナーゼ(細胞外基質分解酵素)と呼ばれる酵素の助けを借りて正常な組織に侵入していく。培養細胞の研究では、クルクミンはいくつかのマトリックスメタロプロテイナーゼの活性を抑制することがわかっている(39-43)。浸潤性の腫瘍は急速な成長を促進するため、血管新生として知られるプロセスによって新しい血管も形成しなければならない。培養された血管内皮細胞(44,45)および動物モデル(46)において、クルクミンは血管新生を抑制したことがわかった。
注記:上記の生物活性の多くは、クルクミンを経口摂取したヒトの細胞で見られるであろうより高い濃度でクルクミンを与えた培養細胞で観察されたものであることを心に留めておくことが大切である。(「代謝と生物学的利用性」の項参照)。
疾病予防
がん
クルクミンがいくつかの異なるメカニズムで培養がん細胞でアポトーシスを誘発するという効力から、クルクミンをある種のがんの予防に使う可能性について科学的関心が喚起された(1)。口腔がん(47,48)、胃がん(49,50)、肝臓がん(51)、および大腸がん(52-54)の動物モデルでは、化学的に誘発されるがんの発症がクルクミンの経口投与で抑制されることがわかっている。APC Min/+マウスは、多数の結腸直腸腺腫(大腸腺腫)というポリープを作ることと結直腸がんのリスクが高いことが特徴の遺伝性疾患であるヒトの家族性大腸腺腫症に似たApc(大腸腺腫症)遺伝子に変異がある。クルクミンの経口投与は、APC Min/+マウスの腸腺腫の発症を抑制することがわかった(55,56)。対照的に、動物モデルでは乳がんの発症がクルクミンの経口投与で一貫して抑制されたわけではなかった(52,57,58)。
動物実験の結果は有望であり、結直腸がんで特に有望であるが、クルクミンやターメリックの高摂取がヒトのがんリスクの低下と関連があるというエビデンスは現在ほとんどない。台湾での第I相臨床試験では、口(口腔白板症)、子宮頸部(高悪性度の子宮頸部上皮内腫瘍)、皮膚(扁平上皮がん)、または胃(腸上皮化生)の前癌性病変の患者が最大8g/日のクルクミンを3ヶ月間経口摂取した効果を調べた(8)。口腔白板症の7人のうち2人で、子宮頸部上皮内腫瘍の4人のうち1人で、 扁平上皮がんの6人のうち2人で、腸上皮化生の6人のうち1人で、組織的な改善が生体組織検査で見られた。しかしながら、口腔白板症の7人のうちの1人と 子宮頸部上皮内腫瘍の4人のうち1人が、試験の終了までにがんを発症した。この研究はクルクミンの経口投与の生物学的利用性と安全性を主に調べるもので、比較のための対照群がないことから、この結果の解釈は限定されたものになる。動物研究での有望な発見の結果、腺腫のような前癌性結直腸病変に対するクルクミンの経口投与の効果を評価することを意図したヒトでの対照臨床試験がいくつか進行中である(59)。
疾病の治療
がん
様々ながんの細胞株でアポトーシスを誘発するクルクミンの効力とその低毒性によって、クルクミンを使ったがんの治療や予防の可能性への科学的興味が喚起された(60)。現在までのところ、がんの患者に対するクルクミン補給の対照臨床試験のほとんどは第I相の段階である。第I相試験は、生物学的利用性、安全性、および新しい治療法の効果への初期的なエビデンスの見極めを目的とした少人数のグループでの試験である(61)。進行した結直腸がん患者の第I相臨床試験では、最大で3.6g/日を4ヶ月間投与しても良好な許容性が示されたが、経口投与されたクルクミンの体内での生物学的利用性は低かった(62)。肝臓への転移のある結直腸がんの患者が3.6g/日のクルクミンを7日間経口摂取したら、肝臓組織でクルクミン代謝物が微量に測定されたが、クルクミンそのものは検出されなかった(11)。対照的に、進行した結直腸がんの患者が3.6g/日のクルクミンを7日間経口摂取したところ、クルクミンは正常な結直腸組織でも悪性の結直腸組織でも測定可能であった(10)。これらの発見は、クルクミンは消化管のがんではその他の組織よりも治療薬としてより効果的であろうことを示唆している。第II相の試験は、より大人数に対して新しい治療法の有効性を調べ、また短期間の副作用や安全性をさらに評価するための臨床試験である。結直腸がんの患者へのクルクミンの第II相臨床試験が現在進行中である(59)。進行したすい臓がんの患者によるクルクミンの第II相臨床試験では、クルクミンは21人の患者のうち2人の患者で何らかの抗がん作用を示したことがわかったが、クルクミンの生物学的利用性は極端に悪かった(63)。全身での生物学的利用性が低いこととクルクミンが疎水性であることから、著者たちはリポゾームに封入したクルクミンの静脈内投与を将来の臨床試験で使用することを提案している(63)。
炎症性疾患
培養細胞や動物の研究ではクルクミンの抗炎症活性が見られるものの、炎症性の病状の治療でのクルクミンの有効性を調べた対照臨床試験はほとんどない。関節リュウマチの患者18人でクルクミンと非ステロイド性の抗炎症薬(NSAID)を比べる予備的な介入試験で、クルクミン補給(1,200mg/日)を2週間した後の朝硬直、歩行時間、および関節の腫れの改善は、フェニルブタゾン(NSAID)での治療(300mg/日)を2週間行った後の改善に匹敵するものだった(64)。鼠径ヘルニアまたは水瘤の治療手術を受けた40人の男性によるプラセボ対照試験では、5日間のクルクミンの経口投与(1,200mg/日)は、手術後の浮腫、圧痛、および痛みを軽減するのにプラセボよりも効果的で、フェニルブタゾンでの治療(300mg/日)と遜色ないものだった(65)。2つの非対照試験では、クルクミンの経口投与(1,125mg/日)を12週間以上続けると、前部ぶどう膜炎と突発性の炎症性眼窩偽腫瘍という眼の炎症性の2つの症状が改善した(66,67)。しかしながら対照群がないので、これらの病状に対するクルクミンの抗炎症効果に関して結論を出すのは難しい。クルクミンの経口投与が関節リュウマチのような炎症性疾患の治療に有効であるかどうかを決定するより大規模な無作為化対照試験が必要である。
嚢胞性線維症
嚢胞性線維症は、嚢胞性線維症膜コンダクタンス制御因子(CFTR)遺伝子の突然変異で起こる遺伝性疾患である(62)。CFTRは塩素イオンチャネル(クロライドチャネル)として作用する膜貫通蛋白質で、イオンと体液の輸送に重大な役割を果たす。肺では、CFTRの突然変異は終いに粘液濃度の上昇と粘液のクリアランス(排出)の減少に至り、肺の進行性疾患を引き起こす。嚢胞性線維症の発症に寄与する最も一般的なCFTRの突然変異はDeltaF508変異であり、CFTR蛋白質が細胞膜に到達する前に間違って折りたたまれたり、分解されたりする。しかし、突然変異した蛋白質が細胞膜に入り込めば、塩素イオンチャネルとして機能する能力もいくらか残っている。DeltaF508変異のあるマウスに関する2004年の研究では、クルクミンの経口投与で異常なイオンの輸送が矯正され、これらのマウスの生存が伸びた(68)。しかしながら、ヒトと異なり、DeltaF508変異のあるマウスは肺の合併症を起こさずに、嚢胞性線維症の消化系での合併症だけを発症する。また、マウスモデルでの治療による利点は、ヒトでも常に現れるとは限らない(62)。最近では同じマウスモデルに同じ用量のクルクミンを投与した別のグループの研究では、クルクミンの有益性が再現できなかった(69)。クルクミン補給がヒトの嚢胞性線維症に有効であるかどうかは不明である。嚢胞性線維症財団が資金提供した第I相臨床試験では、欠陥のあるCFTR蛋白質の機能をクルクミンは補正できなかった。より高用量のクルクミンを使用した追跡調査が現在進行中である(70)。嚢胞性線維症の個人に対するクルクミンの安全性と有効性が臨床試験で評価されるまでは、嚢胞性線維症財団は嚢胞性線維症の治療でのクルクミンの使用を推奨しない(71)。
アルツハイマー病
アルツハイマー病では、アミロイドβと呼ばれるペプチドが凝集物(オリゴマー)を形成し、脳に集積してアミロイド斑という沈着物を作る(72)。炎症や酸化ダメージもアルツハイマー病の進行に伴っておこる(73)。クルクミンは、ガラス容器内ではアミロイドβオリゴマーの形成を抑制することが知られている(74)。アルツハイマー病の動物モデルでは、クルクミンは末梢に注入されると血液脳関門を通過することがわかっている(74)。アルツハイマー病の動物モデルでは、食事からクルクミンを摂取することで、炎症や酸化ダメージ、脳のアミロイド斑負荷、およびアミロイドβに誘発された記憶欠損に関連するバイオマーカー値が減少した(74-77)。ヒトにおいて、口から摂取されたクルクミンが血液脳関門を通過したりアルツハイマー病の進行を抑制したりするのかどうかは不明である。動物モデルでの有望な発見の結果、初期のアルツハイマー病患者へのクルクミンの経口補給の臨床試験が進行中である(59,78)。アルツハイマー病の27人に対する6ヶ月の試験の結果、最大4g/日のクルクミンの経口補給は安全であるとわかった(4)。アルツハイマー病にクルクミンの経口補給が有効であるかを決定するより大規模な対照臨床試験が必要である。
摂取源
食品の摂取源
ターメリックはウコンの地下茎をすりおろして乾燥させたものである(79)。インド、東南アジア、および中東の料理で香辛料として使用される。クルクミノイドはターメリックの約2~9%を占める(80)。クルクミンはターメリックで最も多いクルクミノイドで、クルクミノイド全体の約75%を占める。一方、デメトキシクルクミンは10~20%で、ビスデメトキシクルクミンは一般に5%未満である。カレー粉はターメリックとその他のスパイスを含むが、カレー粉のクルクミンの量は変異が大きく、比較的少ないことがしばしばである(81)。クルクミンの抽出物も食品着色料として使用される(82)。
サプリメント
クルクミン抽出物は、米国では処方箋なしで栄養補助食品として入手可能である。これらの抽出物のラベルの多くには95%クルクミノイドを含むよう規格化されていると記載されているが、そのような主張は米国食品医薬品局(FDA)によって厳密に規制されているわけではない。クルクミン製品の中にはピペリンも含むものがあり、これによってクルクミンの代謝を抑制してクルクミンの生物学的利用性が向上する可能性がある。しかし、ピペリンは薬品の代謝にも影響する可能性がある(「薬物との相互作用」の項参照)。がんの化学予防や治療的使用のための最適なクルクミンの用量はまだ確立されていない。ヒトでは3.6g/日未満の用量が生物学的に活性を持つのかどうか不明である(「代謝と生物学的利用性」の項参照)。
安全性
悪影響
米国では、ターメリックは食品添加物として安全であるとFDAによって一般的に認識(GRASと表記される合格証で認定)されている(82)。クルクミンの高用量摂取によるヒトでの深刻な悪影響の報告はない。24人の成人による用量漸増試験では、1回に最大で12gまでの経口摂取は安全であり、悪影響は用量に関連するものではなかった(5)。台湾での第I相試験では、最大8g/日のクルクミン補給を3ヶ月間しても、前がん病変または非侵襲性がんの患者は良好な耐容性を示した(8)。英国での別の臨床試験では、0.45~3.6g/日のクルクミンを4ヶ月間補給しても進行した結直腸がんの患者は一般に良好な耐容性を示したが、2人の患者が下痢になり、別の1人は吐き気があったと報告された(9)。血清アルカリホスファターゼおよび乳酸デヒドロゲナーゼ濃度の上昇も何人かの参加者で見られたが、これらの増加がクルクミン補給によるものなのかがんの進行によるものなのか不明である(1)。20~40mgのクルクミン補給は、健康な人では胆のうの収縮を促進することが報告されている(83,84)。胆のう収縮の促進は、胆のうの空化を促すことで胆石の形成リスクを下げるかもしれないが、胆石をすでに患っている患者には症状の発生リスクを上げる可能性がある。
妊娠期および授乳期
ターメリックを香辛料として食事で摂取しても妊娠や授乳に悪影響があるというエビデンスはないが、妊娠期や授乳期におけるクルクミンのサプリメント摂取の安全性は確立していない。
薬物との相互作用
クルクミンはガラス容器内で血小板凝縮を抑制することがわかっている(85,86)ことから、アスピリン、クロピドグレル(プラビックス)、ダルテパリン(フラグミン)、エノキサパリン(ラブノックス)、ヘパリン、チクロピジン(チクリッド)、およびワルファリン(クマジン)などの抗凝固薬や抗血小板作用の薬を飲んでいる患者は、クルクミン補給によって出血のリスクが高くなる可能性がある。培養乳がん細胞では、1~10マイクロモル/リットルの濃度のクルクミンは、化学療法薬、カンプトテシン、メクロレタミン、およびドキソルビシンによって誘発されるアポトーシスを抑制した(38)。乳がんの動物モデルでは、食事からのクルクミンはシクロホスファミドに誘発される腫瘍の退縮を抑制した。クルクミンの経口投与によってヒトのがんの化学療法薬を抑制するほどの高濃度でクルクミンが胸部組織に濃縮されることになるのかどうか不明である(11)が、乳がんでの化学療法を受けている女性はクルクミンのサプリメントは避けたほうがよいかもしれない(38)。クルクミンのサプリメントには、クルクミンの生物学的利用性を高めるためにピペリンを含むものもある。しかしながら、ピペリンはフェニトイン(ディランチン)、プロプラノロール(インデラル)、およびテオフィリンを含むいくつかの薬物の生物学的利用性を高めてその除去を遅らせる可能性がある(87,88)。
Authors and Reviewers
Originally written in 2005 by:
Jane Higdon, Ph.D.
Linus Pauling Institute
Oregon State University
Updated in January 2009 by:
Victoria J. Drake, Ph.D.
Linus Pauling Institute
Oregon State University
Reviewed in January 2009 by:
Chung S. Yang, Ph.D.
Professor II and Chair
Department of Chemical Biology
Ernest Mario School of Pharmacy
Rutgers, The State University of New Jersey
Copyright 2005-2026 Linus Pauling Institute
Figure Alternative Text
Figure 1. Major turmeric-derived curcuminoids
The figure shows the major turmeric-derived curcuminoids and their chemical structures.
Shown on the left are two tautomers of curcumin: the bis-keto form and the enolate form. The bis-keto form predominates in neutral and acidic conditions (pH 3-7) and in the solid phase, while the enolate form predominates in alkaline conditions (pH >8).
Shown on the right are two related compounds and their structures: demethoxycurcumin and bisdemethoxycurcumin.
The figure legend states that curcuminoids in turmeric roots are a mixture of three compounds: curcumin (~77%), demethoxycurcumin (~17%), and bisdemethoxycurcumin (~3%).
Figure 2. Curcumin metabolites
The figure shows pathways of curcumin metabolism with chemical structures. At the center, curcumin is shown. Two pathways of conjugation branch upward from curcumin: one forms curcumin sulfate, and the other forms curcumin glucuronide.
Below curcumin, a linear pathway of metabolism is shown where curcumin is reduced to dihydrocurcumin, then to tetrahydrocurcumin. This compound is further metabolized to hexahydrocurcumin and finally to octahydrocurcumin (hexahydrocurcuminol).
References
- Sharma RA, Gescher AJ, Steward WP. Curcumin: The story so far. Eur J Cancer. 2005;41(13):1955-1968. (PubMed)
- Anand P, Kunnumakkara AB, Newman RA, Aggarwal BB. Bioavailability of curcumin: problems and promises. Mol Pharm. 2007;4(6):807-818. (PubMed)
- Maheshwari RK, Singh AK, Gaddipati J, Srimal RC. Multiple biological activities of curcumin: a short review. Life Sci. 2006;78(18):2081-2087. (PubMed)
- Baum L, Lam CW, Cheung SK, et al. Six-month randomized, placebo-controlled, double-blind, pilot clinical trial of curcumin in patients with Alzheimer disease. J Clin Psychopharmacol. 2008;28(1):110-113. (PubMed)
- Lao CD, Ruffin MTt, Normolle D, et al. Dose escalation of a curcuminoid formulation. BMC Complement Altern Med. 2006;6:10. (PubMed)
- Ireson CR, Jones DJ, Orr S, et al. Metabolism of the cancer chemopreventive agent curcumin in human and rat intestine. Cancer Epidemiol Biomarkers Prev. 2002;11(1):105-111. (PubMed)
- Ireson C, Orr S, Jones DJ, et al. Characterization of metabolites of the chemopreventive agent curcumin in human and rat hepatocytes and in the rat in vivo, and evaluation of their ability to inhibit phorbol ester-induced prostaglandin E2 production. Cancer Res. 2001;61(3):1058-1064. (PubMed)
- Cheng AL, Hsu CH, Lin JK, et al. Phase I clinical trial of curcumin, a chemopreventive agent, in patients with high-risk or pre-malignant lesions. Anticancer Res. 2001;21(4B):2895-2900. (PubMed)
- Sharma RA, Euden SA, Platton SL, et al. Phase I clinical trial of oral curcumin: biomarkers of systemic activity and compliance. Clin Cancer Res. 2004;10(20):6847-6854. (PubMed)
- Garcea G, Berry DP, Jones DJ, et al. Consumption of the putative chemopreventive agent curcumin by cancer patients: assessment of curcumin levels in the colorectum and their pharmacodynamic consequences. Cancer Epidemiol Biomarkers Prev. 2005;14(1):120-125. (PubMed)
- Garcea G, Jones DJ, Singh R, et al. Detection of curcumin and its metabolites in hepatic tissue and portal blood of patients following oral administration. Br J Cancer. 2004;90(5):1011-1015. (PubMed)
- Sreejayan, Rao MN. Nitric oxide scavenging by curcuminoids. J Pharm Pharmacol. 1997;49(1):105-107. (PubMed)
- Sreejayan N, Rao MN. Free radical scavenging activity of curcuminoids. Arzneimittelforschung. 1996;46(2):169-171. (PubMed)
- Steele VE, Hawk ET, Viner JL, Lubet RA. Mechanisms and applications of non-steroidal anti-inflammatory drugs in the chemoprevention of cancer. Mutat Res. 2003;523-524:137-144. (PubMed)
- Hong J, Bose M, Ju J, et al. Modulation of arachidonic acid metabolism by curcumin and related beta-diketone derivatives: effects on cytosolic phospholipase A(2), cyclooxygenases and 5-lipoxygenase. Carcinogenesis. 2004;25(9):1671-1679. (PubMed)
- Plummer SM, Holloway KA, Manson MM, et al. Inhibition of cyclo-oxygenase 2 expression in colon cells by the chemopreventive agent curcumin involves inhibition of NF-kappaB activation via the NIK/IKK signalling complex. Oncogene. 1999;18(44):6013-6020. (PubMed)
- Brouet I, Ohshima H. Curcumin, an anti-tumour promoter and anti-inflammatory agent, inhibits induction of nitric oxide synthase in activated macrophages. Biochem Biophys Res Commun. 1995;206(2):533-540. (PubMed)
- Nanji AA, Jokelainen K, Tipoe GL, Rahemtulla A, Thomas P, Dannenberg AJ. Curcumin prevents alcohol-induced liver disease in rats by inhibiting the expression of NF-kappa B-dependent genes. Am J Physiol Gastrointest Liver Physiol. 2003;284(2):G321-327. (PubMed)
- Dickinson DA, Levonen AL, Moellering DR, et al. Human glutamate cysteine ligase gene regulation through the electrophile response element. Free Radic Biol Med. 2004;37(8):1152-1159. (PubMed)
- Dickinson DA, Iles KE, Zhang H, Blank V, Forman HJ. Curcumin alters EpRE and AP-1 binding complexes and elevates glutamate-cysteine ligase gene expression. Faseb J. 2003;17(3):473-475. (PubMed)
- Zheng S, Yumei F, Chen A. De novo synthesis of glutathione is a prerequisite for curcumin to inhibit hepatic stellate cell (HSC) activation. Free Radic Biol Med. 2007;43(3):444-453. (PubMed)
- Lampe JW, Peterson S. Brassica, biotransformation and cancer risk: genetic polymorphisms alter the preventive effects of cruciferous vegetables. J Nutr. 2002;132(10):2991-2994. (PubMed)
- Baird WM, Hooven LA, Mahadevan B. Carcinogenic polycyclic aromatic hydrocarbon-DNA adducts and mechanism of action. Environ Mol Mutagen. 2005;45(2-3):106-114. (PubMed)
- Ciolino HP, Daschner PJ, Wang TT, Yeh GC. Effect of curcumin on the aryl hydrocarbon receptor and cytochrome P450 1A1 in MCF-7 human breast carcinoma cells. Biochem Pharmacol. 1998;56(2):197-206. (PubMed)
- Rinaldi AL, Morse MA, Fields HW, et al. Curcumin activates the aryl hydrocarbon receptor yet significantly inhibits (-)-benzo(a)pyrene-7R-trans-7,8-dihydrodiol bioactivation in oral squamous cell carcinoma cells and oral mucosa. Cancer Res. 2002;62(19):5451-5456. (PubMed)
- Singh SV, Hu X, Srivastava SK, et al. Mechanism of inhibition of benzo[a]pyrene-induced forestomach cancer in mice by dietary curcumin. Carcinogenesis. 1998;19(8):1357-1360. (PubMed)
- Thapliyal R, Maru GB. Inhibition of cytochrome P450 isozymes by curcumins in vitro and in vivo. Food Chem Toxicol. 2001;39(6):541-547. (PubMed)
- Iqbal M, Sharma SD, Okazaki Y, Fujisawa M, Okada S. Dietary supplementation of curcumin enhances antioxidant and phase II metabolizing enzymes in ddY male mice: possible role in protection against chemical carcinogenesis and toxicity. Pharmacol Toxicol. 2003;92(1):33-38. (PubMed)
- Susan M, Rao MN. Induction of glutathione S-transferase activity by curcumin in mice. Arzneimittelforschung. 1992;42(7):962-964. (PubMed)
- Stewart ZA, Westfall MD, Pietenpol JA. Cell-cycle dysregulation and anticancer therapy. Trends Pharmacol Sci. 2003;24(3):139-145. (PubMed)
- Duvoix A, Blasius R, Delhalle S, et al. Chemopreventive and therapeutic effects of curcumin. Cancer Lett. 2005;223(2):181-190. (PubMed)
- Surh YJ, Chun KS. Cancer chemopreventive effects of curcumin. Adv Exp Med Biol. 2007;595:149-172. (PubMed)
- Singh S, Khar A. Biological effects of curcumin and its role in cancer chemoprevention and therapy. Anticancer Agents Med Chem. 2006;6(3):259-270. (PubMed)
- Kuttan G, Kumar KB, Guruvayoorappan C, Kuttan R. Antitumor, anti-invasion, and antimetastatic effects of curcumin. Adv Exp Med Biol. 2007;595:173-184. (PubMed)
- Kunnumakkara AB, Anand P, Aggarwal BB. Curcumin inhibits proliferation, invasion, angiogenesis and metastasis of different cancers through interaction with multiple cell signaling proteins. Cancer Lett. 2008;269(2):199-225. (PubMed)
- Moos PJ, Edes K, Mullally JE, Fitzpatrick FA. Curcumin impairs tumor suppressor p53 function in colon cancer cells. Carcinogenesis. 2004;25(9):1611-1617. (PubMed)
- Tsvetkov P, Asher G, Reiss V, Shaul Y, Sachs L, Lotem J. Inhibition of NAD(P)H:quinone oxidoreductase 1 activity and induction of p53 degradation by the natural phenolic compound curcumin. Proc Natl Acad Sci U S A. 2005;102(15):5535-5540. (PubMed)
- Somasundaram S, Edmund NA, Moore DT, Small GW, Shi YY, Orlowski RZ. Dietary curcumin inhibits chemotherapy-induced apoptosis in models of human breast cancer. Cancer Res. 2002;62(13):3868-3875. (PubMed)
- Banerji A, Chakrabarti J, Mitra A, Chatterjee A. Effect of curcumin on gelatinase A (MMP-2) activity in B16F10 melanoma cells. Cancer Lett. 2004;211(2):235-242. (PubMed)
- Ohashi Y, Tsuchiya Y, Koizumi K, Sakurai H, Saiki I. Prevention of intrahepatic metastasis by curcumin in an orthotopic implantation model. Oncology. 2003;65(3):250-258. (PubMed)
- Menon LG, Kuttan R, Kuttan G. Anti-metastatic activity of curcumin and catechin. Cancer Lett. 1999;141(1-2):159-165. (PubMed)
- Mitra A, Chakrabarti J, Banerji A, Chatterjee A, Das BR. Curcumin, a potential inhibitor of MMP-2 in human laryngeal squamous carcinoma cells HEp2. J Environ Pathol Toxicol Oncol. 2006;25(4):679-690. (PubMed)
- Hong JH, Ahn KS, Bae E, Jeon SS, Choi HY. The effects of curcumin on the invasiveness of prostate cancer in vitro and in vivo. Prostate Cancer Prostatic Dis. 2006;9(2):147-152. (PubMed)
- Thaloor D, Singh AK, Sidhu GS, Prasad PV, Kleinman HK, Maheshwari RK. Inhibition of angiogenic differentiation of human umbilical vein endothelial cells by curcumin. Cell Growth Differ. 1998;9(4):305-312. (PubMed)
- Bhandarkar SS, Arbiser JL. Curcumin as an inhibitor of angiogenesis. Adv Exp Med Biol. 2007;595:185-195. (PubMed)
- Arbiser JL, Klauber N, Rohan R, et al. Curcumin is an in vivo inhibitor of angiogenesis. Mol Med. 1998;4(6):376-383. (PubMed)
- Krishnaswamy K, Goud VK, Sesikeran B, Mukundan MA, Krishna TP. Retardation of experimental tumorigenesis and reduction in DNA adducts by turmeric and curcumin. Nutr Cancer. 1998;30(2):163-166. (PubMed)
- Li N, Chen X, Liao J, et al. Inhibition of 7,12-dimethylbenz[a]anthracene (DMBA)-induced oral carcinogenesis in hamsters by tea and curcumin. Carcinogenesis. 2002;23(8):1307-1313. (PubMed)
- Ikezaki S, Nishikawa A, Furukawa F, et al. Chemopreventive effects of curcumin on glandular stomach carcinogenesis induced by N-methyl-N'-nitro-N-nitrosoguanidine and sodium chloride in rats. Anticancer Res. 2001;21(5):3407-3411. (PubMed)
- Huang MT, Lou YR, Ma W, Newmark HL, Reuhl KR, Conney AH. Inhibitory effects of dietary curcumin on forestomach, duodenal, and colon carcinogenesis in mice. Cancer Res. 1994;54(22):5841-5847. (PubMed)
- Chuang SE, Kuo ML, Hsu CH, et al. Curcumin-containing diet inhibits diethylnitrosamine-induced murine hepatocarcinogenesis. Carcinogenesis. 2000;21(2):331-335. (PubMed)
- Pereira MA, Grubbs CJ, Barnes LH, et al. Effects of the phytochemicals, curcumin and quercetin, upon azoxymethane-induced colon cancer and 7,12-dimethylbenz[a]anthracene-induced mammary cancer in rats. Carcinogenesis. 1996;17(6):1305-1311. (PubMed)
- Rao CV, Rivenson A, Simi B, Reddy BS. Chemoprevention of colon carcinogenesis by dietary curcumin, a naturally occurring plant phenolic compound. Cancer Res. 1995;55(2):259-266. (PubMed)
- Kawamori T, Lubet R, Steele VE, et al. Chemopreventive effect of curcumin, a naturally occurring anti-inflammatory agent, during the promotion/progression stages of colon cancer. Cancer Res. 1999;59(3):597-601. (PubMed)
- Mahmoud NN, Carothers AM, Grunberger D, et al. Plant phenolics decrease intestinal tumors in an animal model of familial adenomatous polyposis. Carcinogenesis. 2000;21(5):921-927. (PubMed)
- Perkins S, Verschoyle RD, Hill K, et al. Chemopreventive efficacy and pharmacokinetics of curcumin in the min/+ mouse, a model of familial adenomatous polyposis. Cancer Epidemiol Biomarkers Prev. 2002;11(6):535-540. (PubMed)
- Huang MT, Lou YR, Xie JG, et al. Effect of dietary curcumin and dibenzoylmethane on formation of 7,12-dimethylbenz[a]anthracene-induced mammary tumors and lymphomas/leukemias in Sencar mice. Carcinogenesis. 1998;19(9):1697-1700. (PubMed)
- Singletary K, MacDonald C, Iovinelli M, Fisher C, Wallig M. Effect of the beta-diketones diferuloylmethane (curcumin) and dibenzoylmethane on rat mammary DNA adducts and tumors induced by 7,12-dimethylbenz[a]anthracene. Carcinogenesis. 1998;19(6):1039-1043. (PubMed)
- National Institutes of Health. Clinical Trials.gov. 2005. Available at: http://clinicaltrials.gov/ Accessed 1/13/09.
- Karunagaran D, Rashmi R, Kumar TR. Induction of apoptosis by curcumin and its implications for cancer therapy. Curr Cancer Drug Targets. 2005;5(2):117-129. (PubMed)
- National Institutes of Health. An Introduction to Clinical Trials. 2005. Available at: http://clinicaltrials.gov/ct/info/whatis. Accessed 1/13/09.
- Mall M, Kunzelmann K. Correction of the CF defect by curcumin: hypes and disappointments. Bioessays. 2005;27(1):9-13. (PubMed)
- Dhillon N, Aggarwal BB, Newman RA, et al. Phase II trial of curcumin in patients with advanced pancreatic cancer. Clin Cancer Res. 2008;14(14):4491-4499. (PubMed)
- Deodhar SD, Sethi R, Srimal RC. Preliminary study on antirheumatic activity of curcumin (diferuloyl methane). Indian J Med Res. 1980;71:632-634.
- Satoskar RR, Shah SJ, Shenoy SG. Evaluation of anti-inflammatory property of curcumin (diferuloyl methane) in patients with postoperative inflammation. Int J Clin Pharmacol Ther Toxicol. 1986;24(12):651-654. (PubMed)
- Lal B, Kapoor AK, Agrawal PK, Asthana OP, Srimal RC. Role of curcumin in idiopathic inflammatory orbital pseudotumours. Phytother Res. 2000;14(6):443-447. (PubMed)
- Lal B, Kapoor AK, Asthana OP, et al. Efficacy of curcumin in the management of chronic anterior uveitis. Phytother Res. 1999;13(4):318-322. (PubMed)
- Egan ME, Pearson M, Weiner SA, et al. Curcumin, a major constituent of turmeric, corrects cystic fibrosis defects. Science. 2004;304(5670):600-602. (PubMed)
- Song Y, Sonawane ND, Salinas D, et al. Evidence against the rescue of defective DeltaF508-CFTR cellular processing by curcumin in cell culture and mouse models. J Biol Chem. 2004;279(39):40629-40633. (PubMed)
- Cystic Fibrosis Foundation. Drug Development Pipeline. [Web page]. http://www.cff.org/research/DrugDevelopmentPipeline/. Accessed 1/13/09.
- Cystic Fibrosis Foundation. Curcumin: Information for Patients and Families. 2004. http://www.cff.org/images/customcontent/CurcuminQAFinal.pdf. Accessed 1/13/09.
- Gandy S. The role of cerebral amyloid beta accumulation in common forms of Alzheimer disease. J Clin Invest. 2005;115(5):1121-1129. (PubMed)
- Cole GM, Morihara T, Lim GP, Yang F, Begum A, Frautschy SA. NSAID and Antioxidant Prevention of Alzheimer's Disease: Lessons from In Vitro and Animal Models. Ann N Y Acad Sci. 2004;1035:68-84. (PubMed)
- Yang F, Lim GP, Begum AN, et al. Curcumin inhibits formation of amyloid beta oligomers and fibrils, binds plaques, and reduces amyloid in vivo. J Biol Chem. 2005;280(7):5892-5901. (PubMed)
- Lim GP, Chu T, Yang F, Beech W, Frautschy SA, Cole GM. The curry spice curcumin reduces oxidative damage and amyloid pathology in an Alzheimer transgenic mouse. J Neurosci. 2001;21(21):8370-8377. (PubMed)
- Frautschy SA, Hu W, Kim P, et al. Phenolic anti-inflammatory antioxidant reversal of Abeta-induced cognitive deficits and neuropathology. Neurobiol Aging. 2001;22(6):993-1005. (PubMed)
- Pan R, Qiu S, Lu DX, Dong J. Curcumin improves learning and memory ability and its neuroprotective mechanism in mice. Chin Med J (Engl). 2008;121(9):832-839. (PubMed)
- Kelley BJ, Knopman DS. Alternative medicine and Alzheimer disease. Neurologist. 2008;14(5):299-306. (PubMed)
- Joe B, Vijaykumar M, Lokesh BR. Biological properties of curcumin-cellular and molecular mechanisms of action. Crit Rev Food Sci Nutr. 2004;44(2):97-111. (PubMed)
- Lechtenberg M, Quandt B, Nahrstedt A. Quantitative determination of curcuminoids in Curcuma rhizomes and rapid differentiation of Curcuma domesticaVal. and Curcuma xanthorrhiza Roxb. by capillary electrophoresis. Phytochem Anal. 2004;15(3):152-158. (PubMed)
- Tayyem RF, Heath DD, Al-Delaimy WK, Rock CL. Curcumin content of turmeric and curry powders. Nutr Cancer. 2006;55(2):126-131. (PubMed)
- US Food and Drug Administration. Food Additive Status List. 2005. http://www.cfsan.fda.gov/~dms/opa-appa.html. Accessed 1/13/09.
- Rasyid A, Lelo A. The effect of curcumin and placebo on human gall-bladder function: an ultrasound study. Aliment Pharmacol Ther. 1999;13(2):245-249. (PubMed)
- Rasyid A, Rahman AR, Jaalam K, Lelo A. Effect of different curcumin dosages on human gall bladder. Asia Pac J Clin Nutr. 2002;11(4):314-318. (PubMed)
- Shah BH, Nawaz Z, Pertani SA, et al. Inhibitory effect of curcumin, a food spice from turmeric, on platelet-activating factor- and arachidonic acid-mediated platelet aggregation through inhibition of thromboxane formation and Ca2+ signaling. Biochem Pharmacol. 1999;58(7):1167-1172. (PubMed)
- Srivastava KC, Bordia A, Verma SK. Curcumin, a major component of food spice turmeric (Curcuma longa) inhibits aggregation and alters eicosanoid metabolism in human blood platelets. Prostaglandins Leukot Essent Fatty Acids. 1995;52(4):223-227. (PubMed)
- Bano G, Raina RK, Zutshi U, Bedi KL, Johri RK, Sharma SC. Effect of piperine on bioavailability and pharmacokinetics of propranolol and theophylline in healthy volunteers. Eur J Clin Pharmacol. 1991;41(6):615-617. (PubMed)
- Velpandian T, Jasuja R, Bhardwaj RK, Jaiswal J, Gupta SK. Piperine in food: interference in the pharmacokinetics of phenytoin. Eur J Drug Metab Pharmacokinet. 2001;26(4):241-247. (PubMed)
免責事項
ライナスポーリング研究所微量栄養素情報センターは、一般向けの食事要因、健康面、栄養補助食品、食品および飲料に関する科学的情報を提供する。著者および出版社は、本サイト上の医学的、心理学的、栄養学的カウンセリングサービスを利用しないことを合意した上で、本情報を利用することができる。本情報は、有資格の医療従事者または栄養士への相談の代わりとして利用することはできない。
本ウェブサイトに掲載されている食事要因、栄養補助食品、食品および飲料に含まれる情報は、実施可能なすべての使用法、行為、使用上の注意、副作用、および相互作用を網羅するものではない。本ウェブサイトは、個々の問題についての栄養学的、医学的助言をすることは意図していない。本サイトの電子的に利用可能な情報に基づく個人的な行為、または不作為に対する責任は、明示的に否認される。
本ウェブサイトにおける著作権を有する資料のいずれも、複製、修正、配布、表示、発信、実行、公開または販売をおこなってはならない。本ウェブサイトにハイパーリンクを貼ることは可能であるが、その際には以下の文言を付記することとする。
「本リンクは、オレゴン州立大学ライナスポーリング研究所の提供するウェブサイトへ移動します。<<名前>>は、オレゴン州立大学ライナスポーリング研究所のアフィリエイトではなく、認証されたリンクでもありません」